Лікування фіброзної гіперплазії, спричиненої протезами, за допомогою вуглекислотного лазера
Машинний переклад
Оригінальна стаття написана мовою EN (посилання для прочитання) .
Анотація
Гіперплазія волокнистої тканини, викликана протезами, є адаптивним ростом, розташованим над м'якими тканинами вестибулярного жолоба, викликаним хронічним подразненням від погано адаптованих протезів. Гемостатичні властивості вуглекислотного лазера широко описуються як корисний інструмент для оральної хірургії. Метою цієї статті є представлення випадку великої гіперплазії волокнистої тканини, викликаної протезами, у пацієнта, який приймає антитромботичні препарати, що демонструє корисність вуглекислотного лазера для лікування цієї ураження. Процедура ексцизії була виконана за допомогою вуглекислотного лазера з додатковою вестибулопластикою під місцевою анестезією. Через три тижні загоєння рани завершилося без ускладнень. Ускладнень у вигляді кровотечі, болю, набряку або інфекції не було зафіксовано. Через рік після лікування пацієнт не мав рецидиву. Використання вуглекислотних лазерів може бути дуже корисним при ексцизії цього типу патології.
Вступ
Гіперплазія волокнистої тканини, викликана протезами (епуліс фіссуратум), є адаптивним ростом, розташованим над м'якими тканинами вестибулярного жолоба, викликаним хронічним подразненням від погано адаптованих протезів з різними ступенями гіпертрофії та гіперплазії. Термін епуліс, вперше використаний Вірхофом, що означає "над яснами", не є доречним для цих уражень, оскільки уражена слизова оболонка є оральною слизовою оболонкою вестибулярного жолоба, а не ясенною слизовою оболонкою. З іншого боку, термін епуліс стосується лише місця. У цьому контексті ми погоджуємося з деякими авторами, які вважають за краще називати ці ураження гіперплазією волокнистої тканини, викликаною протезами.
Клінічно ця адаптивна ураження проявляється піднятою сидячою ураженням у формі складок, з гладкою поверхнею та нормальною кольоровою слизовою оболонкою. Залежно від інтенсивності травми, поверхня може стати виразковою. Остаточне лікування - це ексцизія з відповідною протезною реконструкцією. Рецидиви рідкісні, якщо усунути джерела травми та/або звички пацієнта і забезпечити відповідну протезну реабілітацію. У сучасних суспільствах зростає кількість літніх пацієнтів, які лікуються антикоагулянтною терапією, особливо тих, хто має загальні системні захворювання, такі як серцево-судинні захворювання. У цьому контексті зростає ризик кровотечі під час стоматологічних хірургічних процедур.
Лазери високої потужності є одним з найбільших технологічних досягнень у стоматології. У 1989 році був представлений перший лазер, спеціально розроблений для використання в стоматології, вуглекислотний (CO2) лазер. CO2 лазер випромінює енергію з довжиною хвилі 10,6 мкм в інфрачервоній зоні, яка поглинається водою. Високий вміст води в м'яких тканинах рота робить цей лазер корисним інструментом у м'якій хірургії рота з багатьма перевагами в порівнянні з традиційною хірургією, включаючи зручне видалення слизової оболонки, високу точність у знищенні тканин, відмінну гемостазу з безкровним полем і відсутність необхідності в швах. Крім того, безконтактна хірургія та бактерицидні властивості лазерного променя мінімізують можливість післяопераційної інфекції, болю та набряку. Гемостатична здатність CO2 лазера широко описується як корисний інструмент для хірургії рота у пацієнтів, які страждають від порушень крові. Метою цієї статті є представлення корисності CO2 лазера в лікуванні фіброзної гіперплазії, викликаної протезом верхньої щелепи, у пацієнта з антикоагулянтною терапією.
Клінічний випадок
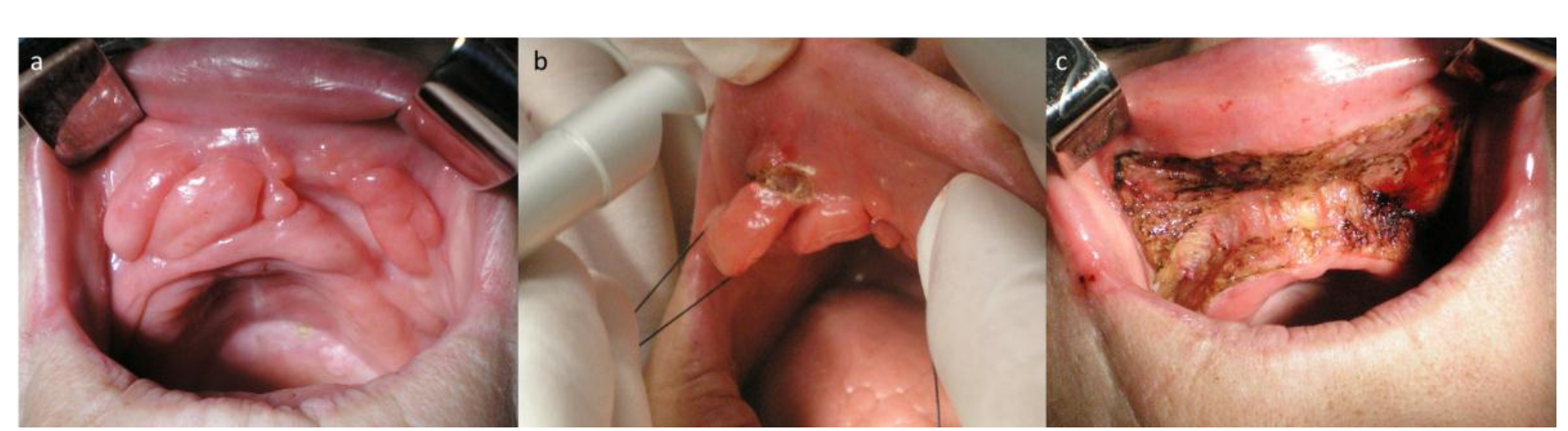
56-річна жінка була направлена до відділення оральної медицини для оцінки ураження в верхній щелепі. Вона повідомила про збільшення верхньої щелепи, яке тривало шість місяців, з дискомфортом у роті протягом останнього місяця. У пацієнтки був анамнез артеріальної гіпертензії та серцевої недостатності відповідно 10 і 3 роки. Звичайні ліки включали тіколопідин 250 мг двічі на день та каптоприл 25 мг. При оральному обстеженні була виявлена фіброзна маса розміром 6 x 3 см, з численними складками, щільна і з нормальною кольоровою слизовою оболонкою, розташована на вестибулярній борозні верхньої щелепи (Рис. 1). Вона використовувала верхні та нижні неправильно підібрані зубні протези. Лімфаденопатії шийної або підщелепної області не було. Попередній діагноз фіброзної гіперплазії, спричиненої протезами, був встановлений. Загальний аналіз крові, тести на коагуляцію та загальна біохімія були в межах норми з INR 3.1. Артеріальний тиск був зафіксований перед операцією (діастолічний 90 мм рт. ст. і систолічний 132 мм рт. ст.). Вона не припиняла прийом своїх ліків перед операцією за згодою лікаря. Це ураження було лікувано під місцевою анестезією за допомогою CO2 (10600 нм) лазера (DEKA™ Smart US20D, Флоренція, Італія), фокусуючи промінь для слизового розрізу (Рис. 2),
в імпульсному режимі (50 Гц), потужність 4,5 Вт, пляма 1 мм, PD 573,25 Вт/см2, флуенс 11,46 Дж/см2 та дефокалізація для коагуляції тканин у безперервному режимі, потужність 7 Вт, пляма 2 мм, PD 222,93 Вт/см2 та флуенс 222,93 Дж/см2. Дотримувалися звичайних заходів безпеки для захисту оператора, пацієнта та асистента. Додатково до видалення фіброзної гіперплазії, викликаної протезами, ми виконали вестибулопластику для підтримки рівномірної глибини сулькуса (Рис. 3). Негайно після операції старий протез був перероблений з використанням кондиціонера для тканин (Viscogel, DENTSPLY®, Констанц, Німеччина). Шви не використовувалися, і рана була дозволена зажити вторинним наміром. Було призначено парацетамол 1 г через 8 годин протягом 3 днів та полоскання рота 0,12% хлоргексидину. Видалені тканини були надіслані на рутинне гістологічне дослідження з вказівкою на ексцизію CO2 лазером. Через три тижні загоєння рани завершилося без ускладнень (Рис. 4). Пацієнт не повідомляв про післяопераційний біль або набряк. Гістопатологічний звіт виявив "фіброзну тканину з деякою інфільтрацією запальних клітин, обмежену багатошаровим епітелієм з акантозом, що підтверджує фіброзну гіперплазію, викликану протезами" (Рис. 5). Потім була надана відповідна нова протезна реабілітація. Пацієнт відвідав прийом через місяць, а потім через рік, не виявляючи ознак рецидиву.
Обговорення
Більшість фіброзної гіперплазії, викликаної протезами, виникає в передній ділянці верхньої або нижньої щелепи. Більше 60% випадків мають множинну презентацію, як було спостережено в нашому випадку. Вони частіше зустрічаються у жінок та у людей похилого віку.
Хірургічна ексцизія є остаточним лікуванням фіброзної гіперплазії, викликаної протезами, завжди з відповідною протезною реконструкцією. Лікування зазвичай проводиться за допомогою традиційної хірургічної ексцизії з використанням скальпеля. Можуть бути використані й інші методи лікування, такі як лазер, електротом або кріохірургія рідким азотом. Однак електротом пов'язаний з підвищеним термічним денатураційним ефектом і може викликати певну електроконтрактильність підлягаючих м'язових тканин. Кріохірургія може мати недостатню точність різання. Лазер CO2 може бути корисним інструментом у цьому типі хірургії завдяки своїй точності різання та унікальній безконтактній техніці, що знижує ризик інфекції та стерилізації хірургічної рани. Однією з основних переваг над традиційними хірургіями є відмінна гемостаз. З цих причин немає потреби в швах, і рана дозволяється загоюватися вторинним інтенсивним загоєнням. Як і пацієнт, представлений у цій статті, багато літніх пацієнтів отримують антикоагулянтні препарати. Як свідчать нещодавні рекомендації, пацієнт і кардіолог віддали перевагу не припиняти цей препарат під час оральної хірургії.
Протягом останніх років лазерна гемостаз встановилася як альтернатива традиційним технікам. Гáспар і Сабо, 1989, не виявили значних відмінностей між групою пацієнтів з геморагічною діатезою та контрольними пацієнтами щодо тривалості операції, ступеня кровотечі, загоєння рани та ускладнень. Автори роблять висновок, що CO2 лазер з високою енергією виявився добре застосовним у галузі оральної хірургії завдяки своєму відмінному гемостатичному ефекту. У нашому випадку ми спостерігали хороший контроль кровотечі. Ми вважаємо, що CO2 лазер є цінною допомогою у лікуванні цих пацієнтів. Кровоносні судини діаметром менше 0,5 мм спонтанно закупорюються, що забезпечує відмінну видимість (безкровне операційне поле) та точність при дисекції через тканинні площини. У порівнянні з хірургією скальпелем на поверхні утворюється коагулят денатурованого колагену, а при лазерній стерилізації рани гостра запальна реакція затримується і є мінімальною, з невеликою кількістю міофібробластів і, отже, малою контрактурою рани.
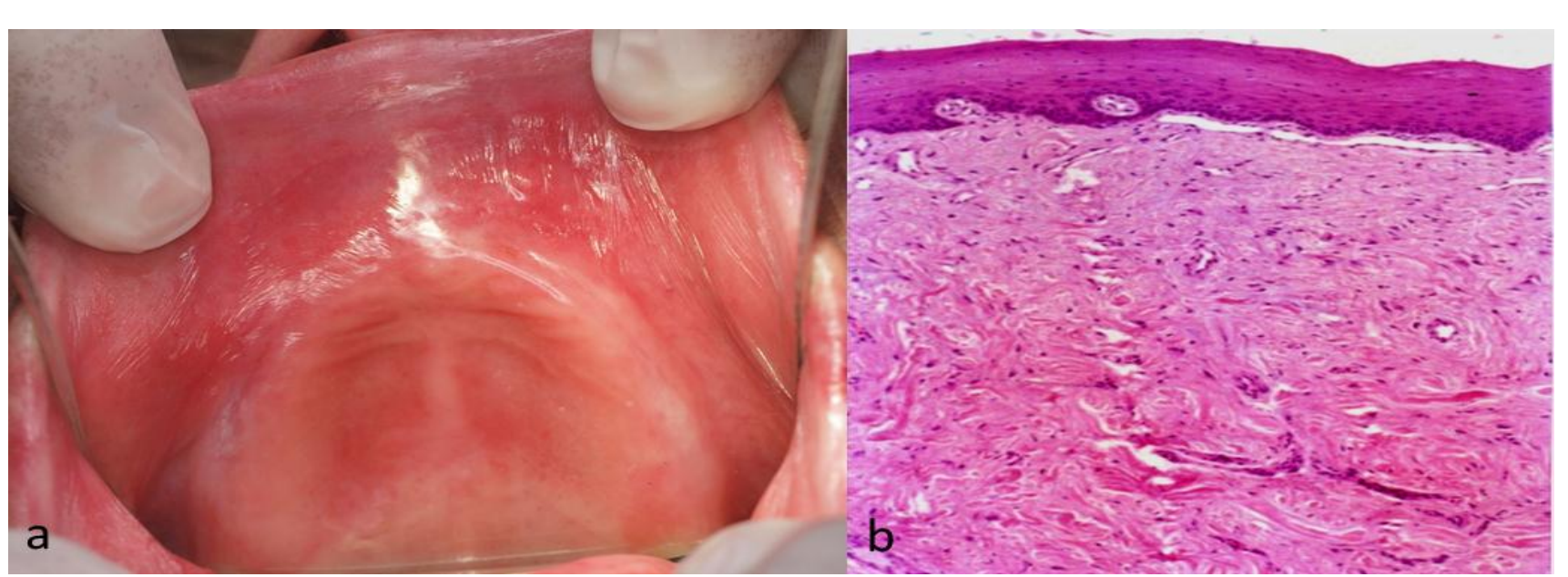
Додатковими та важливими перевагами лазерів, як ми спостерігали у нашому випадку, є мінімальні післяопераційні скарги, такі як біль, інфекція та набряк. Зважаючи на розмір ураження, представленого тут, вражає, що під час операційного та післяопераційного періоду біль був відсутній. Це важлива перевага лазерного лікування, про яку повідомляють багато авторів. Pogrel та ін., 1990, приписали це зменшення болю тому, що запальна реакція, пов'язана з застосуванням CO2 лазера, зменшується, оскільки відбувається герметизація кровоносних та лімфатичних судин, що запобігає екстравазації рідин, відповідальних за запалення та біль. Більше того, лазерне опромінення викликає герметизацію нервових закінчень у зоні хірургічного контакту, а денатурований колагеновий шар, що утворюється на поверхні хірургічної рани, служить для ізоляції від рідин ротової порожнини. Однак при вторинному загоєнні рани повторна епітелізація затримується, і рани потребують більше часу для повторної епітелізації. Процес загоєння закінчується за три тижні з анатомічною цілісністю сосочка. Рецидиви є рідкісними, якщо джерела травми та/або звички пацієнта усунуті, а також забезпечено відповідну протезну реконструкцію.
У цьому погляді ми вважаємо, що ексцизія лазером CO2 з виготовленням нових протезів є найкращим лікуванням для цих пацієнтів. Лазер CO2 ефективно видалив це велике ураження і контролював кровотечу під час хірургічної процедури та післяопераційного періоду. Keng & Loh, 1992, у 20 пацієнтів, яким була проведена ексцизія епулісу фіссураціуму лазером CO2, спостерігали контроль кровотечі у більшості пацієнтів, без геморагії в післяопераційний період, а також помітну відсутність болю та інфекції. Tuncer та ін., 2010, спостерігали, що лазер CO2 був ефективним інструментом для ексцизійних біопсій м'яких тканин з мінімальними внутрішньоопераційними та післяопераційними ускладненнями та хорошим контролем болю в порівнянні з хірургією скальпелем.
Висновок
Враховуючи внутрішні якості лазера CO2 при використанні для хірургії оральних тканин, цей варіант лікування може бути дуже корисним при фіброзній гіперплазії, викликаній протезами, особливо у пацієнтів з геморагічною діатезою або антикоагулянтною терапією.
Луїс Сілва Монтейро, Жоао Музінью, Марко Андре Мартінс
Посилання
- Тамаріт-Боррас М, Дельгадо-Моліно Е, Беріні-Айтес Л, Гей-Ескода К. Видалення гіперпластичних уражень ротової порожнини. Ретроспективне дослідження 128 випадків. Med Oral Patol Oral Cir Bucal 2005;10(2):151-62.
- Реджезі JA, Счубба JJ, Джордан Р. Оральна патологія. Клініко-патологічні кореляції. 5-е видання, Сандерс: 2008.
- Нікколі-Фільо W, Невес AC, Пенна LP, Серайдаріан PI, Ріва Р. Видалення епулісу фіссураційного, асоційованого з вестибулопластикою за допомогою лазера вуглекислого газу. Lasers Med Sci 1999;14:203-6.
- ван Дірмен DE, Аартман IH, Баарт JA, Хоогстратен J, ван дер Ваал I. Стоматологічне управління пацієнтами, які використовують антитромбоцитарні препарати: критична оцінка існуючих рекомендацій. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2009;107(5):616-24.
- Фрейм J. Останні досягнення з лазером CO2 в оральній хірургії. Int Con Ser 2003;1248:3-7.
- Кенг SB, Ло ХС. Лікування епулісу фіссураційного ротової порожнини за допомогою лазерної хірургії CO2. J Clin Laser Med Surg 1992;10(4):303-6.
- Тунчер I, Озчакір-Томрук C, Сенчіфт К, Джолоуглу С. Порівняння традиційної хірургії та CO2 лазера при патологіях м'яких тканин у ротовій порожнині та оцінка супутнього термічного пошкодження. Photomed Laser Surg 2010;28(1):75-9.
- Гама SK, де Араужо TM, Пінейро AL. Переваги використання лазера CO2 в ортодонтії. Lasers Med Sci 2008;23(4):459-65.
- Гаспар Л, Сабо Г. Значення гемостатичного ефекту лазерів в оральній хірургії. Orv Hetil 1989;130(41):2207-10.
- Аргюеро-Гонсалес М, Еспанья-Тост JA, Веласко-Віванко V, Гей-Ескода К. Спадкова геморагічна телангіектазія (хвороба Ренду-Ослера-Вебера). Презентація випадку. Одонтологія 1994:2:15-22.
- Еспанья JA, Веласко V, Гей-Ескода К, Беріні Л, Арнабат J, ред. Застосування лазера CO2 в стоматології. Мадрид: Ергон; 1995.
- Аннерот Г, Сігурдсон А. Гіперпластичні ураження ясен та альвеолярної слизової. Дослідження 175 випадків. Acta Odontol Scand 1983;41(2):75-86.
- Кангер EM, Челенк P, Кайпмаз С. Гіперплазія, пов'язана з протезами: клінічне дослідження групи населення Туреччини. Braz Dent J 2009;20:243-8.
- Погрел МА. Застосування лазера та кріохірургії в оральній та щелепно-лицевій хірургії. Curr Opin Dent 1991;1(3):263-70.
- Нойкам FW, Стельцле Ф. Лазерне лікування пухлин в оральній та щелепно-лицевій хірургії. Physics Procedia 2010;5:91-100.
- Махлер П, Пуйссегур В, Рокка JP, Де Мур Р, Наммур С. Препротезна хірургія беззубої верхньої щелепи: вестибулярне поглиблення за допомогою лазера CO2. Rev Belge Med Dent 2009;64(3):108-13.
- Горч HH, Деппе H. Нові аспекти лазерів в оральній та краніомаксилярній хірургії. Med Las Appl 2005;20:7-11.
- Гаспар Л, Сабо Г. Прояв переваг та недоліків використання лазера CO2 в оральній хірургії. J Clin Laser Med Surg 1990;8(1):39-43.
- Погрел МА, Єн ЧК, Хансен ЛС. Порівняння лазера вуглекислого газу, кріохірургії рідким азотом та ранових ушкоджень від скальпеля в загоєнні. Oral Surg Oral Med Oral Pathol 1990;69:269-73.
- Фішер SE, Фрейм JW. Вплив хірургічного лазера вуглекислого газу на оральні тканини. Br J Oral Maxillofac Surg 1984;22:414-25.