Результати лікування зубними імплантатами у пацієнтів, які проходять активну терапію алендронатом: результати трирічного спостереження в рамках багатопрофільного проспективного дослідження.
Машинний переклад
Оригінальна стаття написана мовою EN (посилання для прочитання) .
Анотація
Мета: Оцінити 3-річні клінічні та радіографічні дані фіксованих зубних протезів на імплантатах, які були встановлені пацієнтам, що приймали алендронат 35–70 мг щотижня протягом щонайменше 3 років до встановлення імплантатів.
Матеріали та методи: Сорок послідовних пацієнтів, які лікувалися пероральними біфосфонатами і потребували відновлення на основі імплантатів, були залучені в двох приватних центрах між січнем 2008 року та груднем 2011 року. Імплантати були встановлені за допомогою мінімально інвазивного підходу під антибактеріальним та антибіотиковим лікуванням, через 6 місяців після припинення прийому алендронату. Після 4 місяців зануреного загоєння імплантати піддалися протезуванню. Підтримка гігієни та клінічні оцінки планувалися кожні 4 місяці протягом 3 років. Критеріями оцінки були: успіх імплантатів та протезів, показники виживання, будь-які спостережувані клінічні ускладнення, ремоделювання країв кістки, глибина пародонтальних кишень і кровотеча під час зондування.
Результати: Наприкінці дослідження вісім пацієнтів вибули. Остаточний розмір вибірки склав 32 послідовних частково або повністю беззубих пацієнтів (32 жінки; середній вік 64,6 років) з 98 зануреними імплантатами. У лише одного пацієнта імплантат у верхній щелепі не прижився під час періоду загоєння. Жоден протез не зазнав невдачі протягом всього періоду спостереження, і жодних серйозних ускладнень не було зафіксовано. Успіх імплантатів і протезів призвів до загального рівня виживання 98, 98% і 100% відповідно. Середня втрата краєвої кістки за три роки склала 1,35 ± 0,21 (CI 95% 1,24–1,38). Успішні параметри м'яких тканин були виявлені навколо всіх імплантатів.
Висновки: Оральна терапія біфосфонатами, здається, не мала значного впливу на виживання та успіх імплантатів у разі точного вибору часу лікування, мінімально інвазивного хірургічного підходу та постійного спостереження. Потрібні подальші проспективні дослідження з залученням більших вибірок і тривалішими термінами спостереження для підтвердження цих результатів.
Вступ
Остеопороз — це прогресуюче системне захворювання скелета, яке характеризується низькою масою кістки та мікроархітектурною деградацією кісткової тканини, що призводить до збільшення крихкості кісток і схильності до переломів (Kanis et al. 2008). Найбільш поширене медичне лікування остеопорозу передбачає використання біфосфонатів (БП) (Bernabei et al. 2014). У 2009 році Управління з контролю за продуктами і ліками США схвалило річну ін'єкцію золедронової кислоти для профілактики остеопорозу у менопаузальних популяціях (Khosla 2009). Біфосфонати є стабільними аналогами природних неорганічних пірофосфатів і класифікуються як антирезорбтивні препарати (Fleisch et al. 1966), які використовуються для зменшення активності остеокластів, запобігання резорбції кістки та зменшення її обігу (Reszka & Rodan 2004). Вони зазвичай використовуються для лікування захворювань, що впливають на метаболізм кісток, включаючи множинну мієлому, вторинну гіперкальціємію, спричинену злоякісними пухлинами, метастази в кістках при метастатичному раку простати або молочної залози, хворобу Педжета, а також остеопороз (Sarzi Amadè et al. 2008).
Дія БП залежить від хімічної структури препарату. Традиційно БП поділяють на препарати, що не містять азоту (non-N-BPs), та препарати, що містять азот (N-BPs). Ненітрогенові біфосфонати метаболізуються в клітині в сполуки, які замінюють термінальну пірофосфатну частину АТФ, формуючи нефункціональну молекулу, яка конкурує з аденозинтрифосфатом (АТФ) у клітинному енергетичному метаболізмі. Остеокласт ініціює апоптоз і гине, що призводить до загального зменшення розпаду кістки. Додавання аміногрупи до кінця бічного ланцюга підвищує потенцію препарату; однак механізм дії азотовмісних БП менш відомий. Згідно з дослідженням Резьки та Родана (2004), N-BPs інгібують фермент фарнезилдисфосфатсинтазу в шляху біосинтезу холестерину та порушують шлях ізопренілізації, що інгібує білки та інші фактори, які відіграють обмежувальну роль у резорбції кістки остеокластами. N-BPs накопичуються в максимальній концентрації в кістковій матриці та в остеокластах, переважно протягом перших 24–48 годин лікування. Кінцевим результатом є дисфункція клітин остеокластів і їхня загибель (Jones et al. 2001). Внаслідок цього інгібування нормальної резорбції кістки спостерігається зменшення обігу кістки, збільшення щільності кістки, покращення мінералізації та зменшення ризику переломів (Jones et al. 2001).
Алендронат - це азотовмісний біфосфонат, який широко використовувався для лікування остеопорозу (Tsetsenekou et al. 2012). Вплив місцево та/або системно введеного алендронату на остеоінтеграцію був ретельно оцінений у експериментах на тваринах (Abtahi et al. 2013). Однак, згідно з робочою групою, створеною Американським товариством з дослідження кісток і мінералів, існує мало інформації про побічні ефекти пероральних N-БП (Kos et al. 2010).
Два недавні систематичні огляди літератури свідчать про те, що прийом пероральних БП не вплинув на короткострокові (1–4 роки) показники виживання імплантатів, навіть коли виникали ускладнення (Madrid & Sanz 2009; Ata-Ali et al. 2014). Проте, все ще бракує проспективних досліджень, що повідомляють про виживання імплантатів та показники успіху. Оскільки загальноприйняті рекомендації ще не були опубліковані, клінічне управління пов'язаним з біфосфонатами ONJ залишається спірним (Rupel et al. 2014). З 2003 року публікувалися звіти про некроз щелепних кісток, який, можливо, пов'язаний з введенням біфосфонатів (Hasegawa et al. 2012). Велися дискусії щодо ризиків, пов'язаних з проведенням пероральних хірургічних процедур, зокрема пересадки кістки та встановлення імплантатів, у пацієнтів, які приймають пероральні БП (Sarzi Amadè et al. 2008; Memon et al. 2012; Kwon et al. 2014). Ті ж автори дійшли висновку, що запобігання ONJ, пов'язаному з БП, не є повністю можливим, але неінвазивні профілактичні процедури можуть допомогти зменшити його частоту (Sarzi Amadè et al. 2008; Memon et al. 2012; Kwon et al. 2014). Американська асоціація оральних і щелепно-лицевих хірургів рекомендує пацієнтам призупинити прийом БП за 3 місяці до та 3 місяці після пероральної хірургії, якщо це можливо, особливо якщо пацієнт приймав БП більше 3 років (Ruggiero et al. 2009; Allen & Ruggiero 2014). Для пацієнтів з історією лікування пероральними біфосфонатами, що перевищує 3 роки, та тих, хто має супутнє лікування преднізоном, слід розглянути додаткові тести та альтернативні варіанти лікування (Grant et al. 2008).
Метою цього багатопрофільного проспективного спостережного дослідження було представити 3-річні дані про виживання та успішність імплантів і протезів, а також втрату кістки навколо імплантів після встановлення фіксованого імплантопідтримуваного стоматологічного протезу, який був наданий пацієнтам, що приймають пероральні біфосфонати (алендронат 70 мг таблетка один раз на тиждень або 5–10 мг один раз на день) протягом щонайменше 3 років перед встановленням імпланта. Це дослідження дотримувалося рекомендацій STROBE (Зміцнення звітності спостережних досліджень в епідеміології).
Матеріали та методи
Дизайн дослідження
Це багатопрофільне проспективне спостережне дослідження було розроблено для оцінки клінічних та радіологічних результатів фіксованого імплантопідтримуваного стоматологічного протезу, наданого пацієнтам, які приймають алендронат 70 мг таблетка один раз на тиждень або 5–10 мг один раз на день, протягом щонайменше 3 років перед встановленням імпланта. Сорок пацієнтів були відібрані та лікувалися в двох приватних центрах (20 у Римі, 20 у Сассарі, Італія) з січня 2008 року по грудень 2011 року. Два досвідчені клініцисти виконали всі імплантаційні та протезні процедури. Дослідження проводилося відповідно до принципів, закладених у Гельсінкській декларації 1964 року для біомедичних досліджень за участю людей, з поправками 2008 року. Пацієнти були проінформовані про клінічні процедури, матеріали, які будуть використовуватися, переваги, потенційні ризики та ускладнення, а також про необхідні оцінки для клінічного випробування, і дали свою письмову згоду на участь у цьому дослідженні.
Будь-який здоровий пацієнт <90 років, старший за 18 років на момент встановлення імплантату, який потребує протеза на імплантатах, був запрошений взяти участь у дослідженні в послідовному порядку. Пацієнти були включені в дослідження після виконання критеріїв включення та відсутності будь-яких критеріїв виключення.
Критерії виключення були наступними:
- Загальні медичні (клас III або IV Американського товариства анестезіологів, ASA) та/або психіатричні протипоказання;
- Вагітність або годування;
- Зловживання алкоголем або наркотиками;
- Сильне куріння (>10 сигарет/день);
- Радіаційна терапія в області голови або шиї протягом останніх 5 років;
- Висока та помірна парафункціональна активність;
- Відсутність зубів/зубного протеза в протилежній щелепі;
- Лікування пародонтиту не проводилось;
- Постекстракційні імплантати;
- Кровотеча з усієї ротової порожнини та індекс зубного нальоту в усій ротовій порожнині вище або дорівнює 25%;
- <10 мм висота та 5 мм ширина кістки для встановлення імплантатів;
- Непридатність для регулярних контрольних оглядів.
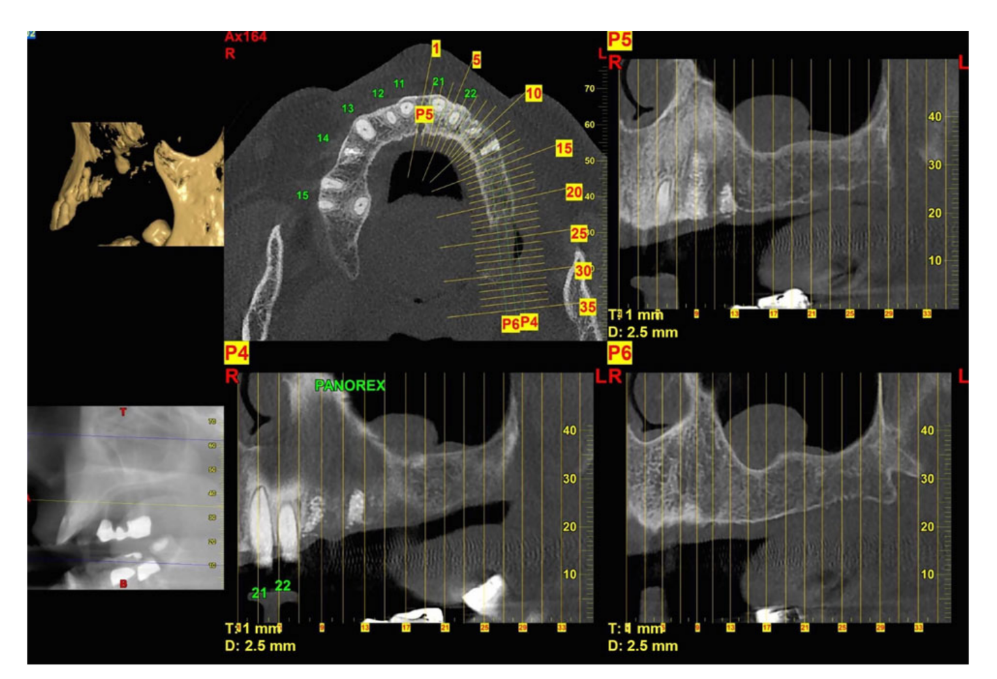
Усі пацієнти були проліковані відповідно до двоетапного діагностичного та терапевтичного протоколу (Рис. 1). Діагностичні етапи такі:
- Анамнез;
- Клінічне обстеження та фотографії;
- Рентгенологічне обстеження, включаючи періапікальні та панорамні рентгенівські знімки, комп'ютерну томографію (КТ) або конусно-променеву комп'ютерну томографію (КБКТ);
- Пародонтальне обстеження (зондування та вимірювання індексів орального здоров'я);
- Фотографічна документація;
- Інформація для пацієнта (ліки, які потрібно приймати, та можливі наслідки).
Клінічні процедури
Терапевтичний протокол (Таблиця 1):
- Професійна гігієна;
- Елімінація всіх вогнищ інфекції (залишкові корені, карієс, пародонтальна терапія):
- неконсервативне-хірургічне лікування всіх уражених зубів або з поганим прогнозом;
- відновлювальне лікування зубів, уражених карієсом;
- пародонтальне лікування та підтримуюча терапія;
- оцінка адекватності знімних та фіксованих протезів. Зокрема, оцінювалася герметичність протезних конструкцій та стабільність знімного протезу, які повинні бути атравматичними.
В кінці етапу профілактики пацієнтів мотивували дотримуватися ретельного домашнього протоколу гігієни порожнини рота та слідувати професійним нагадуванням.
Всі втручання виконували два досвідчені хірурги (MT & SMM). Коли це було заплановано, безболісне видалення зубів проводили не менше ніж за 8 тижнів до встановлення імплантату. Коронки багатокореневих зубів розділяли. Корені потім видалялися індивідуально, і за необхідності, за допомогою періотомів. Залишкові лунки видалення ретельно очищали від грануляційної тканини та залишкових волокон періодонтальної зв'язки за допомогою кюреток.
Передопераційний протокол вимагав призупинення БП за 6 місяців до операції та до повного загоєння 4–6 місяців після встановлення імплантату. Антибіотики призначалися профілактично за 7 днів до операції та продовжувалися протягом 7 днів (Sarzi Amadè et al. 2008):
- Амоксицилін та клавуланова кислота, одна таблетка кожні 12 годин (2 г на день);
- Метронідазол 250 мг; дві таблетки кожні 8 годин (1,5 г на день).
Перед початком хірургії пацієнти полоскали рот розчином хлоргексидину 0,2% протягом 1 хвилини. Місцева анестезія була проведена за допомогою розчину артикаїну 4% з епінефрином 1 : 100.000 (Ubistein; 3M Italy SpA, Мілан, Італія). Імплантати були встановлені в запланованих анатомічних місцях за допомогою безфлапового або мінімального флапового підходу (Рис. 2). Щільність кістки оцінювалася під час свердління на основі досвіду та відчуттів лікаря, і вона ґрунтувалася на класифікації Лекгольма та Зарба (Brånemark et al. 1985). Кожен свердло використовувався під рясним зрошенням відповідно до протоколу, рекомендованого виробником. Платформа імплантату була розташована на рівні альвеолярного гребеня або трохи нижче в естетичній зоні.
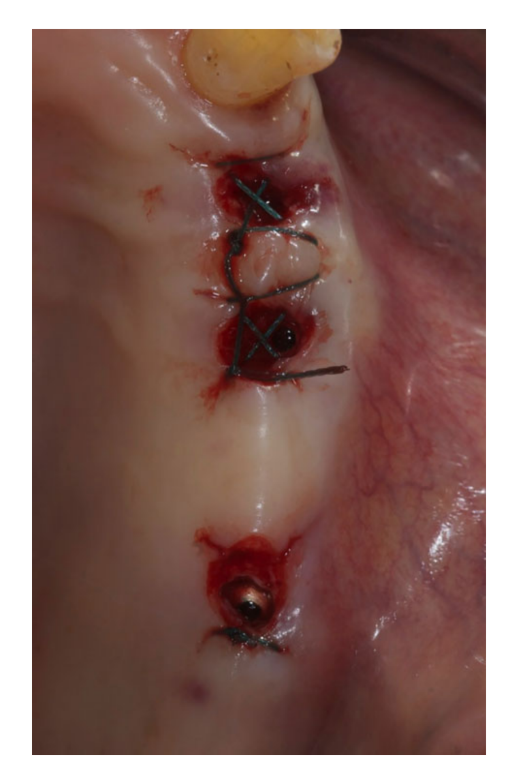
Після встановлення імплантів усі пацієнти отримали усні та письмові рекомендації щодо медикаментів, підтримки гігієни ротової порожнини та дієти. Післяопераційне знеболення проводилося з використанням ібупрофену 100 мг, який приймали кожні 8 годин протягом 2 днів після операції, а потім за потреби. Пацієнтам було рекомендовано полоскати рот розчином хлоргексидину 0,2% двічі на день без чищення області імпланта до зняття швів (через 10–14 днів).
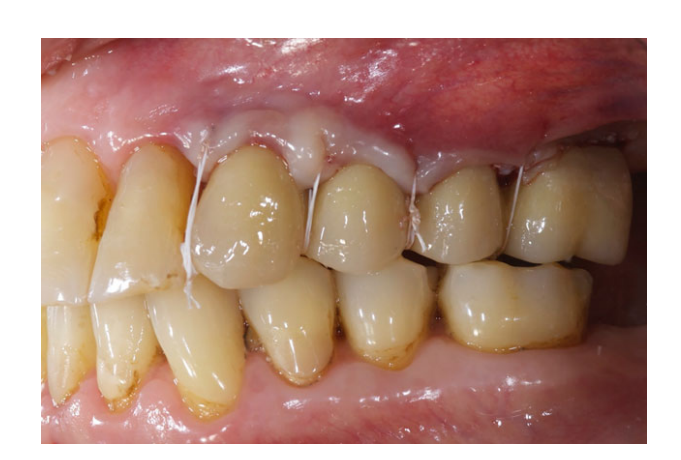
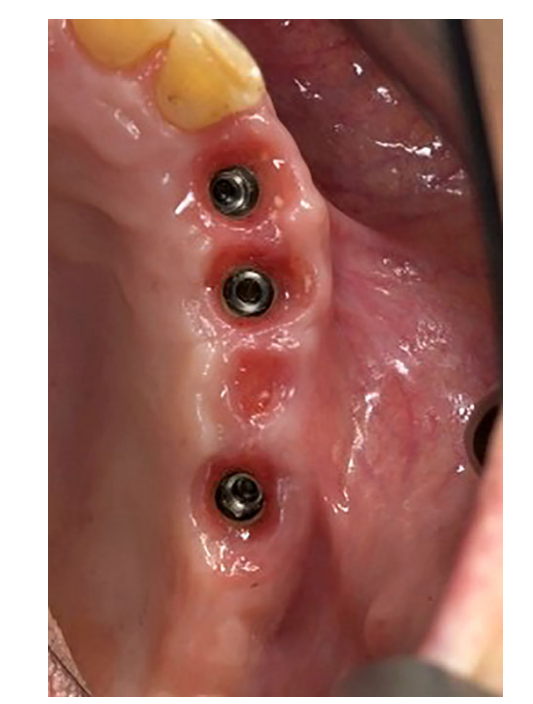
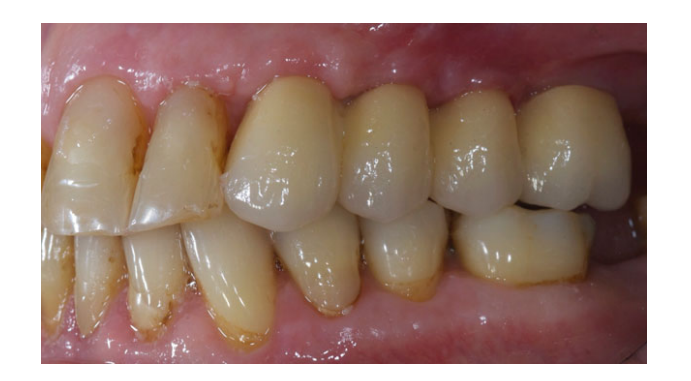
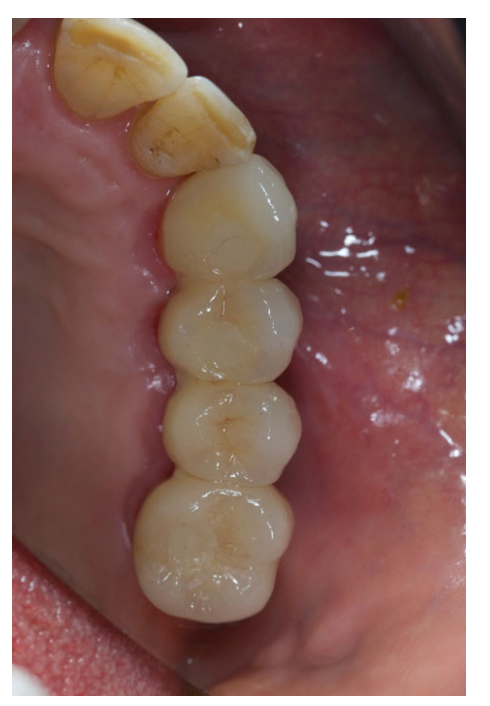
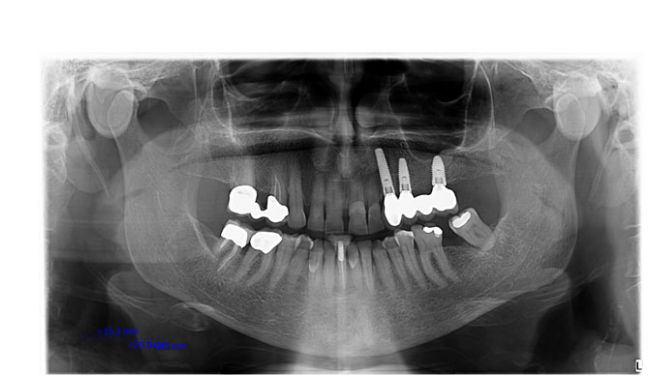
Усі імпланти були встановлені під поверхнею. Імпланти були відкриті через 3 місяці після їх встановлення (Рисунки 3 і 4). Відкриті зліпки були зроблені за допомогою поліефірного матеріалу (ImpregumTM, 3M ESPE, Seefeld, Німеччина) з використанням індивідуальної відкритої ложки (Diatray Top, Dental Kontor, Stockelsdorf, Німеччина). Під час доставки протеза (Рисунки 5 і 6) була проведена корекція оклюзії, а реставрації були або закріплені гвинтами, або цементовані безевгенольним цементом на основі оксиду цинку (Temp Bond NE, Kerr Corporation, Orange, CA, США) через 12 тижнів після першої операції відповідно до звичайного протоколу навантаження (Gallucci et al. 2013). Візити для контролю були заплановані через 1–6 місяців, а потім щорічно до 3 років функціонування (Рисунок 7). На кожному візиті для контролю проводилася корекція оклюзії зубного протеза за потреби. Пацієнти проходили професійну чистку у стоматологічного гігієніста кожні 4–6 місяців. Періапікальні рентгенограми отримувалися щорічно після доставки остаточного протеза з використанням того ж індивідуального тримача Rinn (Rinn, Elgin, IL, США).
Результати вимірювань
Основними показниками результатів були успішність та виживаність імплантів. Під час кожного контрольного обстеження імпланти перевірялися на інтеграцію тканин відповідно до суворих параметрів, визначених Buser та ін. (1990). Зокрема, інтеграція вважалася успішною, якщо були виконані такі параметри: (1) відсутність повторюваної періімплантної інфекції з гноєм; (2) відсутність постійних суб'єктивних скарг, таких як біль, відчуття стороннього тіла та/або дисестезія; (3) відсутність постійної радіолусценції навколо імпланта та (4) відсутність будь-якої виявленої рухливості імпланта. Ці критерії виявилися ефективними для визначення успішності імплантаційної системи та оцінки довгострокових результатів у клінічних випробуваннях. Успішність протезування оцінювалася за модифікацією критеріїв оцінки, запропонованих Каліфорнійською стоматологічною асоціацією (CDA (Асоціація CD 1976)).
Вторинними результатами були наступні: будь-які хірургічні та протезні ускладнення, що виникли протягом всього періоду спостереження, втрата краєвого кістки, глибина зондування (PPD) та кровотеча при зондуванні (BOP).
- Ускладнення: Будь-які технічні (перелом каркасу та/або облицювального матеріалу, розхитування гвинтів тощо) та/або біологічні (біль, набряк, гній тощо) ускладнення вважалися.
- Втрата краєвого кістки: Відстань від найбільш коронального краю коміра імплантату до найбільш корональної точки контакту кістки з імплантатом бралася за рівень краєвого кістки (MBL). MBL навколо імплантатів оцінювали на інтраоральних цифрових рентгенограмах, зроблених за допомогою паралельної техніки з використанням тримача для плівки (Rinn XCP, Dentsply, Elgin, IL, USA) під час встановлення імплантату (базовий рівень) та через 12, 24 і 36 місяців. Рентгенограми приймалися або відхилялися для оцінки на основі чіткості різьби імплантату. Усі читабельні рентгенограми відображалися в програмі аналізу зображень (DFW2.8 для windows, Soredex, Tuusula, Finland) на 24-дюймовому LCD екрані (iMac, Apple, Cupertino, CA, USA) і оцінювалися за стандартизованими умовами (SO 12646:2004). Програмне забезпечення було відкаліброване для кожного окремого зображення, використовуючи відому відстань діаметра або довжини імплантату. Вимірювання рівня кісткового гребеня з мезіальної та дистальної сторін, що прилягає до кожного імплантату, проводилися з точністю до 0.1 мм і середньоарифметично обчислювалися на рівні пацієнта.
- PPD та BoP вимірювалися сліпим оператором за допомогою пародонтального зонда (PCP-UNC 15; Hu-Friedy Manufacturing, Chicago, IL, USA) через 6, 12, 24 та 36 місяців. Для кожного імплантату збиралися три вестибулярні та три лінгвальні значення, які середньоарифметично обчислювалися на рівні пацієнта.
Два незалежних і повністю сліпих стоматолога (LC та EX) для кожного центру оцінили виживаність та успішність імплантів і протезів. Ускладнення оцінювалися та лікувалися лікарями (MT та SMM), які не були сліпими. Втрата краєвого кісткового обсягу (DMBL) оцінювалася незалежним радіологом. Всі пародонтальні вимірювання проводив незалежний гігієніст.
Статистичний аналіз
Статистичний аналіз проводився для числових параметрів, таких як рівень краєвої кістки та параметри м'яких тканин, за допомогою SPSS для Mac OS X версії 22.0 (SPSS, Чикаго, IL, США). Описовий аналіз проводився з використанням середнього стандартного відхилення (SD) та медіани з 95% довірчим інтервалом (CI). Кумулятивні показники виживаності та успішності розраховувалися з використанням імплантів та протезів як статистичної одиниці аналізу. Різниці середніх рівнів краєвої кістки між контрольними точками, в середньому на рівні пацієнтів, порівнювалися за допомогою тесту Вілкоксона для парних вибірок. Рівень статистичної значущості був встановлений на 0.05. Порівняння між центрами проводилися за допомогою одностороннього аналізу дисперсії (ANOVA).
Результати
Наприкінці дослідження вісім пацієнтів (20%) з 18 імплантатами (15.5%) вибули. Один пацієнт у римському центрі помер від раку печінки. У п'яти пацієнтів (двоє в римському центрі та троє в центрі Сассарі) були серйозні проблеми зі здоров'ям, не пов'язані з терапією зубними імплантатами, тому вони не змогли прийти на заплановані контрольні огляди. Двоє пацієнтів виїхали за кордон. Однак, за результатами телефонного інтерв'ю, всі ці пацієнти мали свої імплантати в функції без ускладнень, пов'язаних з пацієнтами (біль, набряк). Остаточний розмір вибірки становив 98 імплантатів з грубою окисленою поверхнею та імплантатами з конічним корпусом (NobelReplace, Nobel Biocare AB), які були встановлені у 32 послідовних беззубих пацієнтів (32 жінки) зі середнім віком 64.6 років (діапазон 46–80). Кожен центр лікував однакову кількість 16 пацієнтів. Кожен пацієнт спостерігався протягом ≥3 років функції (діапазон 36–72 місяців; середнє 47.6 місяців). Не було помітних початкових дисбалансів між двома групами, окрім більшої кількості довших імплантатів, використаних римським центром, та наявності більшої кількості випадків, лікуваних за допомогою комп'ютерної асистованої шаблонної хірургії в центрі Сардинії. Відхилень від початкового протоколу не було. Усі зібрані дані були включені в статистичний аналіз.
- Один з 98 імплантатів (1.02%) зазнав невдачі під час періоду загоєння, перед доставкою остаточних протезів, що призвело до загального кумулятивного показника виживання імплантатів 98.98% на 3-річному спостереженні. Єдиний випадок невдачі імплантату стався у одного пацієнта з центру Сардинії (імплантат вузької платформи довжиною 10 мм). Імплантат не був замінений.
- На 3-річному спостереженні жоден з остаточних протезів не зазнав невдачі, що призвело до кумулятивного показника виживання протезів 100%.
- Не було зафіксовано жодних протезних ускладнень. Не було зареєстровано серйозних біологічних ускладнень. У трьох пацієнтів спостерігалося запалення слизової оболонки навколо імплантату з BoP через 6 місяців. Поліпшення гігієни ротової порожнини зменшило запалення навколо імплантату без будь-яких хірургічних втручань.
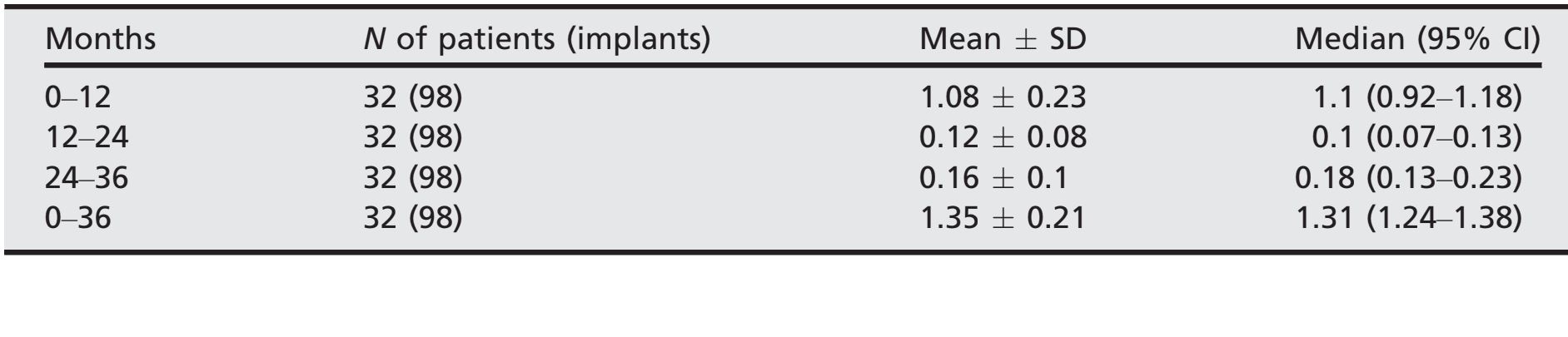
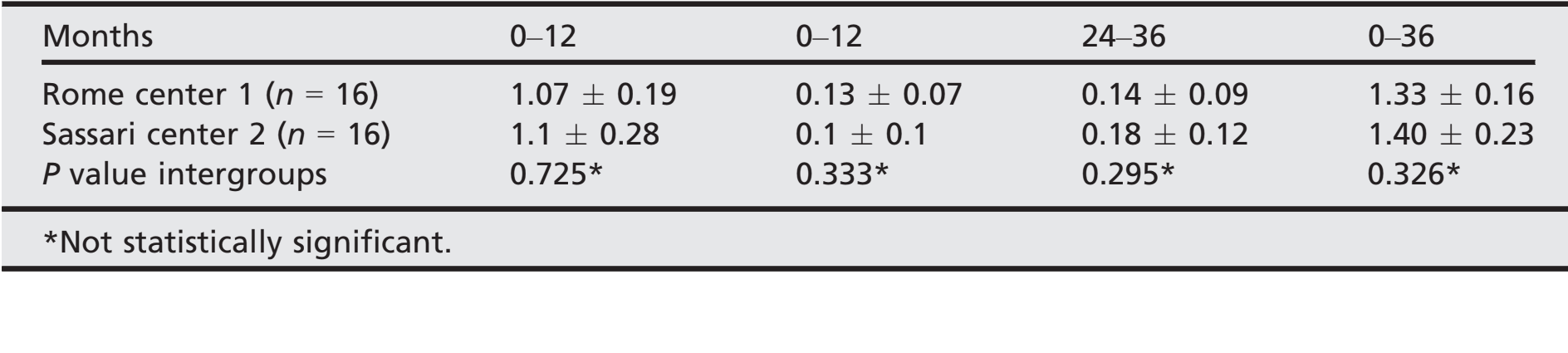
- Після початкової середньої втрати краєвого кісткового об'єму 1.08 ± 0.23 (медіана 1.1; CI 95% 0.92–1.18), всі імплантати втратили в середньому 0.12 ± 0.08 (медіана 0.1; CI 95% 0.07–0.13) між 1-им і 2-им роками спостереження, і 0.16 ± 0.1 (медіана 0.18; CI 95% 0.13–0.23) між 2-им і 3-ім роками спостереження, без статистично значущої різниці (P = 0.059). На 3-річному спостереженні середня втрата краєвого кісткового об'єму становила 1.35 0.21 (медіана 1.31; CI 95% 1.24–1.38). Усі дані наведені в Таблиці 2. На кожному спостереженні зміни рівня кістки були подібними для обох центрів (P ≥ 0.05). Усі дані наведені в Таблиці 3.
- На 3-річному спостереженні середні значення PPD становили 2.71 0.38 мм (95% CI = 2.54–2.86). Середні значення BoP становили 1.29 ± 0.76 (95% CI = 0.93–1.63).
Обговорення
Дане проспективне обсерваційне дослідження було розроблено для оцінки 3-річних клінічних та рентгенографічних результатів фіксованого імплантованого стоматологічного протеза, який був встановлений пацієнтам, що приймали алендронат у дозі 70 мг один раз на тиждень або 5–10 мг один раз на день протягом щонайменше 3 років до встановлення імплантату.
На 3-річному контрольному обстеженні результати даного дослідження показали, що виживаність імплантів та протезів становила 99% та 100% відповідно. Зміни в краєвій кістці, а також значення BOP та PPD, здається, залишаються стабільними після 3 років, підтверджуючи, що імплантаційна терапія у пацієнтів, які приймають пероральні БП, є життєздатним методом лікування відповідно до запропонованого терапевтичного протоколу. Ці результати узгоджуються з іншими дослідженнями, що вивчають ту ж тему. У ретроспективному дослідженні Мемон та ін. (2012) дійшли висновку, що біфосфонати не вплинули на ранній успіх імплантації або зміни в краєвій кістці. Джеффкот (2006) та Руссо Делло та ін. (2007) у двох проспективних дослідженнях повідомили, що пероральні БП, здається, не збільшують частоту виникнення ОНЖ. Грант та ін. (2008) у ретроспективному дослідженні на 115 пацієнтах (468 імплантів) повідомили, що терапія пероральними біфосфонатами, здається, не має значного впливу на успіх імплантації.
Основними обмеженнями цього дослідження є обмежена кількість учасників, які спостерігалися протягом короткого періоду. Тим не менш, незважаючи на те, що вісім пацієнтів вибули, 98 імплантатів було встановлено у 32 пацієнтів, які лікувалися за одним і тим же протоколом, і спостерігалися протягом щонайменше 3 років, що дозволяє узагальнити результати цього дослідження на більшу популяцію з подібними характеристиками.
Дослідження на тваринах показало, що застосування БП впливає на нормальне ремоделювання кістки після видалення зуба, ставлячи під загрозу тривале загоєння навколо імплантатів (Kim et al. 2013). Одним з найсерйозніших, хоча й рідкісних ускладнень є остеонекроз щелеп, пов'язаний з біфосфонатами (BRONJ) (Kwon et al. 2014). Частота BRONJ може варіюватися в залежності від способу введення та сили використовуваних препаратів. Американська асоціація оральних і щелепно-лицевих хірургів повідомила, що поширеність BRONJ становила близько 0,8% до 12%, коли БП вводяться внутрішньовенно (Ruggiero et al. 2009; Allen & Ruggiero 2014). Повідомляється, що поширеність нижча, коли БП вводяться перорально. Однак було запропоновано приділяти особливу увагу, коли пацієнти проходять лікування БП більше 3 років, оскільки поширеність BRONJ зростає протягом періоду лікування БП (Sarzi Amade` et al. 2008). Після поганих ентузіастичних попередніх результатів, основаних на неконтрольованих ретроспективних дослідженнях, деякі систематичні огляди запропонували більш ентузіастичні результати. Madrid & Sanz (2009) дійшли висновку, що пацієнт, який отримує пероральні біфосфонати протягом періоду <5 років, є “безпечним” для проведення стоматологічних процедур, зокрема стоматологічних імплантатів (Madrid & Sanz 2009). Крім того, існує загальний консенсус щодо відсутності протипоказань для встановлення імплантатів у неонкологічних пацієнтів, які отримують пероральні БП, переважно призначені для остеопорозу (Madrid & Sanz 2009). Нещодавно Кумар & Хонне (2012), оцінюючи виживаність стоматологічних імплантатів у користувачів біфосфонатів та не-користувачів, дійшли висновку, що короткострокова терапія БП не збільшує і не зменшує рівень виживаності стоматологічних імплантатів у порівнянні з не-користувачами.
Хоча занурена техніка не є обов'язковою для остеоінтеграції (Tallarico et al. 2011), у даному дослідженні всі імплантати були встановлені занурено, без будь-яких хірургічних ускладнень. Це може бути одним з ключових факторів разом із значною антибіотикотерапією та тимчасовою зупинкою прийому алендронату, що запобігає бактеріальному забрудненню місця імплантації.
У даному дослідженні, незважаючи на обмежену кількість пацієнтів, хірургія імплантації не призвела до остеонекрозу щелепи, пов'язаного з біфосфонатами, через 3 роки після встановлення імплантів. Проте існує достатньо доказів, щоб стверджувати, що всіх пацієнтів, які проходять імплантацію, слід запитувати про терапію біфосфонатами, включаючи прийняті препарати, дозування та тривалість лікування перед операцією. Потенційні ризики BRONJ потрібно пояснити пацієнтам перед установкою імплантів. Для пацієнтів з історією лікування пероральними біфосфонатами, що перевищує 3 роки, та тих, хто отримує супутнє лікування преднізоном, слід розглянути додаткові тести та альтернативні варіанти лікування, а профілактика залишається найефективнішим засобом для уникнення можливих ускладнень. Крім того, анатомічне розташування імпланта та тривалість терапії препаратом на момент встановлення не були значними факторами у рівні успіху або змінах кістки.
Висновок
В межах обмежень цього дослідження, відповідно до запропонованого терапевтичного протоколу та виконання мінімально інвазивної зануреної хірургії, терапія оральними біфосфонатами не здавалася значно впливаючою на виживання та успіх імплантів у середньостроковому спостереженні. Ці висновки повинні бути підтверджені подальшими проспективними дослідженнями з залученням більших вибірок та тривалішими термінами спостереження.
Марко Талларіко, Луїджі Канулло
Посилання
- Абтагі, Дж., Агхолме, Ф., Сандберг, О. & Аспенберг, П. (2013) Вплив місцевої та системної доставки біфосфонатів на фіксацію зубних імплантів у моделі остеонекрозу щелепи. Журнал стоматологічних досліджень 92: 279–283.
- Аллен, М.Р. & Руджеро, С.Л. (2014) Огляд фармацевтичних засобів та орального здоров'я кісток: як остеонекроз щелепи вплинув на цю галузь. Міжнародний журнал оральних та щелепно-лицевих імплантів 29: e45–e57.
- Ата-Алі, Дж., Ата-Алі, Ф., Пенарроча-Ольтра, Д. & Галіндо-Морено, П. (2014) Який вплив має терапія біфосфонатами на виживання зубних імплантів? Систематичний огляд та мета-аналіз. Клінічні дослідження оральних імплантів doi: 10.1111/clr.12526. [Epub ahead of print].
- Бернабеї, Р., Мартоне, А.М., Ортолані, Е., Ланді, Ф. & Марзетті, Е. (2014) Скринінг, діагностика та лікування остеопорозу: короткий огляд. Клінічні випадки в мінеральному та кістковому метаболізмі 11: 201–207.
- Бранемарк, П.І., Зарб, Г.А. & Альбректссон, Т. (1985) Тканинно-інтегровані протези: остеоінтеграція в клінічній стоматології. Чикаго: Quintessence ed.
- Бусер, Д., Вебер, Х.П. & Ланг, Н.П. (1990) Тканинна інтеграція несубмерджених імплантів. Результати 1 року проспективного дослідження з 100 порожнистими циліндровими та порожнистими гвинтовими імплантами ITI. Клінічні дослідження оральних імплантів 1: 33–40.
- Каліфорнійська стоматологічна асоціація, Робоча група з оцінки якості. (1976) Оцінка якості стоматологічної допомоги: рекомендації щодо оцінки клінічної якості та професійної діяльності та стандарти для програми, що забезпечує якість допомоги. Лос-Анджелес: Каліфорнійська стоматологічна асоціація ed. Чикаго.
- Флейш, Х., Рассел, Р. & Штрауманн, Ф. (1966) Вплив пірофосфату на гідроксиапатит і його наслідки для гомеостазу кальцію. Природа 212: 901–903.
- Грант, Б.Т., Аменедо, К., Фріман, К. & Краут, Р.А. (2008) Результати встановлення зубних імплантів у пацієнтів, які приймають оральні біфосфонати: огляд 115 випадків. Журнал оральної та щелепно-лицевої хірургії 66: 223–230.
- Хасегава, Й., Кавабе, М., Кімура, Х., Куріта, К., Фукута, Дж. & Ураде, М. (2012) Вплив протезів на початкове місце виникнення на прогноз остеонекрозу щелеп, пов'язаного з біфосфонатами: ретроспективне дослідження. Оральна хірургія, оральна медицина, оральна патологія та оральна радіологія 114: 318–824.
- Джефкоут, М.К. (2006) Безпека оральних біфосфонатів: контрольовані дослідження на альвеолярній кістці. Міжнародний журнал оральних та щелепно-лицевих імплантів 21: 349–353.
- Джонс, Д.Х., Накашіма, Т., Санчес, О.Х., Козерадзький, І., Комарова, С.В., Саросі, І., Морони, С., Рубін, Е., Сарао, Р., Ходжила, С.В., Комненович, В., Конг, Й.Й., Шрайбер, М., Діксон, С.Й., Сімс, С.М., Хоха, Р., Вада, Т. & Пеннінгер, Дж.М. (2006) Регуляція міграції ракових клітин та кісткових метастазів RANKL. Природа 440: 692–696.
- Каніс, Дж.А., МакКлоскі, Е.В., Йоганссон, Х., Оден, А., Мелтон, Л.Й. & Халтаєв, Н. (2008) Референтний стандарт для опису остеопорозу. Кістка 42: 467–475.
- Хосла, С. (2009) Зростаючі можливості для лікування остеопорозу. Нью-Інглендський журнал медицини 361: 818–820.
- Кім, І., Кі, Х., Лі, В., Кім, Х. & Парк, Дж.Б. (2013) Вплив системно введених біфосфонатів на кісткове загоєння після видалення зуба та остеоінтеграцію зубних імплантів у верхній щелепі кролика. Міжнародний журнал оральних та щелепно-лицевих імплантів 28: 1194–1200.
- Кос, М., Бруско, Д., Кюблер, Дж. & Енгельке, В. (2010b) Клінічне порівняння пацієнтів з остеонекрозом щелеп, з історією та без історії введення біфосфонатів. Міжнародний журнал оральної та щелепно-лицевої хірургії 39: 1097–1102.
- Кос, М., Кюблер, Дж.Ф., Луцзак, К. & Енгельке, В. (2010a) Остеонекроз щелеп, пов'язаний з біфосфонатами: огляд 34 випадків та оцінка ризику. Журнал краніо-щелепно-лицевої хірургії 38: 255–259.
- Кумар, М.Н. & Хонне, Т. (2012) Виживання зубних імплантів у користувачів біфосфонатів порівняно з некористувачами: систематичний огляд. Європейський журнал протезування та відновної стоматології 20: 159–162.
- Квон, Т.Г., Лі, Ч.О., Парк, Дж.В., Чой, С.Й., Ріджал, Г. & Шин, Х.І. (2014) Остеонекроз, пов'язаний з зубними імплантами у пацієнтів, які проходять лікування біфосфонатами. Клінічні дослідження оральних імплантів 25: 632–640.
- Мадрид, С. & Санз, М. (2009) Який вплив мають системно введені біфосфонати на оральну імплантацію? Систематичний огляд. Клінічні дослідження оральних імплантів 20: 87–95.
- Мемон, С., Вельтман, Р.Л. & Катанчік, Дж.А. (2012) Оральні біфосфонати: ранній успіх ендооссальних зубних імплантів та зміни кістки на вершинах. Ретроспективне дослідження. Міжнародний журнал оральних та щелепно-лицевих імплантів 27: 1216–1222.
- Резка, А.А. & Родан, Г.А. (2004) Механізм дії біфосфонатів, що містять азот. Міні-огляди в медичній хімії 4: 711–719.
- Руджеро, С.Л., Додсон, Т.Б., Ассаель, Л.А., Ландесберг, Р., Маркс, Р.Е. & Мехротра, Б. (2009) Позиційний документ Американської асоціації оральних та щелепно-лицевих хірургів щодо остеонекрозу щелеп, пов'язаного з біфосфонатами – оновлення 2009 року. Австралійський ендодонтичний журнал 35: 119–130.
- Рупель, К., Оттавіані, Дж., Гоббо, М., Контардо, Л., Тіреллі, Дж., Вескові, П., Ді Ленарда, Р. & Біазотто, М. (2014) Систематичний огляд терапевтичних підходів до остеонекрозу щелеп, пов'язаного з біфосфонатами (BRONJ). Оральна онкологія 50: 1049–1057. Руссо Делло, Н.М., Джефкоут, М.К., Маркс, Р.Е. & Фугаццотто, П. (2007) Остеонекроз у щелепах пацієнтів, які використовують оральні біфосфонати для лікування остеопорозу. Міжнародний журнал оральних та щелепно-лицевих імплантів 22: 146–153.
- Сарці Амаде, Д., Талларіко, М., Лореті, М.Ц., Монтеккі, П.П. & Нікколі, А. (2008) Клінічні рекомендації щодо профілактики остеонекрозу щелеп у пацієнтів, які проходять лікування біфосфонатами: огляд літератури та звіт про три випадки. Мінера Стоматологіка 57: 429–446.
- Талларіко, М., Ваккарелла, А. & Марці, Г.Ц. (2011) Клінічні та радіологічні результати 1- та 2-етапного встановлення імплантів: результати 1 року рандомізованого клінічного випробування. Європейський журнал оральної імплантології 4: 13–20.
- Цеценекоу, Е., Пападопулос, Т., Калівас, Д., Папаіоанну, Н., Тангл, С. & Ватзек, Г. (2012) Вплив алендронату на остеоінтеграцію нанолікованих зубних імплантів у кроликах Нової Зеландії. Клінічні дослідження оральних імплантів 23: 659–666.