Використання вакуумної плазмової обробки поверхні для покращення гідрофільності та змочуваності замінників кісткових трансплантатів і резорбованих мембран: дослідження in vitro
Машинний переклад
Оригінальна стаття написана мовою EN (посилання для прочитання) .
Анотація
Передумови/Цілі: Ми хотіли оцінити in vitro, чи може вакуумна плазмова обробка поверхні замінників кісткових трансплантатів та резорбованих мембран покращити гідрофільність та змочуваність протестованих матеріалів.
Методи: Усього було розглянуто 28 стерилізованих зразків для цього дослідження, які були поділені на три групи. Шість зразків були використані для аналізу SEM-EDS. Інші 22 зразки були випадковим чином розподілені на тестову (оброблену плазмою, n = 11) та контрольну (без обробки, n = 11) групи. Вакуумна плазмова обробка поверхні була проведена в тестовій групі перед аналізом SEM-EDS за допомогою ACTILINK reborn з тримачем для матеріалів (Plasmapp Co., Ltd., Деаджон, Республіка Корея). Чорнила Plasmatreat (Plasmatreat, Штайнхаген, Німеччина) використовувалися для оцінки різниць у гідрофільності між тестовою та контрольною групами. Результати вимірювалися за часом поглинання, ступенем змочуваності та ступенем дезінфекції після різних циклів часу.
Результати: Після обробки поверхні вакуумним плазмовим методом час поглинання чорнил статистично зменшився у всіх підгрупах (p < 0.05), тоді як ступінь змочуваності збільшився. Аналізи SEM-EDS показали підвищену швидкість зменшення вмісту вуглецевих домішок після до трьох циклів обробки поверхні вакуумним плазмовим методом. Крім того, аналіз SEM-EDS не виявив жодних ділянок пошкодження, викликаних багаторазовими обробками.
Висновки: В межах обмежень цього in vitro дослідження обробка поверхні вакуумним плазмовим методом збільшила гідрофільність і змочуваність протестованих біоматеріалів. Кістковий графт у вигляді частинок та кісткові блоки слід обробляти за допомогою програм з більш тривалим часом. Потрібні подальші добре проведені рандомізовані клінічні випробування з розрахунками розміру вибірки для підтвердження цих попередніх результатів.
Вступ
Оральна імплантологія визнана безпечною та передбачуваною клінічною методологією, здатною забезпечити довгострокові результати в галузі оральної реабілітації. Оссеоінтеграція зубних імплантатів бере свій початок на початку 1950-х років, коли професор Пер-Інгвар Бранемарк, шведський ортопед, спочатку проводив ортопедичні експерименти на ногах кроликів. В даний час імплантат вважається оссеоінтегрованим, коли немає прогресуючого
відносний рух між імплантатом і кісткою, з якою він повинен мати прямий контакт. У минулому одним з найважливіших аспектів досягнення остеоінтеграції була первинна стабільність під час встановлення імплантату. Від своїх витоків до сьогодні література була зосереджена на чисто біологічно орієнтованих принципах. Щодо останнього, було досліджено та впроваджено численні методи обробки поверхні для покращення біологічних характеристик поверхні імплантатів, включаючи модифікації шорсткості поверхні імплантатів та покращення гідрофільності в процесі остеоінтеграції. Згідно з останніми дослідженнями, обидва методи, здається, покращують механізм остеоінтеграції, забезпечуючи більш сильне та швидке формування кістки, що дозволяє швидшій остеоінтеграції та успішним довгостроковим результатам.
Кілька досліджень оцінили обробку поверхні стоматологічних імплантатів та абатментів. Активація поверхні титанових імплантатів за допомогою плазмового оброблення може представляти позитивну стратегію для видалення забруднень з стоматологічних абатментів та мінімізації резорбції кістки навколо імплантату, а також для збільшення відсотків нової кістки в близькому контакті з поверхнею імплантату. Цей феномен, як було показано, опосередковується в умовах in vitro збільшенням адсорбції білків та адгезії остеобластів на титановій поверхні. Однак, на момент написання, на думку авторів, жодне дослідження ще не оцінювало жодних методів, які здатні збільшити енергетичну поверхню кісткових замінників та мембран. У дослідженні на тваринах Хо Джік Ян та ін. оцінили вплив вакуумного плазмового оброблення поверхні на людську акцелярну дермальну матрицю, підкреслюючи потенційний вплив оброблення на покращення результатів реконструктивної хірургії. Вакуумне плазмове оброблення поверхні також продемонструвало покращення адгезії клітин, модифікуючи змочуваність поверхні титанової пластини, зі зменшенням кута контакту між біологічними рідинами та поверхнею імплантату, що сприяє дифузії остеобластичних клітин і не залишає залишків після оброблення. Було зафіксовано деякі зміни у фізико-хімічних характеристиках, такі як вільна енергія поверхні, вміст вуглеводнів та функціональні гідроксильні групи, які можуть потенційно впливати на запальну реакцію в периімплантних тканинах. У клінічному рандомізованому контрольованому випробуванні оброблення аргоновою плазмою продемонструвало зменшення ремоделювання кістки навколо імплантату, з статистично сильнішими результатами до 5 років спостереження.
Основною метою цього in vitro дослідження було оцінити, чи може вакуумна плазмова обробка поверхні замінників кісткових трансплантатів та резорбованих мембран, які зазвичай використовуються для збереження альвеол та процедур GBR, покращити поверхневу енергію (гідрофільність) та змочуваність протестованих матеріалів. Нульова гіпотеза полягала в тому, що вакуумна плазмова обробка поверхні не має жодного впливу на час абсорбції або змочуваність. Додатковою метою було оцінити, використовуючи SEM-EDS аналізи, ступінь деконтамінації після різних циклів часу. Це дослідження було представлене відповідно до рекомендацій CRIS (Контрольний список для звітування про in-vitro дослідження).
Матеріали та методи
2.1 Зразки
У цьому in vitro рандомізованому (тестовому та контрольному) дослідженні було розглянуто всього 28 стерилізованих зразків. Розрахунок розміру зразка не проводився, оскільки в науковій літературі не було інших досліджень, які порівнювали біоматеріали з вакуумною плазмовою обробкою поверхні та без неї. Максимальна кількість зразків була використана відповідно до доступності відділу. Зразки включали різні біоматеріали, які зазвичай використовуються під час збереження альвеол та/або процедур GBR, і наведені нижче:
- Чотирнадцять блоків RE-BONE розміром 10 × 10 × 10 (8) та 10 × 10 × 20 (6) мм (UBGEN SRL, Вігонца, Італія);
- Чотири мембрани перикардію HEART (Bioteck SPA, Аркуняно, Італія);
- Два пористих гранули, 0.5 г~1 cc, 0.25–1 мм, OSTEOXENON (Bioteck SPA, Італія);
- Чотири пористих гранули, 0.5 г, 0.25–1 мм (неколлагенові), BIO-GEN (Bioteck SPA, Італія);
- Чотири колагенові Xenomatrix XC (Bioteck SPA).
Всього 6 з 28 зразків (блоки RE-BONE [UBGEN SRL, Вігонца, Італія]) були використані для аналізу SEM-EDS. Інші 22 зразки були випадковим чином поділені на дві рівні групи по 11 зразків (тестові, оброблені плазмою, та контрольні, без обробки) і протестовані для оцінки часу абсорбції та ступеня зволоження. Усі вимірювання були проведені в кафедрі медицини, хірургії та фармацевтики Університету Сассарі, Італія. Аналіз SEM-EDS трьох оброблених плазмою блоків RE-BONE (UBGEN SRL) був проведений у Центрі досліджень та розробок Plasmapp (Plasmapp Co, Республіка Корея).
ACTILINK, відроджений з тримачем для матеріалів (Plasmapp Co., Ltd., Дежеон, Республіка Корея), використовувався для обробки зразків. Чернила Plasmatreat (Plasmatreat, Штайнхаген, Німеччина) з різними поверхневими натягами були використані. Поверхнева енергія різних стерильних біоматеріалів з (тест) та без (контроль) вакуумної плазмової обробки поверхні оцінювалася шляхом вимірювання кута контакту (для оцінки змочуваності) та часу поглинання (для оцінки гідрофільності) використаних чернил.
2.2 Вакуумна плазмова обробка поверхні
У тестовій групі вакуумна плазмова обробка поверхні проводилася за допомогою машини ACTILINK reborn (Рисунок 1) з індивідуальним тримачем (вихровий тримач), розробленим для зручного використання. Згідно з протоколом виробників, час циклу вакуумної плазмової обробки поверхні, названий режимом VORTEX PLASMA, становив 30 с. Усі біоматеріали в тестовій групі пройшли той самий час циклу вакуумної плазмової обробки поверхні. На відміну від цього, жоден з біоматеріалів у контрольній групі не отримав жодного типу обробки. У тестовій групі, після відкриття стерильного ящика, випробуваний біоматеріал брався стерильними пінцетом і вставлявся в стерильний вихровий тримач, а потім поміщався в машину ACTILINK для вакуумної плазмової обробки поверхні. Після закінчення обробки як оброблені, так і необроблені біоматеріали вставлялися за допомогою стерильного пінцета в стерилізований тримач, і на кожен зразок було нанесено п’ять крапель чернил Plasmatreat з двома різними поверхневими натягами (56 і 72 мН/м). Негайно після цього відповідний час поглинання та ступінь змочуваності були зафіксовані, сфотографовані та критично порівняні для оцінки гідрофільності та кута контакту між чернилами та поверхнею використаних біоматеріалів. Поверхневі натяги 56 і 72 мН/м були використані, оскільки значення 56 мН/м було найближчим до значення людської крові.

2.3 SEM Аналіз
Для оцінки впливу часу обробки вакуумною плазмою на деконтамінацію (зменшення вуглецевих домішок) поверхні блоку кістки було проаналізовано три блоки RE-BONE (UBGEN SRL) за допомогою системи SEM-EDS після до трьох циклів обробки вакуумною плазмою. Шість блоків RE-BONE розміром 10 × 10 × 20 мм (UBGEN SRL) були використані для дослідження SEM-EDS. Два блоки RE-BONE (UBGEN SRL) були оброблені за трьома різними циклами кожен ([A] 30 с, [B] 60 с та [C] 90 с) перед обробкою вакуумною плазмою. Для обробки використовувалася машина ACTILINK reborn у режимі VORTEX PLASMA. Після кожного циклу обробки блоки кістки аналізувалися під скануючим електронним мікроскопом (SEM, Thermo Fisher Scientific, Phenom XL, Waltham, MA, USA), підключеним до енергетично-дисперсійного рентгенівського спектроскопа (EDS), щоб забезпечити цілеспрямований аналіз поверхонь зразків.
2.4 Результати вимірювань
Час поглинання та ступінь зволоження оцінювалися за відео, записаними під час процедур (Blackmagic Design Pocket Cinema Camera 4K, Blackmagic, Fremont, CA, USA). Тестова та контрольна групи були протестовані одночасно. Усі тести виконували два дослідники (М.Т. та М.Т.).
- Час поглинання визначався як інтервал, у секундах, від моменту, коли остання крапля торкнулася поверхні біоматеріалу, до моменту, коли всі краплі чорнила були поглинуті біоматеріалом. Записане відео оцінювалося за допомогою програми для редагування відео (iMovie для MacOS), а час поглинання вимірювався за допомогою розширеного таймлайну. Усі вимірювання повторювалися тричі двома різними операторами (М.Т. та М.Т.). Було розраховано середнє значення та стандартне відхилення (SD).
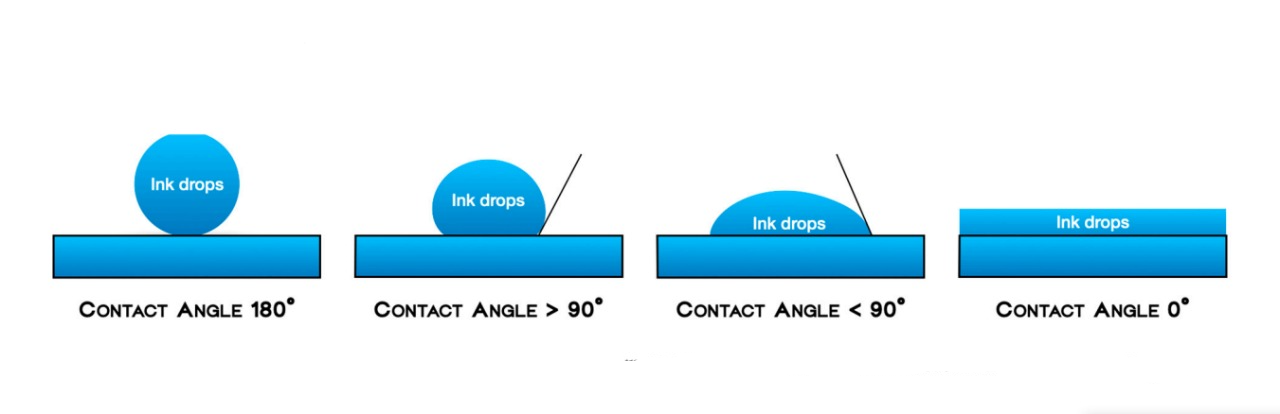
- Зволоження (зазвичай називається гідрофільністю) визначалося як розподіл крапель чорнила по поверхнях біоматеріалів, вимірюваний плоскістю краплі на твердій поверхні. Чотири ступені зволоження були визначені наступним чином:
Нульовий клас: Краплі чорнила залишалися на тій же позиції, на якій їх кинули, з кутом контакту 180°; Низький клас: Коли пляма чорнила трохи розширилася на поверхні, з кутом контакту > 90°; Середній клас: Коли помітне помірне розширення плями чорнила на поверхні, і кут контакту був <90°; Високий клас: Коли пляма чорнила була явно поглинена, з кутом контакту 0° (Рисунок 2).
- SEM аналіз. Для візуалізації зображень високої роздільної здатності поверхонь зразків використовували скануючу електронну мікроскопію. За допомогою SEM було проаналізовано топографію поверхні на зображеннях. Зокрема, зображення SEM використовувалися для оцінки швидкості зменшення вуглецевих домішок при трьох різних часах циклу. Для вимірювання енергії випромінюваних фотонів в електромагнітному спектрі рентгенівських променів та отримання хімічної інформації (атомний відсоток) використовувався детектор енергодисперсійної рентгенівської спектроскопії (EDS).
2.5 Статистичний аналіз
Весь аналіз даних був проведений відповідно до заздалегідь встановленого плану аналізу. Біостатистик з експертизою в стоматології проаналізував дані за допомогою програмного забезпечення Ky Plot 2.0, Informer Technologies, Inc. NY, США, не знаючи кодів груп. Середні значення та стандартні відхилення були розраховані для кожного вимірювання. Для порівняння часу абсорбції між групами використовувався калькулятор двовибіркового тесту Колмогорова–Смірнова. Статистичні порівняння проводилися на рівні значущості 0.05.
Результати
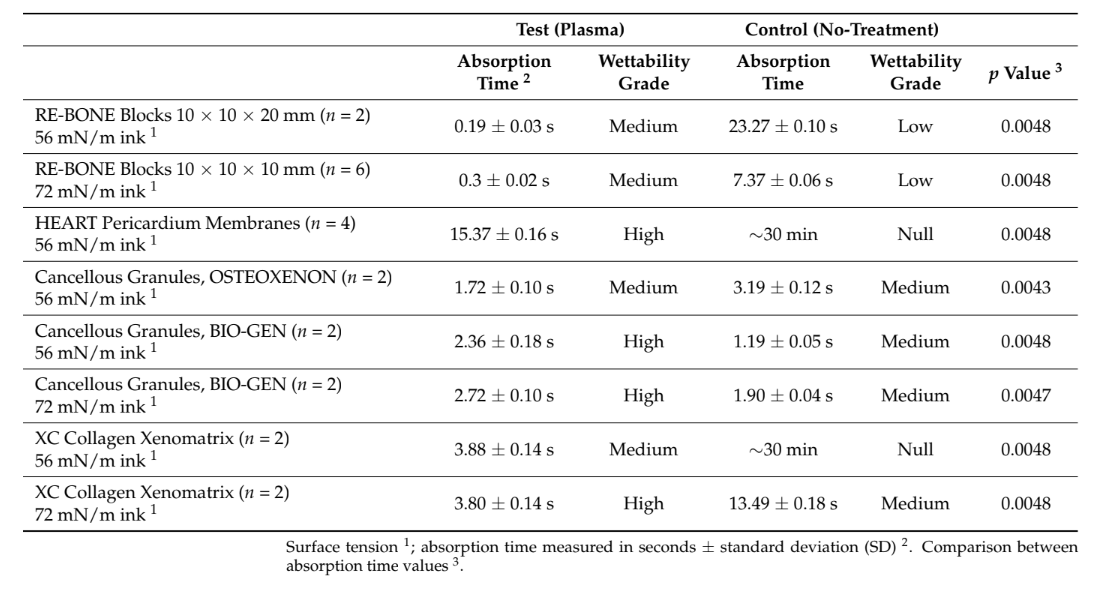
Всього було використано 28 зразків. Час поглинання та змочуваність 22 зразків після нанесення різних чорнил з різними поверхневими натягами були оцінені в обох групах. Вакуумна плазмова обробка поверхні статистично зменшила час поглинання у всіх оброблених зразках (p значення < 0.05, Таблиця 1). Більше того, для всіх зразків, за винятком остеоксенонових пористих гранул з чорнилом 56 мН/м, змочуваність у тестовій групі була вищою порівняно з контролем. Найбільша різниця в змочуваності була виявлена для перикардіальної мембрани, з високим рівнем у тестовій групі в порівнянні з нульовим рівнем у контрольній групі. Найкращі результати були отримані для вакуумної плазмової обробки поверхні кісткових блоків, колагенових мембран, перикардіальних мембран та колагенових кісткових трансплантатів відповідно. Всі дані наведені в Таблиці 1. Пояснювальні зображення наведені в Рисунку 3.
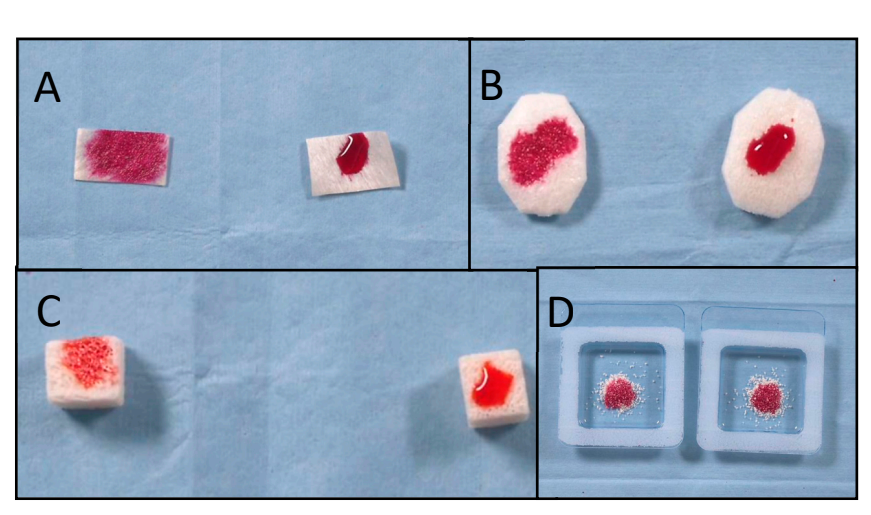
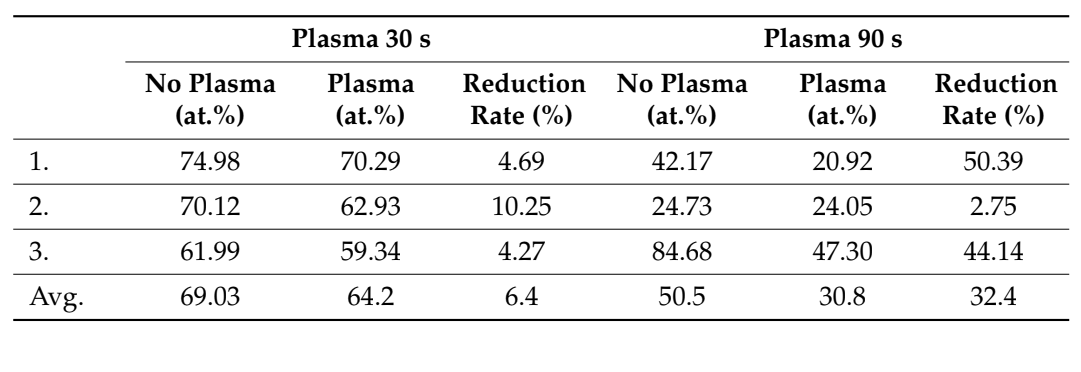
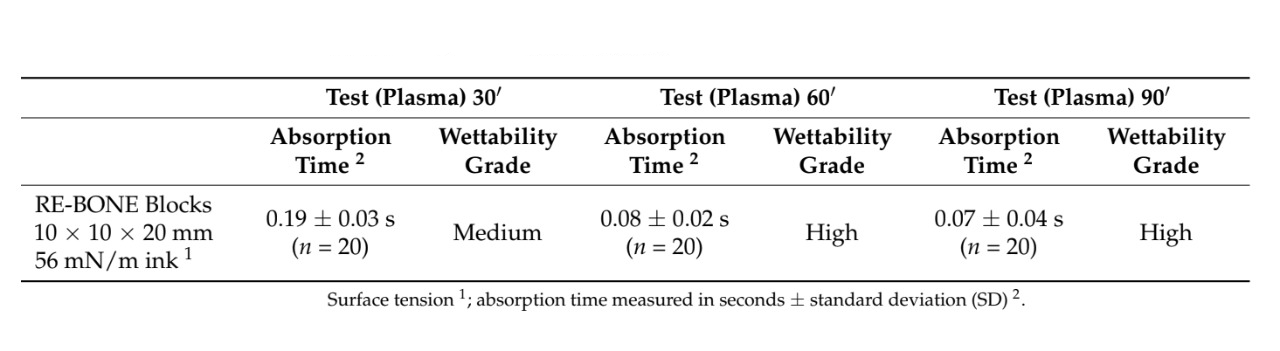
Шість блоків кістки (три після вакуумної плазмової обробки поверхні та три без будь-якої обробки) були оцінені в аналізі SEM-EDS після одного, двох і трьох циклів відповідно. Швидкість зменшення вмісту вуглецю, що забруднює, мала тенденцію до збільшення після трьох циклів у порівнянні з одним і двома циклами. Крім того, аналіз SEM-EDS не виявив пошкоджень біоматеріалів після багатократних (до трьох разів, 90 с, малюнок 4) вакуумних плазмових обробок поверхні, тоді як верхня частина поверхні показала кращу змочуваність після трьох циклів (малюнок 5). Усі ці дані наведені в таблицях 2 та 3.


Обговорення
Метою цього дослідження було оцінити, чи може вплив вакуумної плазмової обробки поверхні різних біоматеріалів, що використовуються для збереження альвеол і процедур GBR, покращити їх гідрофільність та змочуваність. Гідрофільність вимірювалася за допомогою часу поглинання чорнила та ступеня змочуваності. Час поглинання чорнила зразків, оброблених плазмою, був значно коротшим, ніж у необроблених зразків. Отже, нульова гіпотеза про відсутність різниці була частково відхилена. Ці початкові in vitro тести вказали на те, що вакуумна плазмова обробка поверхні мала позитивний ефект на кісткові блоки, мембрани перикардію, колагенові матриці та колагенові кісткові трансплантати як за часом поглинання, так і за ступенем змочуваності. Навпаки, вакуумна плазмова обробка поверхні не змогла зменшити час поглинання для некологенових кісткових трансплантатів. Це вказує на те, що вакуумна плазмова обробка поверхні перетворила поверхні висушених біоматеріалів з гідрофобних на високогідрофільні. Однак початкові характеристики поверхні є важливими для визначення очікуваних результатів.
Збільшення загального часу лікування, до трьох циклів, покращило результати. Одне з можливих пояснень полягає в тому, що вуглецеві домішки, як правило, зменшуються після трьох циклів. In vivo, вакуумна плазмова обробка поверхні людської акцелярної дермальної матриці показала покращене інфільтрування фібробластів, що свідчить про покращену біосумісність. У даному дослідженні вакуумна плазмова обробка поверхні продемонструвала деякі позитивні ефекти в термінах дезінфекції оброблених біоматеріалів та активації поверхонь, зменшуючи домішки та підвищуючи їх гідрофільність.
Кілька досліджень у літературі підтвердили ефективність плазмових обробок у термінах адгезії клітин та активності фібробластів. Однак основними темами цих досліджень були стоматологічні абатменти та поверхні імплантів.
Зволожуваність поверхні є одним з найважливіших параметрів, що впливають на біологічну реакцію на імплантований матеріал, впливаючи на адсорбцію білків, адгезію/активацію тромбоцитів, згортання крові та адгезію клітин і бактерій. У даному дослідженні були використані чорнила для вимірювання часу абсорбції та ступеня зволожуваності протестованих біоматеріалів. Поверхневий натяг крові відіграє важливу роль у людському організмі. Згідно з дослідженнями Грнціра та Росіни, поверхневий натяг крові, оцінений у групі з 71 здорового суб'єкта за допомогою методу краплі при температурі 22 градуси Цельсія, становив 55.89 × 10(−3) N × m(−1), з SD = 3.57 × 10(−3) N × m(−1). Враховуючи, що зміни в поведінці поверхневого натягу людської біологічної рідини є характерними для деяких захворювань, для даного дослідження були використані чорнила з поверхневими натягами 56 мН/м та 72 мН/м.
Аналізуючи дані, зібрані в даному дослідженні, було виявлено, що в контрольній групі чорнило з вищим поверхневим натягом (72 мН/м) всмоктувалося швидше, ніж чорнило з нижчим поверхневим натягом (56 мН/м) як кістковими блоками, так і колагеновими ксеноматриксами, але не некологеновими кістковими трансплантатами. Навпаки, в експериментальній групі різниця не була суттєвою. Ці результати можуть означати, що після обробки поверхні вакуумним плазмовим методом варіації в поверхневому натягу можуть бути менш значущими для процесу загоєння.
Після трьох циклів часу зображення SEM топографії поверхні не виявило змін під час обробки поверхні вакуумною плазмою, і фізичних пошкоджень не було зафіксовано. Збільшення гідрофільності, зменшення ступеня забруднення та збереження первісної структури без будь-яких фізичних пошкоджень оброблених плазмою кісткових блоків слід вважати доказом покращеної біосумісності та потенційної біоінтеграції протестованих матеріалів.
Вакуумна плазмова обробка широко використовується в медицині для покращення біосумісності та біоінтеграції в реконструктивних хірургічних втручаннях. Результати подібного дослідження in vitro підкреслюють потенціал плазмової обробки для покращення ефективності hADM у клінічних умовах, пропонуючи багатообіцяючий шлях для покращення результатів реконструктивної хірургії. Крім того, вакуумна плазмова обробка також використовується в інших сферах, таких як підвищення електричних властивостей органосилікатних плівок або зволожуваності поліефірефіркетонових (PEEK) полімерів.
Основним обмеженням даного дослідження є мала кількість зразків і, звичайно, його in vitro природа. Іншим обмеженням є те, що кут зволожуваності повинен був бути наданий замість рівня зволожуваності. Навіть якщо результати з даного дослідження є обнадійливими для вакуумної плазмової обробки поверхні, дані in vitro не дозволяють нам зробити жодних остаточних клінічних висновків. Однак аналіз даних з SEM-EDS показав, що рівень вуглецевих домішок на поверхнях кісткових блоків мав тенденцію зменшуватися при збільшенні кількості циклів часу; отже, можна запропонувати збільшити кількість циклів часу до трьох залежно від використаних замінників кісткових трансплантатів. Більше того, час абсорбції та рівень зволожуваності також покращилися після двох і трьох циклів часу. Що стосується останнього, мембрани перикардіуму та кісткові трансплантати, зокрема некаллагенові кісткові трансплантати, можуть бути оброблені шляхом збільшення кількості циклів до двох або трьох для зменшення ступеня вуглецевих домішок і підвищення їх гідрофільності. Однак для підтвердження цих попередніх результатів необхідні подальші клінічні рандомізовані контрольовані випробування. Іншим обмеженням цього дослідження є те, що оскільки не було багато подібних досліджень у науковій літературі, було нелегко визначити критерій для інтерпретації результатів, особливо щодо рівня зволожуваності протестованих замінників кісткових трансплантатів та резорбованих мембран. Дані з подібних досліджень in vitro та in vivo підтвердили позитивний ефект плазмової обробки на імплантати та абатменти при використанні аргонової плазми. Що стосується останнього, дані з цього дослідження in vitro повинні розглядатися як попередній звіт для заохочення подальших клінічних оцінок.
Висновки
Обробка поверхні вакуумним плазмовим методом статистично збільшила гідрофільність більшості протестованих біоматеріалів, зменшуючи час поглинання та підвищуючи ступінь змочування. Крім того, рівень вуглецевих домішок можна було зменшити, збільшивши час циклу. Однак для підтвердження цих попередніх результатів потрібні подальші рандомізовані контрольовані дослідження з розрахунками розміру вибірки.
Марко Талларіко, Сільвіо Маріо Мелоні, Мікеле Троя, Карлотта Каччіо, Аурея Іммаколата Лумбау, Ієва Гендвілієнє, Франческо Маттіа Черузо та Мілена Пізано
Посилання
- Бузенлехнер, Д.; Фюраузер, Р.; Хаас, Р.; Ватзек, Г.; Майлат, Г.; Поммер, Б. Довгостроковий успіх імплантатів в Академії оральної імплантології: 8-річне спостереження та аналіз факторів ризику. J. Periodontal Implant. Sci. 2014, 44, 102–108. [CrossRef] [PubMed]
- Кім, Т.-І. Дань пам'яті доктору Пер-Інгвару Бранемарку. J. Periodontal Implant. Sci. 2014, 44, 265. [CrossRef] [PubMed]
- Маврогеніс, А.Ф.; Дімітріу, Р.; Парвізі, Дж.; Бабіс, Г.Ц. Біологія остеоінтеграції імплантатів. J. Musculoskelet. Neuronal Interact. 2009, 9, 61–71. [PubMed]
- Пеньярроха, Д.М.; Кавані, У.; Квадрадо, Л. Атлас негайного навантаження зубних імплантатів; Springer International Publishing: Берлін/Гейдельберг, Німеччина, 2019; ISBN 9783030055462, 3030055469.
- Вонг, М.; Еуленбергер, Дж.; Шенк, Р.; Хунцікер, Е. Вплив топології поверхні на остеоінтеграцію імплантаційних матеріалів у трабекулярній кістці. J. Biomed. Mater. Res. 1995, 29, 1567–1575. [CrossRef]
- Веннерберг, А.; Альбректссон, Т. Про поверхні імплантатів: огляд сучасних знань та думок. Int. J. Oral Maxillofac. Implant. 2010, 25, 63–74. [PubMed]
- Веннерберг, А.; Альбректссон, Т. Вплив топографії поверхні титану на інтеграцію кістки: систематичний огляд. Clin. Oral Implant. Res. 2009, 20, 172–184. [CrossRef]
- Беутнер, Р.; Майкл, Дж.; Швенцер, Б.; Шарнвебер, Д. Біологічна нанофункціоналізація поверхонь біоматеріалів на основі титану: гнучкий інструмент. J. R. Soc. Interface 2010, 7, S93–S105. [CrossRef]
- Сун, Х.Д.; Лю, Т.Т.; Ван, Q.Q.; Чжан, Дж.; Цао, М.С. Модифікація поверхні та функціональність для титанових зубних імплантатів. ACS Biomater. Sci. Eng. 2023, 9, 4442–4461. [CrossRef] [PubMed]
- Канулло, Л.; Талларіко, М.; Пеньярроха, М.; Корренте, Г.; Фіорелліні, Дж.; Пеньярроха, Д. Обробка імплантаційних абатментів плазмою аргону у періодично здорових пацієнтів: результати шести років після навантаження рандомізованого контрольованого дослідження. Int. J. Periodontics Restor. Dent. 2017, 37, 683–690. [CrossRef]
- Канулло, Л.; Талларіко, М.; Боттічеллі, Д.; Алккайгюаман, К.А.А.; Нето, Е.Ц.М.; Ксав'єр, С.П. Зміни жорстких і м'яких тканин навколо імплантатів, активованих плазмою аргону: гістоморфометричне дослідження на собаках. Clin. Oral Implant. Res. 2018, 29, 389–395. [CrossRef]
- Ян, Х.Д.; Лі, Б.; Шин, Ч.; Ю, Б.; Ох, Х.С.; Лі, Дж.; Лі, Дж.; Ох, С.К.; Ох, С.Х. Поліпшення біосумісності та біоінтеграції людської безклітинної дермальної матриці шляхом обробки поверхні вакуумною плазмою. Bioengineering 2024, 11, 359. [CrossRef] [PubMed]
- Каваї, Х.; Шібата, Й.; Міязакі, Т. Обробка плазмою з розрядом світла покращує диференціацію остеокластів та їх виживання на титанових пластинах. Biomaterials 2004, 25, 1805–1811. [CrossRef]
- Шібата, Й.; Хосака, М.; Каваї, Х.; Міязакі, Т. Обробка титанових пластин плазмою з розрядом світла покращує адгезію остеобластоподібних клітин до пластин через механізм, опосередкований інтегринами. Int. J. Oral Maxillofac. Implant. 2002, 17, 771–777. [PubMed]
- Канулло, Л.; Генова, Т.; Мандраччі, П.; Муссано, Ф.; Абундо, Р.; Фіорелліні, Дж.П. Морфометричні зміни, викликані обробкою холодною плазмою аргону на остеобластах, вирощених на різних поверхнях зубних імплантатів. Int. J. Periodontics Restor. Dent. 2017, 37, 541–548. [CrossRef] [PubMed]
- Норо, А.; Канеко, М.; Мурата, І.; Йошинарі, М. Вплив топографії поверхні та фізико-хімії поверхні на змочуваність цирконію (тетрагональний цирконій полікристал). J. Biomed. Mater. Res. Biomater. 2013, 101, 355–363. [CrossRef]
- Канулло, Л.; Талларіко, М.; Пеньярроха-Ольтра, Д.; Монье, А.; Ван, Х.; Пеньярроха-Діаго, М. Очищення абатментів імплантатів плазмою аргону: 5-річне спостереження рандомізованого контрольованого дослідження. J. Periodontol. 2016, 87, 434–442. [CrossRef]
- Крітхікадатта, Дж.; Гопікрішна, В.; Датта, М. Керівні принципи CRIS (Перелік для звітування про in-vitro дослідження): концептуальна записка про необхідність стандартизованих керівних принципів для покращення якості та прозорості у звітуванні про in-vitro дослідження в експериментальній стоматології. J. Conserv. Dent. 2014, 17, 301–304. [CrossRef]
- Канулло, Л.; Генова, Т.; Чініго, Г.; Іаконо, Р.; Песче, П.; Меніні, М.; Муссано, Ф. Пристрій для обробки вакуумною плазмою для підвищення активності фібробластів на оброблених та шорстких титанових поверхнях. Dent. J. 2024, 12, 71. [CrossRef]
- Джон, Х.Д.; Чунг, А.; Кім, Х.Д.; Сео, Дж.С.; Кім, Дж.Й.; Юм, М.С.; Гвйон, Б.; Лім, Й. Поліпшена адгезія та проліферація остеобластів на поверхні імплантату, обробленій вакуумною плазмою. Appl. Sci. 2022, 12, 9884. [CrossRef]
- Песче, П.; Меніні, М.; Сантори, Г.; Джованні, Е.Д.; Багнаско, Ф.; Канулло, Л. Фото- та плазмова активація титанових поверхонь зубних імплантатів. Систематичний огляд з мета-аналізом доклінічних досліджень. J. Clin. Med. 2020, 9, 2817. [CrossRef]
- Лі, Х.; Джон, Х.Д.; Чунг, А.; Кім, Дж.; Кім, Дж.Й.; Лі, С.Х.; Кім, Х.; Єом, М.С.; Чое, В.; Гвйон, Б.; та ін. Поліпшення ефективності остеоінтеграції титанових імплантатів шляхом обробки поверхні плазмою. Biomed. Eng. Lett. 2022, 12, 421–432. [CrossRef] [PubMed]
- Фаті-Азарбайджані, А.; Джуйбан, А. Поверхневе натягування в патофізіології людини та його застосування як медичного діагностичного інструменту. Bioimpacts 2015, 5, 29–44. [CrossRef] [PubMed]
- Грнчір, Е.; Розіна, Й. Поверхневе натягування крові. Physiol. Res. 1997, 46, 319–321. [PubMed]
- Бакланов, М.Р.; Гісматулін, А.А.; Наумов, С.; Перевалов, Т.В.; Гриценко, В.А.; Вишневський, А.С.; Рахімова, Т.В.; Воротілов, К.А. Комплексний огляд впливу хімічного складу, обробки плазмою та вакуумного ультрафіолетового (VUV) випромінювання на електричні властивості органосилікатних плівок. Polymers 2024, 16, 2230. [CrossRef]
- Прімц, Г. Стратегії для покращення змочуваності поліефірефіркетонових (PEEK) полімерів шляхом обробки нееквілібріумною плазмою. Polymers 2022, 14, 5319. [CrossRef]
