Повторна місцева доставка гелю гіалуронової кислоти як додаткова терапія залишкових кишень у пацієнтів з пародонтитом, які проходять підтримуючу пародонтологічну допомогу. Рандомізоване контрольоване клінічне дослідження.
Машинний переклад
Оригінальна стаття написана мовою EN (посилання для прочитання) .
Анотація
Мета Оцінити ефект застосування гіалуронової кислоти (ГіА) як додатку до повторної інструментації залишкових кишень у пацієнтів, які проходять регулярну підтримуючу пародонтологічну терапію (ППТ).
Методи Пацієнти з хронічним пародонтитом (стадії III та IV, градації B і C) з 4 міжзубними залишковими кишенями були випадковим чином розподілені на тестову (гель ГіА) або контрольну (фізіологічний розчин) групу. Після субгінгівальної інструментації тестова або контрольна речовина застосовувалася субгінгівально, а потім щоденно супрагінгівально протягом 3 місяців, і, якщо потрібно, повторно після субгінгівальної реінструментації через 3 місяці. Клінічні та пацієнтські результати фіксувалися кожні 3 місяці протягом 12 місяців. Закриття кишень [глибина зондування кишені (ГЗК) ≤ 4 мм з відсутністю кровотечі при зондуванні (КП) на ГЗК = 4 мм] було основним параметром результату.
Результати Було проаналізовано 56 пацієнтів (221 експериментальний сайт). Закриття кишень було досягнуто у 56.8% та 46.6% експериментальних сайтів у тестовій та контрольній групах відповідно (p > 0.05), тоді як медіана ГЗК та розподіл ГЗК (< 5 мм/5 мм/ > 5 мм) суттєво відрізнялися між групами на користь тестової групи через 12 місяців. Крім того, значно менше сайтів у групі ГіА потребували реінструментації через 3 місяці, а сайти в групі ГіА показали тенденцію до нижчих шансів залишитися хворими в порівнянні з контрольною групою (OR 0.48, 95%CI 0.22–1.06). Шанси на те, що сайт залишиться хворим через 12 місяців, значно зросли в присутності нальоту (OR 7.94, 95%CI 4.12–15.28), але в цілому значно зменшилися з часом (OR 0.48, 95%CI 0.28–0.81).
Висновок Повторна інструментація залишкових кишень у пацієнтів з підтримуючою терапією (SPC) сама по собі, призводить до значного збільшення закриття кишень з часом; це було ускладнено поганим контролем за нальотом. Повторне місцеве застосування гіалуронової кислоти (HyA) призводить до меншої кількості ділянок, які потребують повторної інструментації, і може трохи покращити швидкість закриття кишень. (реєстраційний номер clinicaltrials.gov NCT04792541).
Клінічна значущість Гель HyA легко наносити, добре сприймається пацієнтами і може мати певний позитивний ефект у плані меншої кількості ділянок, які потребують повторної інструментації через 3 місяці, та вищої швидкості закриття кишень через 12 місяців.
Вступ
Початкова не хірургічна субгінгівальна інструментація (тобто другий етап терапії), виконана вручну або (ультразвуковими) інструментами (або їх комбінацією), є дуже успішним підходом до лікування пацієнтів з пародонтитом; в середньому, неглибока глибина зондування кишень (PPD) може бути досягнута у 3 з 4 кишень. Нещодавно Всесвітній семінар з класифікації пародонтальних та пері-імплантаційних захворювань і станів та Клінічні практичні рекомендації EFP S3 рівня визначили мету пародонтального лікування. На рівні ділянки закриття кишень визначається як PPD ≤ 4 мм і відсутність кровотечі при зондуванні (BoP), тоді як на рівні пацієнта успішно лікуваний стабільний пацієнт з пародонтитом характеризується наявністю 1) PPD ≤ 4 мм, 2) відсутністю PPD = 4 мм з BoP, і 3) загальною кровотечею в роті < 10%. Хоча досягти цієї мети важко для кожного пацієнта, було показано, що пацієнти, які досягають цих клінічних кінцевих точок, мають знижений рівень прогресування/рецидиву захворювання та втрати зубів через пародонтит під час тривалої підтримуючої пародонтальної терапії (SPC). Отже, використання додаткових продуктів (місцево або системно) під час другого етапу терапії часто обговорюється з метою 1) подальшого покращення швидкості закриття кишень, 2) зменшення потреби в додатковій хірургічній терапії, і/або 3) покращення швидкості досягнення успішно лікуваного стабільного пацієнта з пародонтитом. Це, в свою чергу, повинно не лише покращити тривалу стабільність лікування та зменшити втрату зубів, але й мінімізувати захворюваність пацієнтів і, зрештою, витрати на лікування. Різні варіанти та ефективність місцево введених додатків (тобто модулюючих агентів або антимікробних засобів) під час другого етапу терапії були широко оцінені в рамках Клінічних практичних рекомендацій EFP S3 рівня. Врешті-решт було запропоновано, що лише місцево застосовані препарати з контрольованим вивільненням хлоргексидину та антибіотиків можуть вважатися дійсними варіантами. У цьому контексті є обмежена інформація про "найкращий" момент введення місцево застосованих додатків з точки зору (вартісної) ефективності, тобто чи слід їх застосовувати під час другого етапу терапії або під час третього чи четвертого етапу терапії при повторній інструментації залишкових/рецидивуючих кишень відповідно. Враховуючи вплив пацієнтів, суспільства та/або можливі біологічні наслідки непотрібного використання будь-яких додаткових заходів, останній підхід дозволив би обмежити їх використання лише для тих пацієнтів/ділянок, які не загоюються після початкової субгінгівальної інструментації. Два недавні систематичні огляди охоплювали ефективність додатків для пацієнтів з пародонтитом з залишковими/рецидивуючими кишенями під час SPC. Зокрема, серед місцево введених антимікробних засобів, препарати з контрольованим вивільненням хлоргексидину та волокна тетрацикліну зайняли найвищі позиції з статистично та клінічно значущим додатковим зменшенням PPD приблизно на 0,6 до 0,7 мм, тоді як недостатньо доказів для будь-якого іншого варіанту додаткового лікування (тобто, окрім антимікробних засобів).
Однак ще один локально введений ад'ювант, який не був включений до жодного з вищезазначених систематичних оглядів або до Клінічних практичних рекомендацій EFP S3, - це гіалуронова кислота (HyA). Різні гелі, що містять HyA в різних концентраціях, протягом кількох років тестувалися як ад'юванти до неінвазивного механічного субгінгівального інструментування, і їх ефективність навіть була підсумована в кількох систематичних оглядах. Ці огляди мали добре порівнянні висновки, тобто більшість включених клінічних випробувань повідомляли про позитивний, хоча й помірний, ефект на користь HyA в термінах зменшення PPD та BoP. Однак існувала велика варіація в режимах застосування та частоті в оригінальних дослідженнях, і всі огляди підкреслювали необхідність подальших добре спроектованих рандомізованих контрольованих клінічних випробувань (RCT), включаючи достатнє повідомлення про деталі продукту. У цьому контексті наразі неясно, чи є повторне застосування локально введеного ад'юванта загалом вигіднішим у порівнянні з одноразовим застосуванням, тобто лише одразу після інструментування. Проте 2 недавні RCT оцінили застосування HyA в офісі, зокрема при повторному інструментуванні залишкових/рецидивуючих кишень. Кожне дослідження тестувало різний продукт HyA та частоту застосування; в одному з досліджень HyA було застосовано субгінгівально один раз, тоді як в іншому дослідженні HyA було застосовано субгінгівально на 2 послідовних прийомах, але обидва показали тенденцію на користь застосування HyA.
Отже, здається розумним оцінити, чи має комбіноване місцеве застосування Гіалуронової кислоти, тобто субгінгівально в офісі, після механічної інструментації, та повторне супрагінгівальне застосування пацієнтом один раз на день протягом 3 місяців, потенціал для покращення швидкості закриття кишень у порівнянні з повторною інструментацією лише в лікуванні залишкових кишень у пацієнтів з пародонтитом, які проходять регулярну SPC.
Матеріали та методи
Дизайн дослідження та учасники
Дане дослідження було рандомізованим, подвійно сліпим (пацієнт та спостерігач), контрольованим плацебо, паралельним клінічним випробуванням з 12-місячним спостереженням та звітується відповідно до стандартів звітування клінічних випробувань (Заява CONSORT; Додаток 1). Протокол був затверджений регіональною етичною комісією (Dnr. 2016/468) та зареєстрований на clinicaltrials.gov (NCT04792541); будь-які зміни в протоколі після його публікації наведені в Додатку 2. Набір пацієнтів проводився з грудня 2016 року по січень 2020 року, тобто набір пацієнтів розпочався до Всесвітнього семінару з класифікації пародонтальних та пері-імплантаційних захворювань і станів у 2017 році. Усі пацієнти з пародонтитом, які завершили активну фазу лікування протягом ≥ 6 місяців та були зараховані до регулярної програми SPC (тобто етап 4 лікування) в Спеціалізованій клініці пародонтології (Державна стоматологічна служба, Вермланд, Швеція), які відповідали наступним критеріям включення, були послідовно включені: (i) 35-75 років, (ii) діагноз хронічного пародонтиту, (iii) принаймні 10 залишкових зубів, та (iv) 4-8 міжзубних ділянок з ППД ≥ 5 до < 8 мм та наявність BoP на момент включення. Додатково були визначені наступні критерії виключення: (i) моляри з залученням розгалуження класу II або III, (ii) рухливість зубів класу II або III, (iii) > 2 мм глибший ППД на іншій ділянці в тому ж міжзубному просторі, (iv) антибіотикотерапія протягом попередніх 6 місяців або під час участі в дослідженні, (v) потреба в антибіотикопрофілактиці перед пародонтальним обстеженням та/або лікуванням, (vi) тривале використання протизапальних та імуносупресивних препаратів, (vii) неконтрольований або ново діагностований цукровий діабет до або під час участі в дослідженні, (viii) вагітність або лактація, (ix) важка оклюзійна дисфункція, (x) триваюче ортодонтичне лікування, та (xi) ендодонтичні ураження. Вік, стать, статус куріння (тобто ніколи / колишній / поточний курець) та наявність/відсутність добре контрольованого цукрового діабету були зафіксовані для кожного учасника.
Тестовий та плацебо продукт
Продукт, що використовувався в групі "тест/HyA" для суб- та супрагінгівального застосування, був гелем, що містить гіалуронову кислоту (0,3%, не зшита, середня молекулярна вага; Afta Clear™ Gel; Sunstar Europe SA, Етой, Швейцарія), тоді як група "контроль/плацебо" отримала маленьку пляшечку фізіологічного розчину. Обидва продукти були замасковані білою стрічкою, щоб пацієнт не знав про розподіл по групах.
Втручання, рандомізація та сліпе дослідження
Перед початком дослідження комп'ютерним способом була згенерована випадкова послідовність для розподілу по групах (співвідношення 1:1 для групи тест/HyA та контроль/плацебо) періодонтологом, який не брав участі в процесі набору (KB). Усі учасники були залучені одним з трьох досвідчених стоматологічних гігієністів (LG, AS, MSS). Чотири міжзубні ділянки кожного учасника були визначені як експериментальні ділянки (тобто, мезіобукальний, мезіопалатальний/-лінгвальний, дистобукальний або дистопалатальний/-лінгвальний); якщо це було можливо, вибиралася одна ділянка на квадрант, в іншому випадку експериментальні ділянки повинні були бути в різних міжзубних просторах. Усі учасники отримали на початковому етапі стандартну сесію SPC, що включала повторну інструментацію з ультразвуковим пристроєм (E.M.S. Electro Medical Systems S.A., Ньон, Швейцарія) та/або ручними інструментами (HuFriedyGroup, Чикаго, США) всіх залишкових кишень одним з вищезгаданих трьох стоматологічних гігієністів; кожен пацієнт лікувався одним і тим же стоматологічним гігієністом протягом усього періоду дослідження. Розподіл по групах був прихований до повторної інструментації залишкових кишень. Після повторної інструментації до лікувальної сесії приєднався періодонтолог (AZ), який розкрив розподіл по групах лише для себе, відкривши приховану записку в конверті з формою звіту про випадок пацієнта, і застосував або тестовий, або плацебо продукт субгінгівально на всіх експериментальних ділянках. Для субгінгівального застосування тестовий та плацебо продукти були перенесені в стерильний шприц з тупим голкою, і експериментальні ділянки були заповнені до переповнення продуктом з кишені (Рис. 1). Той же періодонтолог виконував цю процедуру для всіх учасників, тоді як стоматологічні гігієністи та пацієнти залишалися сліпими до розподілу по групах. Кожен пацієнт отримав листівку з коротким викладом відповідних інструкцій та малюнком, що вказує на 4 експериментальні ділянки, включаючи правильний розмір міжзубних щіток (TePe Munhygienprodukter AB, Мальме, Швеція) для конкретного міжзубного простору та або тестового, або плацебо продукту. Пацієнти повинні були застосовувати продукт один раз на день супрагінгівально з міжзубною щіткою після чищення зубів, лише на експериментальних ділянках, протягом наступних 3 місяців до другого візиту на SPC (тобто, 3-місячний контроль). Крім того, пацієнтам було рекомендовано уникати чищення зубів або їжі протягом 3 годин після застосування та не використовувати жодних розчинів для полоскання рота або інших гелів під час участі в даному дослідженні. Сесії SPC повторювалися через 3, 6, 9 і 12 місяців, однак пацієнт припинив застосування тестового або плацебо продукту після перших 3 місяців. Нарешті, всі експериментальні ділянки з PPD = 5 мм і BoP або PPD > 5 мм на 3-місячному контролі знову отримали повторну інструментацію та друге субгінгівальне застосування виділеного продукту, як описано вище. Загалом, всі ділянки з PPD= 5 мм і BoP або PPD>5 мм на будь-якій з сесій SPC отримали як стандарт лікування субгінгівальну повторну інструментацію.
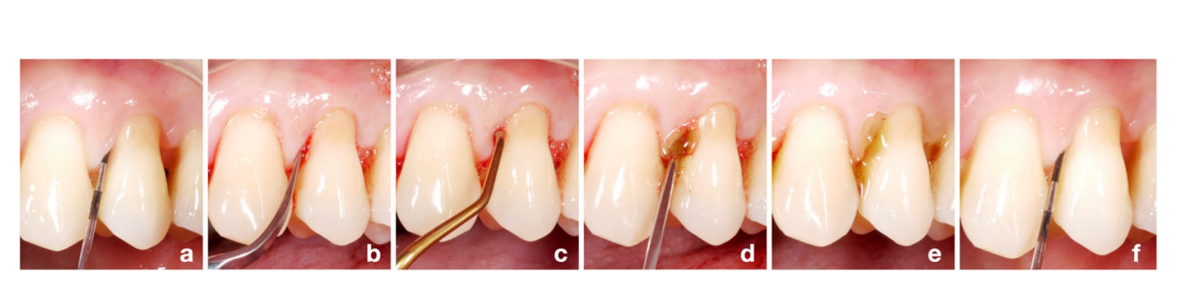
Оцінка результатів та сліпе дослідження
Субгінгівальне мікробіологічне взяття з 4 експериментальних ділянок проводилося на початку дослідження та через 3, 6 і 12 місяців. Результати мікробіологічного взяття будуть опубліковані в іншому місці. Далі, після мікробіологічного взяття та на кожному SPC (тобто на початку дослідження, а також через 3, 6, 9 і 12 місяців) той самий сліпий та калібрований стоматолог-гігієніст (LG, AS, MSS) фіксував PPD, клінічний рівень прикріплення (CAL), наявність/відсутність BoP та наявність/відсутність нальоту на кожній експериментальній ділянці. Як стандарт догляду, пародонтолог (AZ) цієї спеціалізованої клініки контролює вимірювання PPD кожного гігієніста приблизно 2-3 рази на рік, що вважається калібруванням. Далі, на кожному контрольному візиті пацієнтів запитували про будь-які зміни в їх медичній історії та про будь-який прийом антибіотиків за попередні 3 місяці. На другому SPC (тобто через 3 місяці) пацієнти додатково отримали короткий опитувальник про їхню думку щодо протестованого продукту. Опитувальник запитував про наявність та інтенсивність болю під час застосування, а також про думку пацієнтів щодо консистенції та смаку продукту під час домашнього використання, використовуючи шкалу від 1 до 10. Успішний результат лікування (тобто закриття кишені) визначався як PPD≤ 4 мм з відсутністю BoP при PPD = 4 мм; якщо ці критерії не були виконані, експериментальна ділянка залишалася класифікованою як "хвороба". Цей комбінований результат був визначений як первинний параметр результату і оцінювався на кожному SPC.
Критерії відповідності для подальшого спостереження
Пацієнти планувалися на кожні 3 місяці для SPC, однак дозволявся діапазон від 2.5 до 5 місяців між 2 сесіями SPC; якщо час між 2 сесіями SPC перевищував 5 місяців, призначення SPC вважалося пропущеним. Крім того, загальний період від першого до п'ятого призначення SPC не повинен був перевищувати 18 місяців, інакше пацієнт виключався. Оскільки було включено кілька пацієнтів до спалаху пандемії Covid-19, пацієнтам дозволялося пропустити або 6-місячне, або 9-місячне призначення без виключення з дослідження. Однак пацієнти, які пропустили 2 сесії SPC або 3-місячне чи 12-місячне призначення, також виключалися.
Розрахунок розміру вибірки
Для розрахунку розміру вибірки було припущено, що 75% і 25% ділянок у групі тесту/HyA та контрольній/плацебо відповідно досягнуть закриття кишені, тобто PPD ≤ 4 мм за відсутності BoP при PPD = 4 мм. За наявності цих клінічних параметрів ризик прогресування захворювання вважається низьким, а лікування вважається успішним. На основі набору даних попередньої публікації припускається внутрішньоіндивідуальний коефіцієнт кореляції 0.42 для наявності BoP. На основі цього коефіцієнта кореляції, потужності 0.80 та альфа-значення 0.05, було розраховано розмір вибірки 30 учасників на групу (тобто загальна кількість учасників дослідження 60). Для компенсації вибуття було послідовно залучено 80 пацієнтів (40 пацієнтів на групу).
Статистичний аналіз
Частотний розподіл для категоріальних змінних (таких як стать, статус куріння, розподіл PPD тощо) та середні значення (стандартні відхилення) або медіани та міжквартильні діапазони для безперервних змінних (таких як вік, PPD тощо) подаються окремо для групи тесту/HyA та контрольної/плацебо групи. Для перевірки будь-яких відмінностей між групою тесту/HyA та контрольної/плацебо групою застосовувалися або точний тест Фішера, або тест хі-квадрат для категоріальних параметрів (тобто тест хі-квадрат застосовувався, якщо кожна клітинка мала частоту > 5) та для безперервних змінних або незалежний t-тест (для нормально розподілених даних) або тест Манна-Уїтні (для ненормально розподілених даних). Нормальність даних контролювалася за допомогою тесту Шапіро-Уілка. “Стан здоров'я експериментального сайту” визначався як основний параметр результату [дихотомічний; “хворий” (тобто PPD > 4 мм або PPD = 4 мм з BoP) проти “успішно лікуваний/закриття кишені” (тобто PPD ≤4 мм з відсутністю BoP при PPD = 4 мм). Було розраховано дві багатозмінні моделі логістичної регресії з випадковими ефектами, з груповим розподілом як основним предиктором та наступними заздалегідь визначеними конфаундерами: 1) тип зуба (антеріорний / премолярний / молярний), 2) міжпроксимальний сайт (щічний / піднебінний/язиковий), 3) PPD на початковому етапі на експериментальному сайті (5 мм / 6–7 мм), 4) наліт на експериментальному сайті на кожному прийомі (відсутній / присутній), 5) статус куріння (ніколи / колишній / поточний), 6) стать (жінка / чоловік), 7) час, що пройшов між прийомами (місяці), та 8) вік (роки). Перша модель включала лише дані за 3 місяці, тоді як друга модель включала всі дані, зібрані протягом 12-місячного періоду; у останній моделі було додано ще один конфаундер, тобто час спостереження (3- / 6- / 9- / 12-місячне спостереження). Статистичний аналіз проводився за допомогою STATA/IC 17.0 для Mac (Lakeway Drive, Texas, USA), а p-значення ≤ 0.05 вважалося статистично значущим.
Результати
Характеристики населення на початковому етапі (рівень пацієнта)
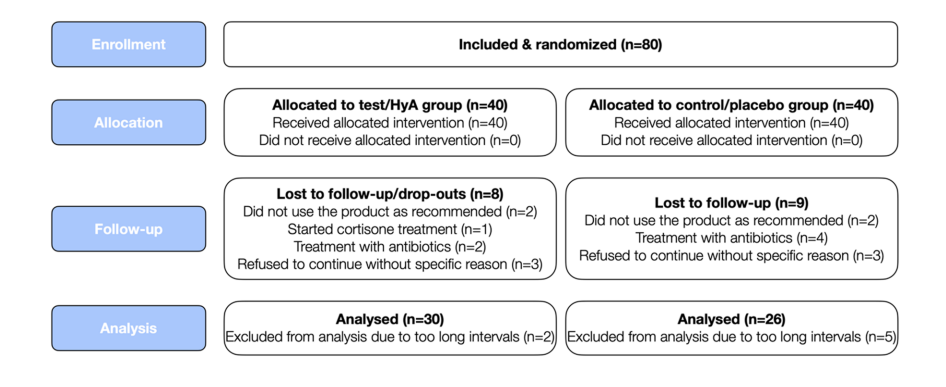
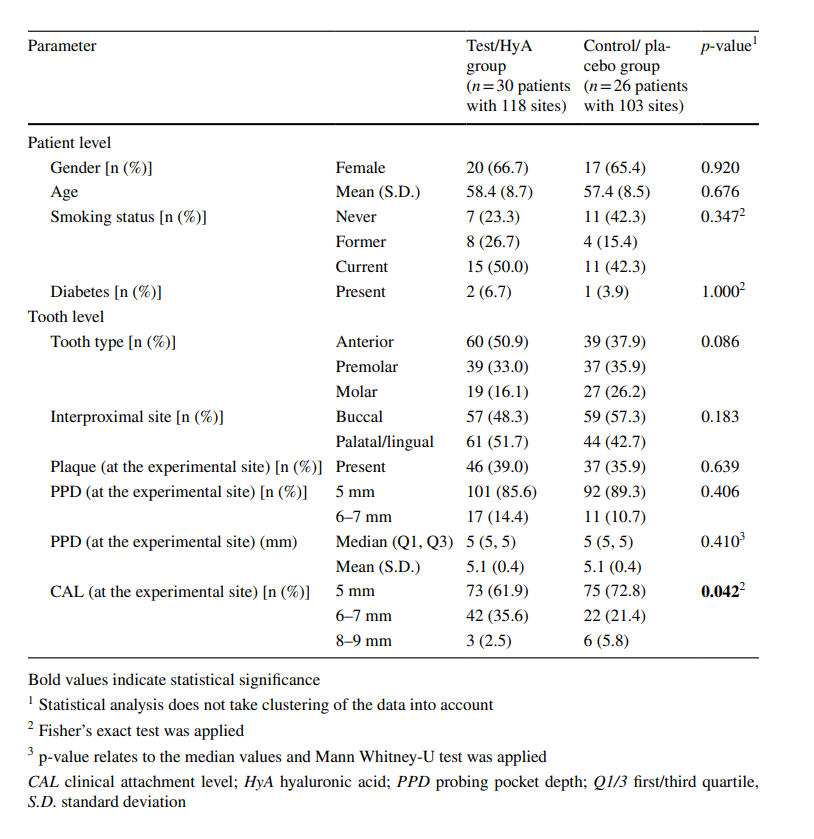
Вісімдесят пацієнтів з хронічним пародонтитом (відповідно до пацієнтів з пародонтитом стадії III та IV та градації B і C), які проходили регулярну SPC, були залучені та рандомізовані. Загалом 24 учасники вибули або не могли бути включені в аналіз з різних причин (деталі див. на рис. 2). Характеристики 56 пацієнтів (тобто 30 і 26 пацієнтів у групі тест/HyA та контроль/плацебо відповідно), які брали участь в аналізі, представлені в таблиці 1; жодна з початкових характеристик на рівні пацієнта не відрізнялася суттєво між 2 групами. Коротко, вибірка 1) складалася приблизно з 66% жінок, 2) мала середній вік 58 років, 3) включала приблизно 46% курців, і 4) мала 3 добре контрольованих діабетиків.
Характеристики експериментальних ділянок на початковому етапі (на рівні зуба)
Вибірка включала 221 експериментальну ділянку, які всі відповідали критеріям відбору і були оцінені як "хворі" з наявністю BoP на початковому етапі. За винятком 3 пацієнтів, кожен пацієнт вніс 4 експериментальні ділянки. Три експериментальні ділянки (по одній ділянці від 2 пацієнтів тест/HyA та 1 пацієнта контроль/плацебо) довелося виключити через реабілітацію з новою протезною реставрацією на експериментальному або сусідньому зубі (n = 2) та через те, що один пацієнт випадково застосував продукт на протилежному зубі, тобто на неправильному (n = 1). Початкові характеристики експериментальних ділянок групи тест/HyA та контроль/плацебо представлені в Таблиці 1. Тип зуба, міжзубні ділянки, наліт та PPD були добре розподілені між 2 групами, тоді як група тест/HyA внесла значно більше ділянок з CAL ≥ 6 мм у порівнянні з групою контроль/плацебо (p = 0.042). Більшість ділянок мали PPD = 5 мм на початковому етапі, тоді як 14.4% та 10.7% групи тест/HyA та контроль/плацебо відповідно мали PPD від 6 до 7 мм на початковому етапі.
Характеристики експериментальних ділянок через 3 місяці (на рівні зуба)
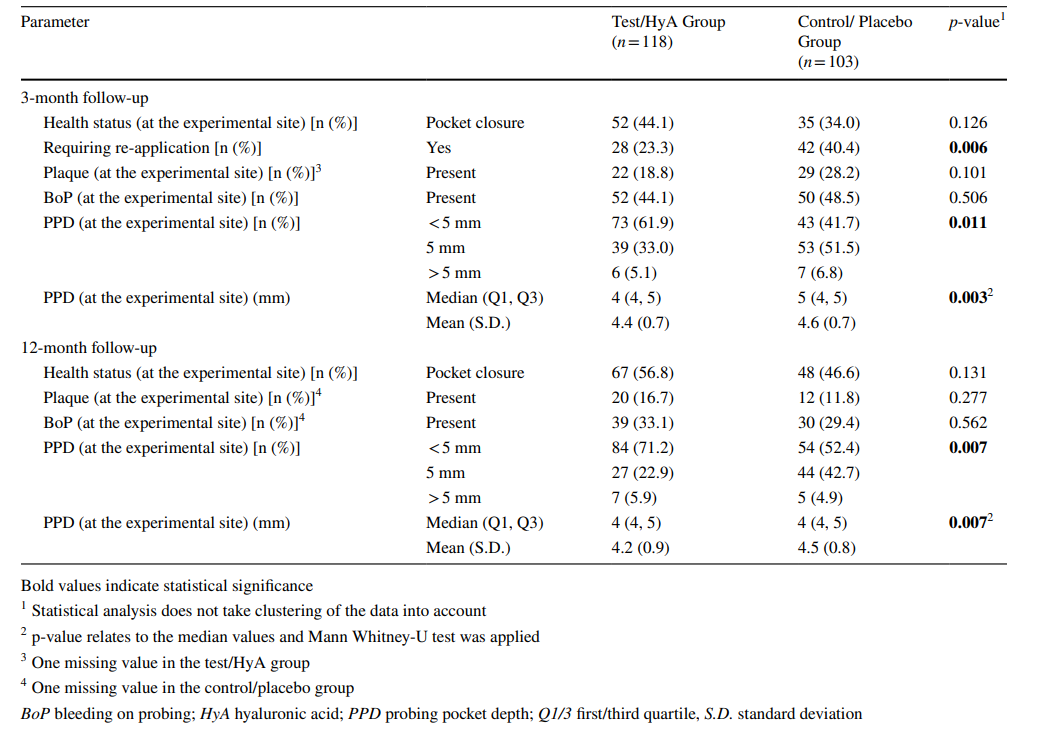
Характеристики експериментальних ділянок через 3 місяці наведені в таблиці 2. Через 3 місяці 44.1 та 34.0% експериментальних ділянок групи тест/HyA та контрольної/плацебо відповідно досягли закриття кишень без значної різниці між групами. Аналогічно, наявність нальоту та BoP була порівнянною між 2 групами. Проте, медіана PPD (p = 0.003) та розподіл PPD (< 5 мм / 5 мм / > 5 мм; p = 0.011) суттєво відрізнялися між групами на користь групи тест/HyA. Зокрема, 61.9 та 41.7% експериментальних ділянок групи тест/HyA та контрольної/плацебо відповідно мали PPD < 5 мм. Крім того, значно менше ділянок у групі тест/HyA (p = 0.006) порівняно з групою контроль/плацебо, 23.3 та 40.4% відповідно, вимагали субгінгівальної повторної обробки на 3-місячному контролі.
Оцінка результатів лікування через 3 місяці
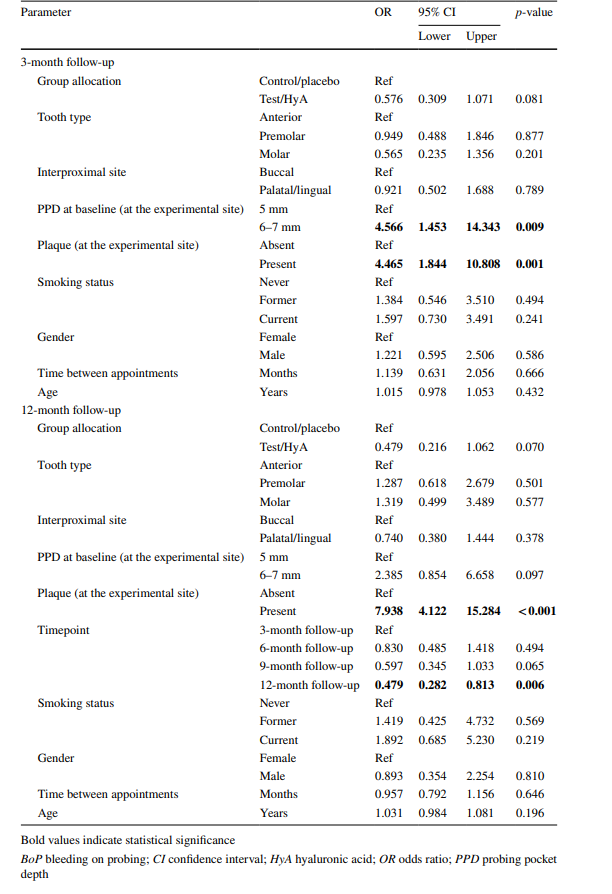
Результати багатозмінного змішаного логістичного регресійного аналізу через 3 місяці SPC представлені на рис. 3a та в таблиці 3. Експериментальні ділянки в групі тест/HyA мали дещо, але статистично незначно нижчі шанси залишитися "хворими" (тобто, PPD > 4 мм або PPD = 4 мм з BoP) (OR 0.58, 95% CI 0.31–1.07; p = 0.081). З включених конфаундерів лише наліт і PPD на початку мали значний вплив на результат. Зокрема, наявність нальоту (OR 4.47, 95% CI 1.84–10.81; p = 0.001) та вищий PPD на початку (OR 4.57, 95% CI 1.45–14.34; p = 0.009) значно збільшили шанси залишитися "хворими" на 3-місячному контролі.
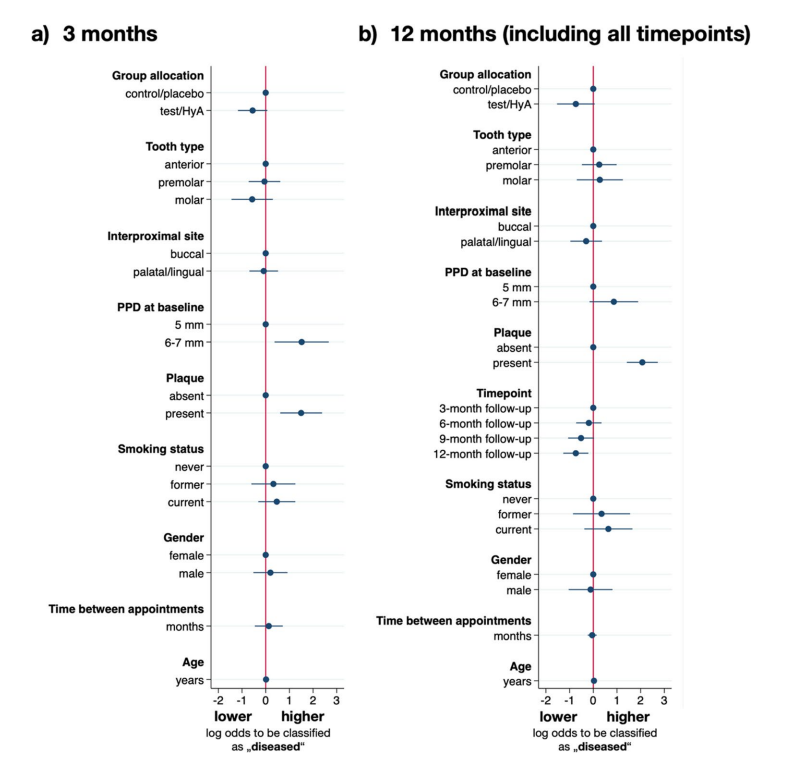
Характеристики експериментальних сайтів після 12 місяців (рівень зуба)
Характеристики експериментальних ділянок на фінальному оцінюванні (через 12 місяців) наведені в таблиці 2. На фінальному оцінюванні 56.8% та 46.6% експериментальних ділянок групи тест/HyA та контрольної/плацебо відповідно досягли закриття кишень без значної різниці між групами. Подібно, наявність нальоту та BoP були порівнянні між 2 групами. Проте, медіана PPD (p = 0.007) та розподіл PPD (< 5мм / 5 мм / > 5мм; p = 0.007) суттєво відрізнялися між групами на користь групи тест/HyA. Зокрема, 71.2% та 52.4% ділянок тест/HyA та контрольної/плацебо відповідно мали PPD < 5 мм, а медіана PPD була нижчою в групі тест/HyA. У групі тест/HyA з 28 експериментальних ділянок, які отримали повторне застосування через 3 місяці, 28.6% більше не були хворими через 12 місяців, тоді як з 90 експериментальних ділянок, які не отримували повторне застосування через 3 місяці, 34.4% знову були класифіковані як “хворі”. У контрольній/плацебо групі з 42 експериментальних ділянок, які отримали повторне застосування через 3 місяці, 33.3% більше не були хворими через 12 місяців, тоді як з 61 експериментальної ділянки, які не отримували повторне застосування через 3 місяці, 44.3% знову були класифіковані як “хворі”.
Оцінка результатів лікування через 12 місяців
Результати багатозмінного змішаного регресійного аналізу логістичної регресії представлені на рис. 3b та в таблиці 3. Експериментальні ділянки групи тест/HyA мали дещо, але статистично незначно нижчі шанси залишитися "хворими" (тобто, PPD > 4 мм або PPD = 4 мм з BoP) в порівнянні з контрольною/плацебо групою (OR 0.48, 95% CI 0.22–1.06; p = 0.070). З включених конфаундерів лише наліт і час мали значний вплив на результат. Зокрема, наявність нальоту значно підвищила шанси залишитися "хворими" приблизно в 8 разів (OR 7.94, 95% CI 4.12–15.28; p < 0.001), і, в цілому, шанси залишитися "хворими" зменшувалися протягом періоду дослідження, досягаючи значущості на фінальному оцінюванні (OR 0.48, 95% CI 0.28–0.81; p = 0.006).
Думка пацієнтів
Один пацієнт з кожної групи повідомив про біль у яснах під час застосування продукту з інтенсивністю 3-4 з 10, де 10 означає максимальний біль. Один пацієнт з групи тест/HyA не відповів на питання про консистенцію, а один пацієнт з контрольної/плацебо групи не відповів на питання про смак. Групи не продемонстрували значних відмінностей у своїй думці щодо консистенції та смаку продукту (Рис. 4). Зокрема, середні значення (середнє квадратичне відхилення) шкали для консистенції становили 7.2 (2.6) та 7.0 (3.0) у групі тест/HyA та контрольній/плацебо групі відповідно (p = 0.822), а медіанні значення (перший, третій квартиль) шкали для смаку становили 8.5 (7, 10) та 10 (8, 10) у групі тест/HyA та контрольній/плацебо групі відповідно (p = 0.184); для обох параметрів значення 10 означало дуже задоволеність.
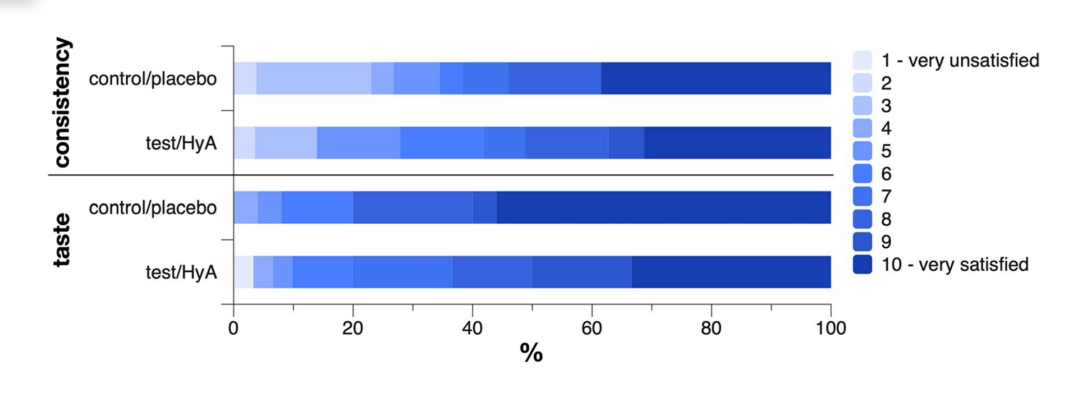
Безпека
Жоден з пацієнтів не повідомив про побічні ефекти/ускладнення, пов'язані з застосуванням продукту, і жодних негативних подій не було виявлено клінічно.
Обговорення
Локально доставлені хіміотерапевтичні засоби часто використовуються як доповнення до нехірургічного лікування у пацієнтів з пародонтитом, як на початковій стадії лікування, так і в залишкових/рецидивуючих кишенях на пізніших етапах лікування. Однак, оскільки початкове нехірургічне субгінгівальне інструментування є досить успішним лікуванням саме по собі, більш специфічний підхід для кишень, які не загоїлися під час другого етапу терапії, і/або рецидивуючих кишень під час SPC може бути більш релевантним підходом. У цьому випадку гель, що містить HyA, який повторно застосовувався (щодня) протягом 3 місяців, як доповнення до повторного інструментування залишкових/рецидивуючих кишень у пацієнтів, які проходили регулярний SPC, показав певну тенденцію до покращення результату, тобто було виявлено на 10% вищий рівень закриття кишень для ділянок, які отримували HyA, порівняно з тими в контрольній групі, які отримували фізіологічний розчин (тобто 57 проти 47% ділянок відповідно) через 12 місяців. Крім того, відсоток експериментальних ділянок з PPD < 5 мм був приблизно в 1.4 рази вищим у тестовій/HyA групі порівняно з контрольною/плацебо групою (тобто 71 і 52% ділянок відповідно).
Ці результати узгоджуються з тими, що були повідомлені в 2 недавніх РКТ, які оцінювали гель, що містить гіалуронову кислоту (HyA), як доповнення до повторної інструментації залишкових/рецидивуючих кишень і показали, що використання гелю, що містить HyA, призвело до тенденції до кращих результатів у порівнянні з лише повторною інструментацією. Більше того, обидва дослідження повідомили в своїй тестовій групі про подібну частоту ділянок з ПДП < 5 мм після 12 місяців, а саме 76-77% у 2 попередніх дослідженнях і 71% тут. Крім того, в одному з РКТ, що повідомляло про закриття кишень (тобто ПДП ≤ 4 мм без кровотечі), було спостережено порівнянну частоту в групі HyA, а саме 59% і 57% відповідно. Однак значна різниця між цими 2 РКТ і поточним дослідженням стосується характеристик продукту застосованого гелю HyA. Конкретно, в цьому дослідженні використовувався не зшитий, середньомолекулярний HyA з відносно низькою концентрацією (0,3%), тоді як в інших дослідженнях або використовувався продукт з зшитим, високомолекулярним HyA з вищою концентрацією, або комбінований продукт з полінуклеотидами та високомолекулярним HyA з вищою концентрацією. Лабораторні дослідження на періодонтальних клітинах або патогенах, асоційованих з пародонтитом, порівнювали ефекти або не зшитого, або зшитого HyA, або HyA різних молекулярних ваг; жодна з протестованих формул не показала негативного ефекту з точки зору загоєння пародонтальних ран. У цьому контексті, через відсутність порівняльних клінічних випробувань до теперішнього часу, залишається незрозумілим, чи дійсно різні характеристики HyA перетворюються на клінічно значущі відмінності. Ще одна різниця між цими 2 РКТ і цим дослідженням стосується режиму/частоти застосування HyA. У цьому дослідженні гель, що містить HyA, повторно (щоденно) застосовувався супрагінгівально протягом 3 місяців пацієнтами на додаток до субгінгівальних офісних застосувань. Одне з попередніх досліджень оцінювало ефект повторного офісного застосування після 3 місяців, але не змогло продемонструвати жодного додаткового позитивного ефекту HyA після повторного застосування; однак перед повторним застосуванням у цьому конкретному дослідженні не проводилася додаткова субгінгівальна інструментація. Тут лише ділянки з залишковими ознаками патології отримали повторне застосування в поєднанні з субгінгівальною повторною інструментацією. У обох групах (тобто тестовій та контрольній) приблизно 30% ділянок, які вимагали повторної інструментації та повторного застосування, були визнані успішно лікуваними наприкінці випробування. Тим не менш, хоча повторне лікування покращило ситуацію в 1 з 3 випадків і жодного чітко позитивного ефекту HyA не було відзначено, кількість ділянок, які вимагали повторної інструментації (повторного лікування) через 3 місяці, була значно нижчою в групі HyA, у порівнянні з тією, що отримувала NaCl. Нарешті, також поточні дані не дозволяють зробити жодних висновків щодо будь-якого потенційного додаткового ефекту повторного супрагінгівального застосування пацієнтами протягом 3 місяців, оскільки тут не вистачало третьої групи з субгінгівальним офісним введенням лише.
В цілому, зменшення кількості залишкових кишень після активного пародонтального лікування (тобто, етапи 1 до 3) було виявлено корисним з точки зору рецидиву/прогресування захворювання та втрати зубів у різних дослідженнях, що зосереджені на довгострокових результатах SPC після активного пародонтального лікування. Таким чином, розумно припустити, що будь-який лікувальний захід, такий як використання локально застосованих додатків, який покращує швидкість закриття кишень – незалежно від стадії лікування – може позитивно вплинути також на довгостроковий результат. У цьому контексті гелі, що містять HyA, як додаток до субгінгівальної інструментації на другому етапі терапії, продемонстрували певний потенціал у зменшенні PPD та BoP, що було підтверджено більш сучасними RCT. У порівнянні з іншими дослідженнями з подібним дизайном, але з оцінкою різних продуктів як додатків до повторної інструментації залишкових кишень у пацієнтів з SPC, частота закриття кишень тут здавалася трохи нижчою. Наприклад, 2 недавні RCT, що оцінювали додатковий ефект безшовного застосування похідних емалі, гелю натрію гіпохлориту та гелю хлоргексидину, повідомили про закриття кишень (тобто, PPD ≤ 4 мм без BoP) у 80, 78 та 63% ділянок порівняно з 57% тут. Отже, враховуючи відсутність RCT, які безпосередньо порівнюють ці продукти, HyA виявилася подібно ефективною до гелю CHX, але трохи меншою за похідні емалі та гель натрію гіпохлориту. Останнє може бути особливим інтересом, оскільки комбінація гелю натрію гіпохлориту з перехреснозв'язаним гелем HyA нещодавно привернула увагу як комбіноване додаткове лікування у пацієнтів з пародонтитом. Однак нещодавнє ретроспективне серійне дослідження, що включало 29 пацієнтів з SPC з залишковими/рецидивуючими кишенями, повідомило про дещо нижчу частоту закриття кишень для цього комбінованого підходу – 25%.
Серед факторів, які використовувалися для корекції поточного аналізу, два мали значний вплив на результати фінальної оцінки, а саме контроль за нальотом і дотримання/час, що добре узгоджується з літературою. Зокрема, тут наявність нальоту, яка оцінювалася на кожному експериментальному майданчику на кожній сесії SPC, значно знижувала ймовірність досягнення закриття кишені. Успішно мотивувати пацієнтів на підтримання високого рівня контролю за нальотом під час SPC є добре відомим клінічним викликом, і нещодавні довгострокові дослідження SPC підтвердили клінічну значущість цього. Обидва дослідження, в яких брали участь 100 і більше 200 осіб відповідно, які проходили приблизно 10 років SPC після активного пародонтального лікування, показали підвищений ризик рецидиву захворювання та втрати зубів через пародонтит при поганому контролі за нальотом. Крім того, пацієнти поточного RCT показали в загальному і незалежно від групової належності значне покращення з часом, яке стало значним після 12 місяців. Зокрема, також у контрольній/плацебо групі майже 50% експериментальних майданчиків досягли закриття кишені наприкінці випробування. Цей ефект досягнення закриття кишені лише за допомогою механічної повторної інструментації добре порівнянний з попередніми дослідженнями, які повідомляли про показники від 42 до 60%. Крім того, участь у дослідженні сама по собі, ймовірно, має позитивний ефект на дотримання з точки зору пацієнта, але також з точки зору лікаря-стоматолога/стоматологічного гігієніста, який може бути більш наполегливим у дотриманні 3-місячного інтервалу. У цьому контексті було показано, що коротший час між послідовними сесіями SPC може з часом призвести до зменшення PPD і пародонтальної стабільності, тоді як довший час може призвести до пародонтальної нестабільності і, відповідно, до втрати зубів.
Дослідження, проведене в умовах "реального життя", має деякі обмеження, такі як відносно високий рівень відмови 30%, що не дозволило досягти запланованого розміру вибірки в контрольній/плацебо групі, тобто було проаналізовано 26 замість 30 учасників. Високий рівень відмови, принаймні частково, зумовлений тим, що учасники пропускали свої заплановані візити під час пандемії Covid-19, тобто, хоча було прийнято інтервал від 2.5 до 5 місяців між 2 сесіями SPC, майже 10% учасників (тобто 2 і 5 з групи тест/HyA та контроль/плацебо відповідно) були виключені з аналізу через занадто довгі інтервали. Тим не менш, оскільки час між 2 сесіями SPC виявляється важливим фактором, цей параметр був включений у регресійний аналіз, щоб виправити в моделі незначні варіації в інтервалах SPC. Однак, оскільки дане випробування було проведене в дизайні паралельних груп, пацієнти не отримували обидва продукти, що, в свою чергу, повинно обмежити будь-який упередженість через недостатню сліпоту пацієнтів. У цьому контексті було цікаво, що групи не продемонстрували значних відмінностей щодо думки пацієнтів про консистенцію та смак продукту; обидва продукти були добре сприйняті пацієнтами, що, в свою чергу, може свідчити про хорошу відповідність.
Висновок
Повторна інструментація залишкових кишень у пацієнтів з SPC, сама по собі, призводить до значного збільшення закриття кишень з часом. Це покращення залежало від гігієни рота пацієнта, тобто наявність нальоту збільшувала ймовірність залишитися хворим приблизно в 8 разів. Додаткова суб- та супрагінгівальна повторна аплікація гелю, що містить HyA, призвела до значно меншої кількості ділянок, які потребували повторної інструментації через 3 місяці, а також до деяких клінічно значущих відмінностей після 12 місяців SPC в порівнянні з контрольною/плацебо групою, таких як 71 проти 52% експериментальних ділянок, які досягли PPD < 5 мм, відповідно. Однак статистична значущість цього ефекту була трохи пропущена в скоригованому аналізі досягнення закриття кишень. Отже, потрібні подальші клінічні випробування, щоб підтвердити перевагу цього додатку в порівнянні з субгінгівальною повторною інструментацією.
Автори: Крістіна Бертл, Стефанія Влаху, Ніколаос Пандіс, Антоніс Зампеліс, Андреас Ставропулос
Посилання:
- Санз М, Еррера Д, Кебшулл М та ін. (2020) Лікування періодонтиту стадії I-III - клінічні практичні рекомендації EFP S3. J Clin Periodontol 47(Suppl 22):4–60. https://doi.org/10.1111/jcpe.13290
- Суван Дж, Лейра Й, Морено Санчо ФМ, Граціані Ф, Деркс Дж, Томасі С (2020) Субгінгівальна інструментація для лікування періодонтиту. Систематичний огляд. J Clin Periodontol 47(Suppl 22):155–175. https://doi.org/10.1111/jcpe.13245
- Чаппл ІЛК, Мілі БЛ, Ван Дайк ТЕ та ін. (2018) Пародонтальне здоров'я та гінгівальні захворювання та стани на незайманому та зменшеному пародонті: консенсусний звіт робочої групи 1 Всесвітнього семінару 2017 року з класифікації пародонтальних та пері-імплантних захворювань і станів. J Clin Periodontol 45(Suppl 20):S68–S77. https://doi.org/10.1111/jcpe.12940
- Бертл К, Пандіс Н, Стопфер Н, Харіріан Х, Брукманн С, Ставропулос А (2022) Вплив статусу "успішно лікуваного стабільного пацієнта з періодонтитом" на параметри результатів, пов'язані з пацієнтом, під час довгострокового підтримуючого пародонтального лікування. J Clin Periodontol 49:101–110. https://doi.org/10.1111/jcpe.13582
- Ратту В, Райнді Д, Антоноглу Г, Нібалі Л (2023) Поширеність стабільних та успішно лікуваних пацієнтів з періодонтитом та випадки подальшої втрати зубів під час підтримуючого пародонтального лікування: систематичний огляд з мета-аналізами. J Clin Periodontol. https://doi.org/10.1111/jcpe.13835
- Донос Н, Кальчіоларі Е, Брусселарс Н, Голдоні М, Бостанджі Н, Белібасакіс ГН (2020) Додаткове використання модулюючих агентів у неоперативній пародонтальній терапії. Систематичний огляд рандомізованих, плацебо-контрольованих клінічних досліджень. J Clin Periodontol 47(Suppl 22):199–238. https://doi.org/10.1111/jcpe.13232
- Еррера Д, Матесанц П, Мартін С, Уд В, Ферес М, Тейгельс В (2020) Додатковий ефект локально введених антимікробних засобів у терапії періодонтиту: систематичний огляд та мета-аналіз. J Clin Periodontol 47(Suppl 22):239–256. https://doi.org/10.1111/jcpe.13230
- Кальчіоларі Е, Еркал П, Дуроу М, Аккалі А, Тагліаферрі С, Донос Н (2022) Ефективність додаткових пародонтальних терапій під час підтримуючого пародонтального лікування у пацієнтів з залишковими кишенями. Систематичний огляд та мета-аналіз. J Periodontal Res 57:671–689. https://doi.org/10.1111/jre.13001
- Ван ЦЙ, Ян ЙХ, Лі Х та ін. (2020) Додаткові локальні лікування для пацієнтів з залишковими кишенями під час підтримуючого пародонтального лікування: систематичний огляд та мережевий мета-аналіз. J Clin Peri- odontol 47:1496–1510. https://doi.org/10.1111/jcpe.13379
- Бертл К, Брукманн С, Ісберг ПЕ, Клінге Б, Готфредсен К, Ставропулос А (2015) Гіалуронан у неоперативній та хірургічній пародонтальній терапії: систематичний огляд. J Clin Periodontol 42:236–246. https://doi.org/10.1111/jcpe.12371
- Еліезер М, Імбер ДжК, Скулян А, Пандіс Н, Тейх С (2019) Гіалуронова кислота як додаток до неоперативної та хірургічної пародонтальної терапії: систематичний огляд та мета-аналіз. Clin Oral Investig 23:3423–3435. https://doi.org/10.1007/s00784-019-03012-w
- Каракостас П, Давидопулу С, Кальфас С (2022) Використання гіалуронової кислоти в лікуванні пародонтальних захворювань: систематичний огляд. J Contemp Dent Pract 23:355–370
- Тан ОЛ, Сафії Ш, Разалі М (2021) Клінічна ефективність повторних застосувань локальної доставки лікарських засобів та додаткових агентів у неоперативній пародонтальній терапії: систематичний огляд. Antibiotics (Basel) 10:1178. https://doi.org/10.3390/antibiotics10101178
- Піллоні А, Рохас МА, Трезза Ч та ін. (2023) Клінічні ефекти додаткового використання полінуклеотидного та гіалуронової кислоти на основі гелю під час субгінгівальної повторної інструментації залишкових пародонтальних кишень: рандомізоване, спліт-майт клінічне дослідження. J Periodontol 94:354–363. https://doi.org/10.1002/JPER.22-0225
- Піллоні А, Зеза Б, Куіс Д та ін. (2021) Лікування залишкових пародонтальних кишень за допомогою гелю на основі гіалуронової кислоти: 12-місячне багатосерединне рандомізоване тричі сліпе клінічне дослідження. Antibiotics (Basel) 10:924. https://doi.org/10.3390/antibiotics10080924
- Шульц КФ, Алтман ДГ, Мохер Д, CONSORT Г (2010) Заява CON-SORT 2010: оновлені рекомендації щодо звітування про паралельні групові рандомізовані випробування. PLoS Med 7:e1000251. https://doi.org/ 10.1371/journal.pmed.1000251
- Папапаноу ПН, Санз М, Будунелі Н та ін. (2018) Пародонтит: консенсусний звіт робочої групи 2 Всесвітнього семінару 2017 року з класифікації пародонтальних та пері-імплантних захворювань і станів. J Clin Periodontol 45(Suppl 20):S162–S170. https:// doi.org/10.1111/jcpe.12946
- Тонетті МС, Грінвелл Х, Корнман КС (2018) Стадіювання та градація пародонтиту: структура та пропозиція нової класифікації та визначення випадків. J Clin Periodontol 45(Suppl 20):S149– S161. https://doi.org/10.1111/jcpe.12945
- Армітаж ГК (2000) Розробка системи класифікації пародонтальних захворювань і станів. Northwest Dent 79:31–35
- Гамп СЕ, Німан С, Ліндхе Дж (1975) Пародонтальне лікування багатокореневих зубів. Результати через 5 років. J Clin Periodontol 2:126–135. https://doi.org/10.1111/j.1600-051x.1975.tb01734.x
- Аспарухова МБ, Кіряк Д, Еліезер М, Міхов Д, Скулян А (2019) Активність двох препаратів гіалуронану на первинних людських оральних фібробластах. J Periodontal Res 54:33–45. https://doi.org/10. 1111/jre.12602
- Фудзіока-Кобаяші М, Мюллер ХД, Мюллер А та ін. (2017) Впливи гіалуронової кислоти на клітини людського періодонтального зв'язку in vitro. BMC Oral Health 17:44. https://doi.org/10.1186/ s12903-017-0341-1
- Мюллер А, Фудзіока-Кобаяші М, Мюллер ХД та ін. (2017) Вплив гіалуронової кислоти на морфологічні зміни поверхонь дентину та подальший вплив на виживання, прикріплення та розповсюдження клітин періодонтального зв'язку. Clin Oral Investig 21:1013–1019. https://doi.org/10.1007/s00784-016-1856-6
- Чен М, Лі Л, Ван З, Лі П, Фенг Ф, Чжен Х (2019) Гіалуронова кислота великої молекулярної маси регулює запалення та міграцію, індуковані P. gingivalis, у людських гінгівальних фібробластах через сигнальний шлях MAPK та NF-κB. Arch Oral Biol 98:75–80. https:// doi.org/10.1016/j.archoralbio.2018.10.027
- Данневіц Б, Зейдлер А, Хюзінг Дж та ін. (2016) Втрата молярів у пацієнтів, які проходили пародонтальне лікування: результати через 10 років і більше після активної пародонтальної терапії. J Clin Periodontol 43:53–62. https:// doi.org/10.1111/jcpe.12488
- Граєц Ц, Шутцхольд С, Плауманн А та ін. (2015) Прогностичні фактори втрати молярів - 18-річне ретроспективне когортне дослідження. J Clin Periodontol 42:943–950. https://doi.org/10.1111/jcpe.12460
- Граєц Ц, Плауманн А, Шлаттманн П та ін. (2017) Довгострокове збереження зубів при хронічному пародонтиті - результати після 18 років консервативного пародонтального лікування в університетських умовах. J Clin Periodontol 44:169–177. https://doi.org/10.1111/jcpe.12680
- Матуліне Г, П'єтурссон БЕ, Сальві ГЕ та ін. (2008) Вплив залишкових кишень на прогресування пародонтиту та втрату зубів: результати після 11 років підтримки. J Clin Periodontol 35:685– 695. https://doi.org/10.1111/j.1600-051X.2008.01245.x
- Сальві ГЕ, Мішлер ДС, Шмідлін К та ін. (2014) Фактори ризику, пов'язані з тривалістю життя багатокореневих зубів. Довгострокові результати після активної та підтримуючої пародонтальної терапії. J Clin Periodontol 41:701–707. https://doi.org/10.1111/jcpe.12266
- Аріель Х, Кан А, Хіла ЗО, Антон С, Натан Г, Колерман Р (2022) Термосенситивний гель з активним інгредієнтом гіалуронової кислоти, що містить систему збереження оксетінідину, як доповнення до чистки та планування коренів: рандомізоване проспективне клінічне дослідження. Clin Oral Investig 26:3721–3733. https://doi.org/10.1007/s00784-021-04344-2
- Мохаммад КА, Мірза БА, Махмуд ЗС, Зардаві ФМ (2023) Вплив гелю гіалуронової кислоти на пародонтальні параметри, про-запальні цитокіни та біохімічні маркери у пацієнтів з періодонтитом. Gels 9:325. https://doi.org/10.3390/gels9040325
- Олшевська-Чиж І, Кралік К, Прпіч Дж (2021) Біомолекули в стоматологічних застосуваннях: рандомізоване контрольоване клінічне дослідження, що оцінює вплив додаткової терапії гіалуроновою кислотою на клінічні параметри помірного пародонтиту. Biomolecules 11:1491. https://doi.org/10.3390/biom11101491
- Раманаускайте Е, Мачюльскіене В, Шираката Й, Двилене УМ, Недзельскіене І, Скулян А (2023) Клінічна оцінка натрію гіпохлориту/амінокислот та перехресно-зв'язаного гіалуронату, додаткових до неоперативного пародонтального лікування: рандомізоване контрольоване клінічне дослідження. Clin Oral Investig. https://doi.org/10.1007/ s00784-023-05271-0
- Єнтш ХФР, Роццузо М, Піллоні А, Касай А, Фіммерс Р, Єпсен С (2021) Безфлапове застосування похідної матриці емалі в повторному лікуванні пародонтиту: багатосерединне рандомізоване дослідження доцільності. J Clin Periodontol 48:659–667. https://doi.org/10.1111/jcpe.13438
- Радулеску В, Боаріу МІ, Русу Д та ін. (2022) Клінічні та мікробіологічні ефекти одноразового застосування гелю натрію гіпохлориту під час субгінгівальної повторної інструментації: тричі сліпе рандомізоване плацебо-контрольоване клінічне дослідження. Clin Oral Investig 26:6639–6652. https://doi.org/10.1007/s00784-022-04618-3
- Діхл Д, Фрідман А, Лідлофф П, Юнг РМ, Скулян А, Білах Х (2022) Додаткове застосування гіалуронової кислоти в комбінації з гелем натрію гіпохлориту для неоперативного лікування залишкових кишень зменшує потребу в пародонтальній хірургії - ретроспективний аналіз клінічної серії випадків. Materials (Basel) 15:6508. https://doi.org/10.3390/ma15196508
- Коста ФО, Коста АМ, Кортеллі ДжР та ін. (2023) Вплив контролю над надясеневим нальотом на рецидивуючий пародонтит та клінічну стабільність серед осіб, які проходять підтримуючу пародонтальну терапію: 10-річне спостереження. J Periodontol 94:55–65. https://doi.org/10. 1002/JPER.22-0301
- Томасі С, Кутузіс Т, Венстром ЙЛ (2008) Локально введений доксициклін як доповнення до механічного очищення під час повторного лікування пародонтальних кишень. J Periodontol 79:431–439. https:// doi.org/10.1902/jop.2008.070383
- Рамсайєр КА, Нідеггер М, Уолтер С та ін. (2019) Час між візитами на контроль та залишкові глибини зондації передбачають довгострокову стабільність у пацієнтів, які проходять підтримуючу пародонтальну терапію. J Clin Periodontol 46:218–230. https://doi.org/10.1111/jcpe.13041