Гіалуронова кислота при видаленні зубів: систематичний огляд та мета-аналіз доклінічних і клінічних випробувань
Машинний переклад
Оригінальна стаття написана мовою EN (посилання для прочитання) .
Анотація
Мета Оцінити, чи призводить застосування гіалуронової кислоти (ГК) у тварин або пацієнтів з ≥ 1 видаленим зубом до кращого загоєння та/або покращеного управління ускладненнями в порівнянні з будь-яким іншим лікуванням або без лікування.
Матеріали та методи Три бази даних були досліджені до квітня 2022 року. Найбільш релевантними критеріями відбору були (1) місцеве застосування ГК як доповнення до видалення зуба або як лікування альвеолярного остеїту, і (2) наявність клінічних, рентгенографічних, гістологічних або даних, що повідомляються пацієнтами. Формування нової кістки та/або її якість вважалися основними параметрами результату в доклінічних дослідженнях, тоді як біль, набряк і тризм визначалися як основні параметри результату в клінічних дослідженнях.
Результати Було включено п’ять доклінічних і 22 клінічні дослідження (1062 пацієнти на фінальному етапі оцінки). У доклінічних випробуваннях ГК застосовували в лунці для видалення зуба. Хоча позитивний ефект ГК спостерігався у всіх окремих дослідженнях на формування кістки, цей ефект не був підтверджений мета-аналізом. У клінічних дослідженнях ГК застосовували в лунці для видалення зуба або використовували як спрей чи ополіскувач. Застосування ГК після неоперативного видалення нормально прорізаних зубів може позитивно вплинути на загоєння м’яких тканин. На основі мета-аналізів, застосування ГК після хірургічного видалення нижніх третіх молярів (НМ3) призвело до значного зменшення сприйняття болю через 7 днів після операції в порівнянні з відсутністю додаткової маніпуляції з раною або застосуванням плацебо/носія. Ранній післяопераційний біль, тризм і ступінь набряку не змінилися.
Висновки Застосування HyA може позитивно вплинути на зменшення болю після видалення LM3, але не після екстракції нормально прорізаних зубів.
Клінічна значущість Застосування HyA може позитивно вплинути на зменшення болю після хірургічного видалення LM3, але, здається, не має жодного впливу на інші ускладнення або після екстракції нормально прорізаних зубів. Крім того, здається, що це не зменшує моделювання альвеолярного гребеня після екстракції, хоча доклінічні дослідження показують підвищене утворення кістки.
Вступ
Хоча процес загоєння після видалення зуба зазвичай проходить без ускладнень, будь-який подальший біль може погіршити добробут пацієнтів, а також можуть виникнути ускладнення. Наприклад, хірургічна екстракція напів-/повністю імпактних третіх молярів регулярно супроводжується значним болем, набряком і тризмом, які посилюються у випадку розвитку альвеолярного остеїту (AO)— також відомого як суха ямка. AO вважається одним з найпоширеніших ускладнень видалення зубів, що трапляється в 20-35% випадків хірургічної екстракції нижніх третіх молярів (LM3) і в 1,4-5% (нехірургічної) екстракції регулярно прорізаних зубів. Окрім таких ранніх ускладнень, які негативно впливають на якість життя пацієнтів, ускладнене загоєння лунки після екстракції може також призвести до значних дефектів твердих тканин, як на місці екстракції, так і на сусідніх зубах. Наприклад, повідомлялося, що глибокі пародонтальні дефекти, наприклад, глибини зондування ≥ 7 мм, на дистальному боці другого моляра виникають майже у кожного четвертого пацієнта після екстракції імпактного LM3.
Щоб зменшити захворюваність пацієнтів і покращити загоєння м'яких і твердых тканин після видалення зубів, а також для лікування ранніх ускладнень (наприклад, AO), було протестовано різні матеріали та/або хірургічні техніки (наприклад, застосування колагенових спонжів, гелів, кров'яних похідних, різних матеріалів для пересадки). Останнім часом зростає увага до гіалуронової кислоти (HyA) через її протизапальні та антибактеріальні властивості, а також позитивний вплив на загоєння м'яких і твердых тканин. Зокрема, доклінічні дослідження продемонстрували позитивний гістологічний ефект на загоєння кісткових і пародонтальних дефектів після застосування HyA. На основі результатів мета-аналізів систематичного огляду клінічних випробувань щодо хірургічного видалення третіх молярів, у групах, що отримували продукти на основі HyA, було зафіксовано значне зменшення болю на третій і сьомий післяопераційний день, але не на тризмус. У цьому контексті відсутня всебічна оцінка доступних доклінічних і клінічних доказів щодо впливу застосування HyA у зв'язку з видаленням зубів загалом, включаючи поширеність, обсяг та/або управління ускладненнями. Тому в даному систематичному огляді було розглянуто таке питання PICOS (популяція (P), втручання (I), порівняння (C), результати (O) та дизайн дослідження (S)): “У тварин/пацієнтів, у яких видалено ≥ 1 зуб, чи призводить застосування HyA самостійно або в поєднанні з іншими продуктами/носіями до кращого загоєння м'яких/твердых тканин, зменшення захворюваності, зменшення частоти ускладнень та/або покращення управління ускладненнями в порівнянні з будь-яким іншим лікуванням або без лікування?”.
Матеріали та методи
Протокол дослідження та реєстрація дослідження
У даній роботі були дотримані наявні рекомендації щодо проведення систематичних оглядів доклінічних та клінічних досліджень (Рекомендовані елементи для систематичних оглядів та мета-аналізу (PRISMA); Додаток 1). Обидва протоколи були зареєстровані в міжнародному перспективному реєстрі систематичних оглядів (PROSPERO), а саме, один для доклінічних (CRD42021266190) та один для клінічних випробувань (CRD42021266183).
Джерела інформації, пошук літератури та критерії відповідності
Пошук літератури був проведений у 3 базах даних (тобто, Ovid (MEDLINE та CENTRAL), EMBASE та Pubmed) 14 жовтня 2021 року та оновлений 7 квітня 2022 року. Деталі пошуку, включаючи ключові слова, представлені в Додатку 2. Після видалення дублікатів, заголовки та анотації були перевірені на відповідність двома рецензентами (DD, TL), а значення каппи для перевірених повних текстів та остаточно включених публікацій були розраховані. Будь-яка неоднозначність була вирішена в обговоренні з третім автором (KB). Незалежно від типу дослідження, дослідження були включені, якщо (a) написані англійською або німецькою мовами, (b) повний текст був доступний, і (c) були надані клінічні, рентгенографічні або гістологічні дані. Додатковими критеріями включення для доклінічних досліджень були (a) рандомізовані та нерандомізовані контрольовані експерименти, та (b) місцеве застосування продукту на основі гіалуронової кислоти самостійно або в комбінації з іншим продуктом в ≥ 1 з груп після видалення ≥ 1 зуба. Додатковими критеріями включення для клінічних досліджень були (a) рандомізоване контрольоване випробування (RCT), контрольоване випробування (CT) або серія випадків з мінімум 10 пацієнтами, та (b) місцеве застосування продукту на основі гіалуронової кислоти самостійно або в комбінації з іншим продуктом в ≥ 1 з груп або після видалення ≥ 1 зуба, або як лікування AO ≥ 1 зуба.
Збір та витяг даних
Два автори (DD, KB) незалежно витягли дані двічі, і будь-які розбіжності були вирішені в обговоренні з третім автором (AS). З доклінічних досліджень було витягнуто таку інформацію: (a) перший автор, (b) рік публікації, (c) дизайн дослідження, (d) модель лікування, (e) місце лікування, (f) вид, (g) форма застосування HyA, (h) лікувальні групи, (i) період спостереження, (j) доступні параметри результатів, та (k) деталі фінансування. Аналогічно, з клінічних випробувань було витягнуто таку інформацію: (a) перший автор, (b) рік публікації, (c) дизайн дослідження, (d) характеристики пацієнтів (тобто стать, вік, стан здоров'я та куріння), (e) специфічні критерії включення для місця, (f) кількість місць на початковому етапі та останньому спостереженні, (g) лікувальні групи, (h) деталі продукту, (i) форма застосування, (j) період спостереження, (k) післяопераційні медикаменти, (l) доступні параметри результатів, (m) клінічна обстановка (тобто приватна практика або університетська обстановка), та (n) деталі фінансування. Нарешті, вся доступна інформація про продукти на основі HyA була узагальнена, тобто (a) торгова назва, (b) виробник, (c) концентрація, (d) хімічна форма, та (e) форма застосування.
Оцінка ризику упередженості
Для доклінічних випробувань використовувався інструмент оцінки ризику упередженості (RoB) SYRCLE. Як було запропоновано, були оцінені такі критерії як “низький”, “високий” або “неясний” ризик упередженості: (1) генерація послідовності, (2) базові характеристики, (3) приховування розподілу, (4) випадкове розміщення, (5) сліпе тестування доглядальників або дослідників, (6) випадкова оцінка результатів, (7) сліпе оцінювання результатів, (8) неповні дані про результати, (9) селективна звітність про результати та (10) інші джерела упередженості. Для кожного дослідження було розраховано кількість та відсоток позитивно оцінених пунктів (тобто “оцінка якості”).
Для RCT використовувався інструмент RoB 2.0 Корану. Ризик упередженості оцінювався як “низький”, “високий” або “деякі” занепокоєння для кожного з наступних критеріїв: (1) процес рандомізації, (2) відхилення від запланованих втручань, (3) відсутні дані про результати, (4) вимірювання результату, (5) вибір звітного результату та (6) загальний ризик упередженості. Для нерандомізованих випробувань використовувався інструмент ROBINS-I. Ризик упередженості оцінювався як “низький”, “помірний”, “серйозний”, “критичний” або “немає інформації” для наступних критеріїв: (1) спотворення, (2) вибір учасників, (3) класифікація втручань, (4) відхилення від запланованих втручань, (5) відсутні дані про результати, (6) вимірювання результату, (7) вибір звітного результату та (8) загальний ризик упередженості.
Оцінка була проведена 2 рецензентами (DD, KB), і у разі будь-якої неоднозначності консенсус був досягнутий шляхом обговорення з третім автором (AS). Один автор повторив оцінку (DD).
Синтез результатів та статистичний аналіз
Для доклінічних досліджень основними параметрами результату вважалися нове утворення кістки та об'єм кістки на об'єм тканини (BV/TV), тоді як для клінічних досліджень основними параметрами результату були визначені біль, тризмус та набряк. Дані були витягнуті з тексту, таблиць та фігур, розраховані та/або були зв'язані з авторами оригінальних публікацій.
У разі виявлення принаймні 2 рандомізованих досліджень з порівнянним дизайном дослідження (тобто, показання до лікування, режим HyA, період спостереження, оцінка результатів) було проведено парний мета-аналіз. Мета-аналізи були обмежені РКД, таким чином включаючи дослідження з вищою методологічною якістю. Групи, що застосовували HyA, або порівнювалися з негативною контрольною групою (тобто, без додаткового лікувального етапу), або з контрольною групою, що застосовувала інше лікування, включаючи плацебо або носійний матеріал тестової групи (“плацебо/носій”). Парні мета-аналізи були проведені для кожного окремого порівняння, а також загалом. Для розрахунку гетерогенності (τ2) використовувався обмежений максимальний правдоподібність, а для врахування невеликої кількості досліджень - корекція стандартної помилки за методом Кнаппа-Гартунга. Було розраховано середню різницю між контрольною та тестовою групами, стандартну помилку середньої різниці та 95% довірчий інтервал (CI). У дослідженнях, що використовували дизайн "розділеного рота", дані розглядалися як залежні при розрахунку стандартної помилки середньої різниці з установкою r = 0.5. Для оцінки гетерогенності використовувався тест хі-квадрат, а значення p < 0.1 вважалося показником значної гетерогенності. Додатково був проведений тест I2 на однорідність, щоб кількісно оцінити ступінь гетерогенності, і у разі принаймні 3 порівнянних досліджень був додатково розрахований 95% прогнозний інтервал. Статистичний аналіз був проведений за допомогою STATA/IC 17.0 для Mac.
Якість доказів (GRADE)
Впевненість у мета-аналітичних доказах доклінічних та клінічних випробувань, що включені в даний документ, була підсумована за допомогою Грейдингу оцінки рекомендацій, розробки та оцінки (GRADE). Для обох типів випробувань, доклінічних та клінічних, використовувалося програмне забезпечення GRADEpro GDT (Інструмент розробки рекомендацій, Університет Макмастера та Evidence Prime, 2022) для оцінки якості доказів результатів.
Результати
Вибір досліджень та характеристики
Пошук літератури представлений у Додатку 3; було виявлено 147 потенційних посилань, і після видалення дублікатів залишилося 90 досліджень для скринінгу заголовків та анотацій. Загалом 57 досліджень було видалено з різних причин, залишивши 33 дослідження для повного текстового аналізу. Після виключення ще 6 досліджень, у яких тип продукту не відповідав критеріям включення або був неправильний дизайн дослідження, у даний систематичний огляд було включено 5 доклінічних та 22 клінічних дослідження. Обидва рецензенти повністю погодилися щодо вибраних досліджень для повнотекстового скринінгу (коефіцієнт Каппа Коена = 1; 100% згода), тоді як суттєва згода була досягнута щодо остаточного включення досліджень (коефіцієнт Каппа Коена = 0.61; 84.9% згода).
У всіх доклінічних випробуваннях HyA застосовувався в лунці зуба після видалення регулярно прорізаних зубів. Клінічні випробування були поділені на 3 групи відповідно до показань до лікування: (1) хірургічне видалення LM3 (RCT (n = 10), CT (n = 1)), (2) видалення регулярно прорізаних зубів (RCT (n = 7), нерандомізоване дослідження з розділеним ротом (n = 1), проспективна серія випадків (n = 1)), та (3) лікування AO (RCT (n = 1), проспективна серія випадків (n = 1)).
Популяція дослідження
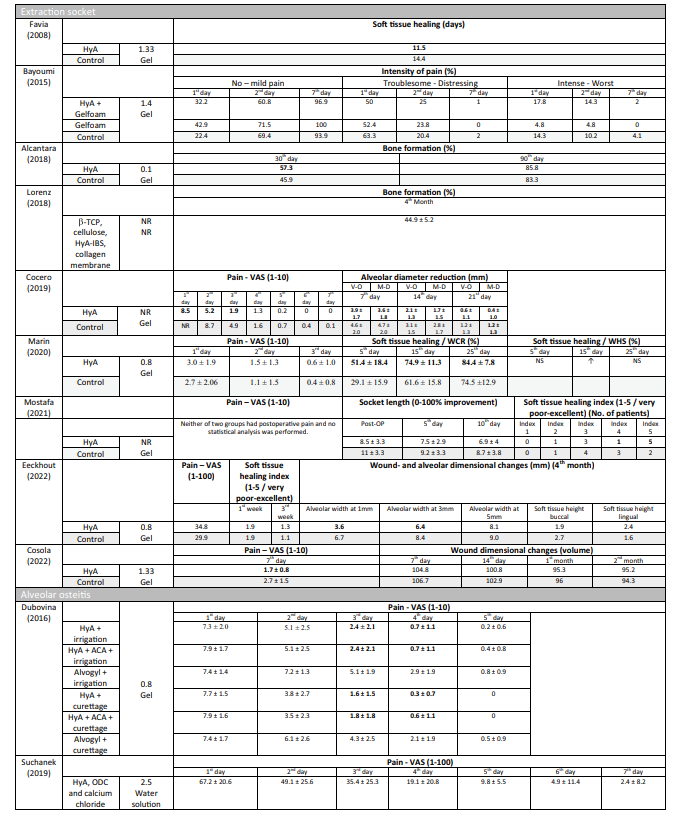
Що стосується доклінічних досліджень, 2 дослідження включали 5–11 щурів Холцмана або 5–6 щурів Вістара в різних групах, відповідно, тоді як 3 дослідження використовували собак породи бігль (всього 20 собак). У дослідженнях на щурах HyA застосовувався в лунці для видалення як у здорових, так і у діабетичних тварин, тоді як у дослідженнях на собаках HyA застосовувався в інфікованих лунках для видалення (Таблиця 1).
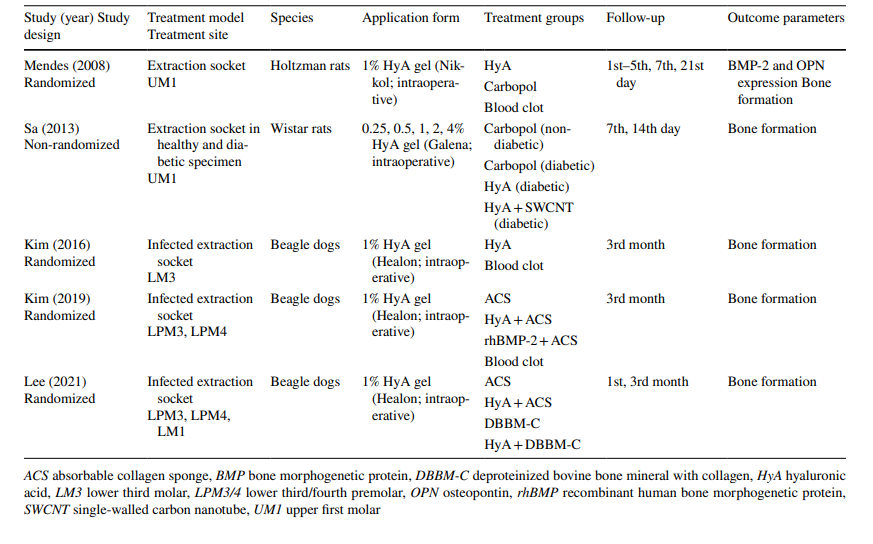
Клінічні дослідження з видалення хірургічного LM3, екстракції регулярно прорізаних зубів та лікування AO включали в остаточну оцінку 603, 349 та 110 пацієнтів відповідно, що внесли 306, 226 та 90 оброблених ділянок HyA, а також 370, 257 та 20 контрольних/необроблених ділянок HyA відповідно (Таблиця 2). У більшості досліджень пацієнти були системно здоровими, тоді як одне дослідження стосувалося пацієнтів з хронічним захворюванням печінки або діабетом; 4 дослідження не повідомляли про стан здоров'я пацієнтів. Статус куріння був зазначений у 12 дослідженнях; 8 досліджень включали лише некурців, 2 дослідження включали пацієнтів, які курили ≤ 10 сигарет/день, а 2 дослідження включали обидва, тобто некурців та курців. Десять досліджень не надали жодної інформації про статус куріння.
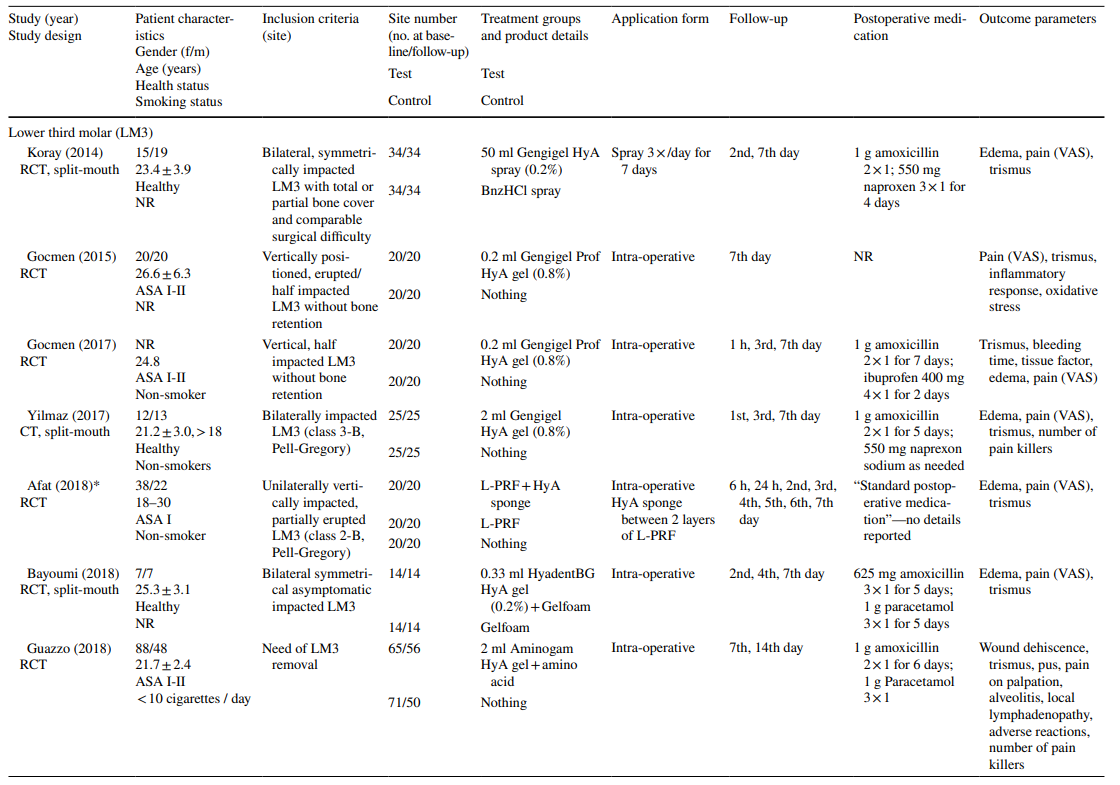
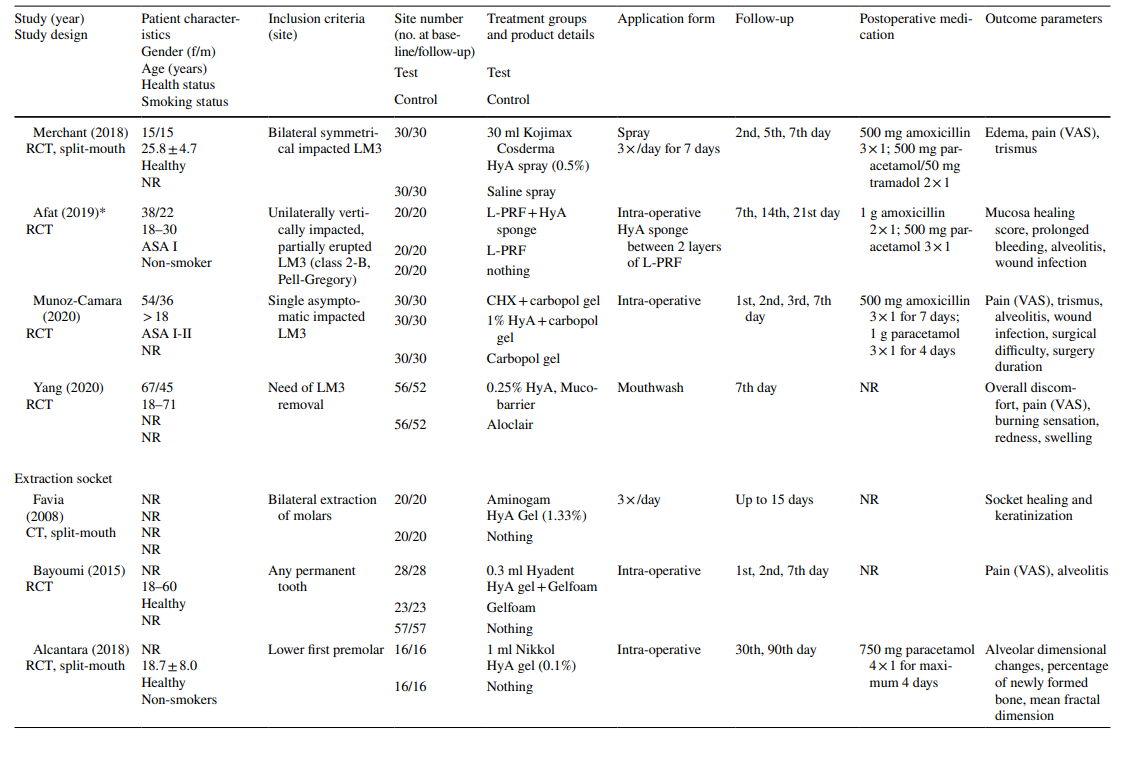
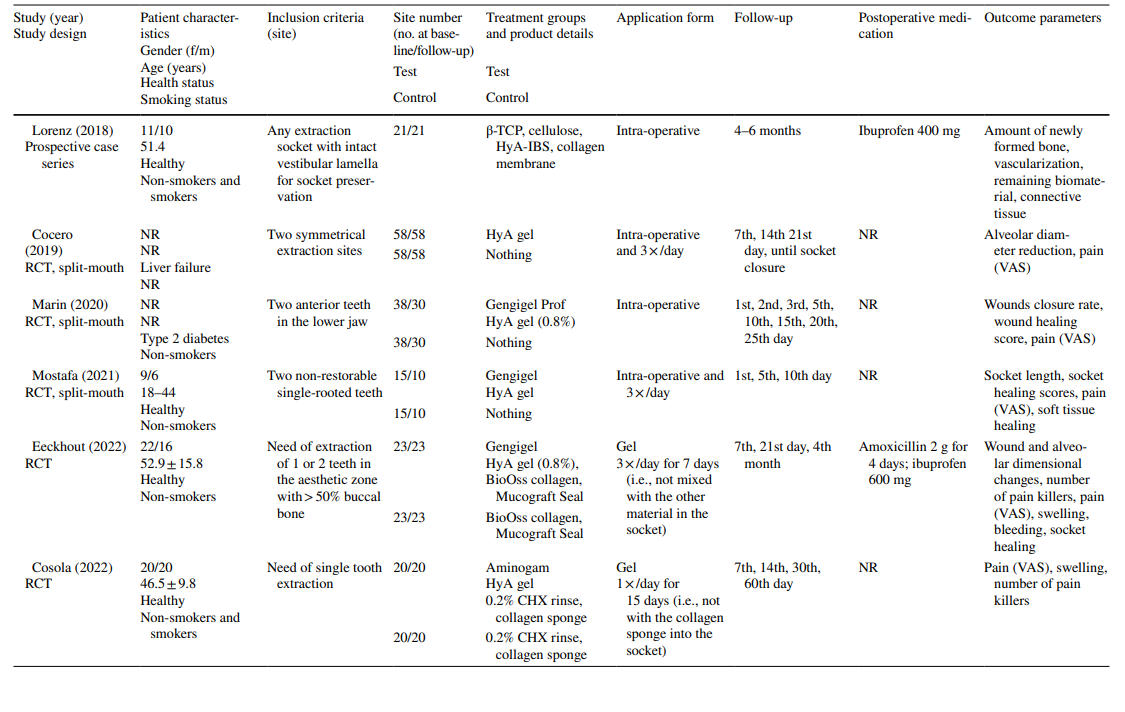
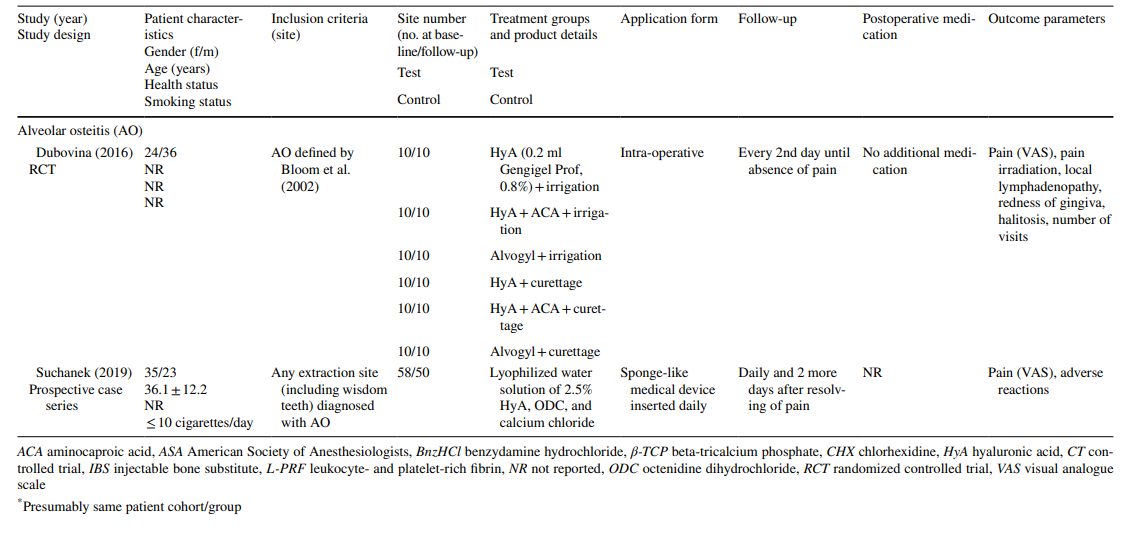
У дослідженнях щодо екстракції LM3 зуби були асимптоматичними, переважно вертикально імпактованими або напівімпактованими, що дозволяло первинне закриття рани після хірургічного видалення. Половина досліджень з екстракції регулярно прорізаних зубів включала лише однокореневі зуби (або передні зуби, або премоляри), тоді як інша половина включала або моляри, або будь-який тип зуба. Обидва дослідження в групі лікування AO включали всі типи зубів, що відповідали критеріям AO відповідно до Blum et al. (2002).
Інтервенція дослідження
У всіх доклінічних випробуваннях HyA застосовувався у вигляді гелю в лунку екстракції безпосередньо після видалення зуба або самостійно (n = 3) або в комбінації з абсорбуючою колагеновою губкою (n = 2) (Таблиця 1).
У більшості клінічних досліджень (n = 19) (Таблиця 2), HyA застосовувався у вигляді гелю під час операції в лунку екстракції або післяопераційно на місці екстракції або самостійно (n = 13) або з деяким носієм (тобто абсорбуюча колагенова губка (n = 3), фібрин, багатий на лейкоцити та тромбоцити (n = 2), або замінники кістки (n = 1)). У решті 3 клінічних досліджень HyA використовувався або у вигляді спрею 3 рази на день протягом 1 тижня (n = 2), або як ополіскувач для рота (n = 1).
Інформація про HyA
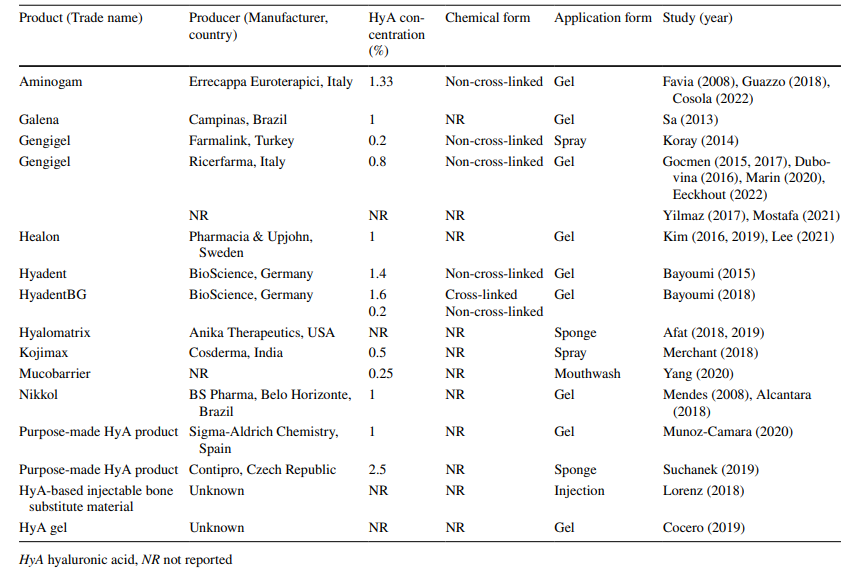
У 5 доклінічних та 22 клінічних дослідженнях, що були включені, використовувалися 11 комерційних, 2 саморобних та 2 HyA продукти невідомого походження (Таблиця 3). У всіх доклінічних дослідженнях (n = 5) HyA застосовувався у вигляді гелю, тоді як у клінічних дослідженнях HyA застосовувався у вигляді гелю (n = 15), спрею (n = 2), ополіскувача для рота (n = 1) або в комбінації з губкою (n = 3) або матеріалом для заміни кістки (n = 1) під час виготовлення. Концентрація HyA варіювала від 0.2% у спреї, 0.25% в ополіскувачі для рота, до 2.5% у самостійно виготовленій губці HyA, тоді як у 5 дослідженнях концентрація HyA не була вказана. Хімічна форма, тобто, не зшита або зшита, не була вказана в більшості досліджень (n = 16), тоді як 10 досліджень використовували не зшитий HyA, а одне дослідження поєднувало не- та зшитий HyA.
Клінічна обстановка та деталі фінансування
Усі доклінічні випробування фінансувалися незалежними одноразовими або багатократними дослідницькими грантами.
У одному клінічному дослідженні було повідомлено про багатопрофільний дизайн дослідження, що включав 8 медичних центрів, тоді як всі інші клінічні дослідження проводилися в одному відділі в університетському середовищі. У одинадцяти клінічних дослідженнях не було повідомлено про джерела фінансування, тоді як у 9 клінічних дослідженнях фінансування надавалося відділом; однак у 3 з цих 9 досліджень гель HyA був наданий виробником. У єдиному дослідженні фінансування було надано 3 різними дослідницькими фондами.
Повідомлені результати та спостереження
У доклінічних дослідженнях формування кістки оцінювалося різними методами через 14 днів і 3 місяці після операції. Одне дослідження додатково вивчало рівень білка морфогенетичного кістки-2 та остеопонтина (Таблиця 1). Крім того, 4 дослідження не зафіксували жодних побічних ефектів після застосування HyA, тоді як одне дослідження не повідомило про відсутність/наявність побічних ефектів.
У клінічних дослідженнях оцінювані параметри результатів варіювали в залежності від показань до лікування (Таблиця 2). У дослідженнях з хірургічного видалення LM3, наявність болю, виміряного за допомогою візуальної аналогової шкали (VAS), набряку та тризму були параметрами результатів, які найчастіше оцінювалися. Інші, менш часто оцінювані параметри, включали наявність/відсутність тривалого кровотечі, наявність/відсутність розходження м'яких тканин, швидкість загоєння слизової оболонки, частоту AO/інфекції рани та лабораторні маркери запалення, окисного стресу та загоєння рани. Серед досліджень з видалення регулярно прорізаних зубів, 3 публікації використовували різні бали загоєння лунки/м'яких тканин, 3 публікації оцінювали кількість новоутвореної кістки та/або зміни розмірів альвеоли, 3 публікації оцінювали біль, а одне дослідження оцінювало частоту AO. Обидва дослідження з лікування AO зосередилися на оцінці болю та побічних реакцій. Більшість клінічних досліджень не зафіксували побічних ефектів після місцевого застосування HyA, тоді як 6 досліджень не згадували про відсутність/наявність побічних ефектів. Одне дослідження, яке застосовувало 0,8% гель HyA після видалення LM3, повідомило про значно подовжений час кровотечі після закриття рани в порівнянні з контрольною групою; однак, оскільки гемостаз був у межах фізіологічного часу, це не вважалося небажаною подією.
Резюме результатів окремих досліджень
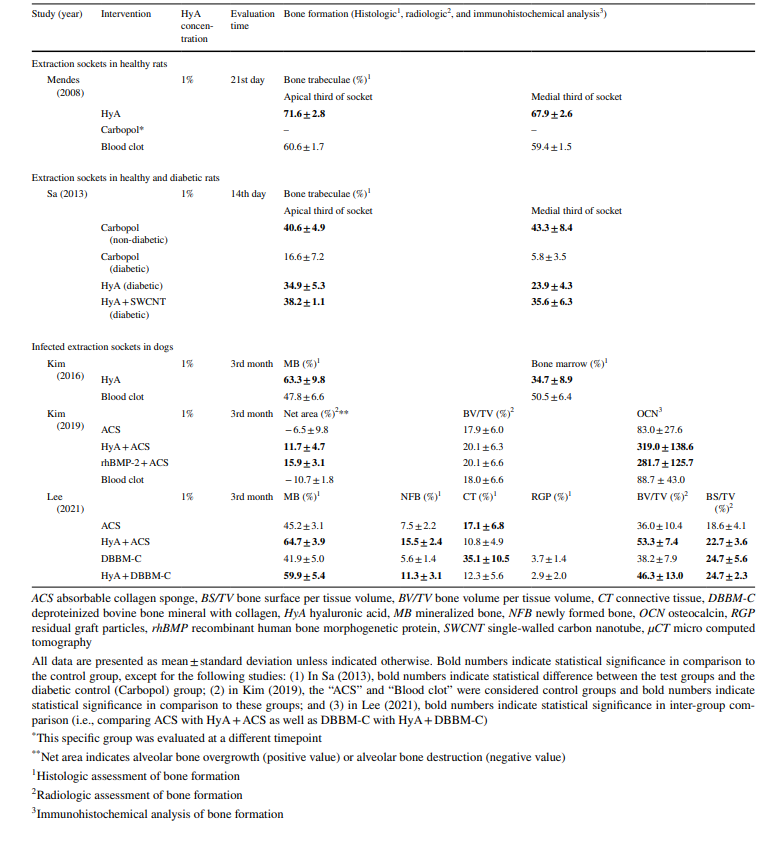
У всіх доклінічних дослідженнях (Таблиця 4), на основі гістологічного, радіологічного або імуногістохімічного аналізу, тестові групи з HyA показали значно кращі результати в порівнянні з контрольною групою принаймні за одним з параметрів, що стосуються утворення кістки; це було незалежно від стану лунки (здорової чи інфікованої) та типу контрольного лікування.
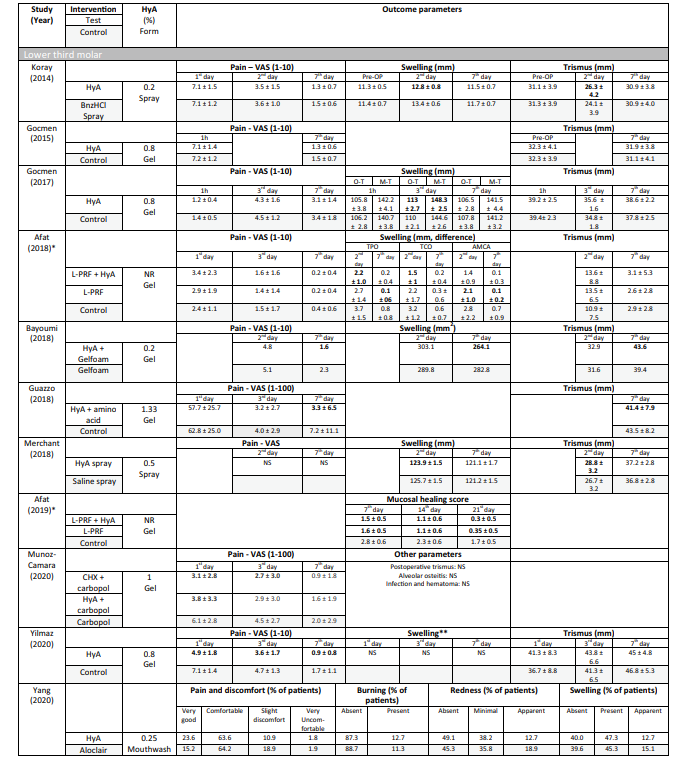
У 4 з 10 клінічних досліджень щодо хірургічного видалення LM3 (Таблиця 5), які повідомляли про біль, були зафіксовані значні переваги для тестової групи, що використовувала HyA, порівняно з контрольною групою, принаймні в одній післяопераційній точці. Аналогічно, у 4 з 7 досліджень та у 3 з 9 досліджень, які повідомляли про набряк і тризм, відповідно, були зафіксовані значні переваги на користь застосування HyA порівняно з контрольною групою. У 3 з 4 досліджень, які повідомляли про загоєння м'яких тканин після видалення регулярно прорізаних зубів, було зафіксовано значне покращення загоєння м'яких тканин після застосування HyA порівняно з контрольною групою. Крім того, одне дослідження повідомило про покращення утворення кістки через 30 днів, одне дослідження повідомило про зменшення діаметра альвеоли до 21 дня, тоді як 2 дослідження повідомили або про відсутність різниці між групами, або про значні недоліки для тестової групи, що використовувала HyA, з точки зору змін розмірів альвеоли. Нарешті, сприйняття болю було зафіксовано в 6 дослідженнях, але лише 2 дослідження повідомили про значні відмінності між групами на користь застосування HyA. Одне дослідження, що оцінювало лікування AO, повідомило про значно нижчий післяопераційний біль після застосування HyA порівняно із застосуванням алвогілю; у другому дослідженні не було контрольної групи.

Синтез результатів
Доклінічні дослідження — об'єм кістки на об'єм тканини в доклінічних випробуваннях
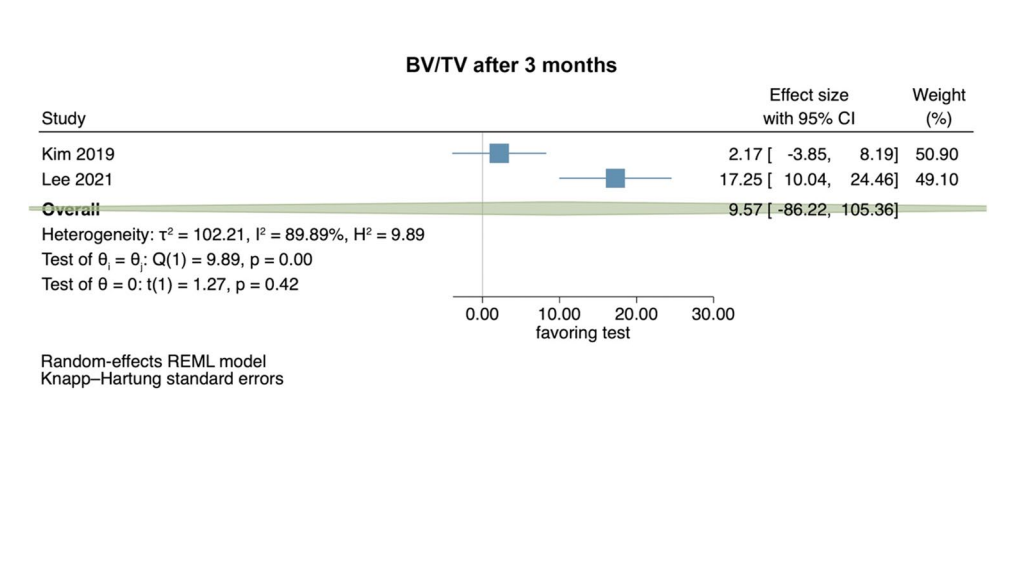
Два доклінічні дослідження надали дані для узагальнення радіографічно оціненого BV/TV через 3 місяці після операції (Рис. 1). Дослідження порівнювали застосування HyA у поєднанні з абсорбційною колагеновою губкою та абсорбційною колагеновою губкою. Загалом, значної різниці між групами не було виявлено (розмір ефекту: 9.57; 95% CI: − 86.22 до 105.36; p = 0.42), але статистична гетерогенність серед досліджень була значною (I2 = 89.89%; p < 0.01).
Клінічні дослідження — оцінка болю через 2–3 та 7 днів після хірургічного видалення LM3
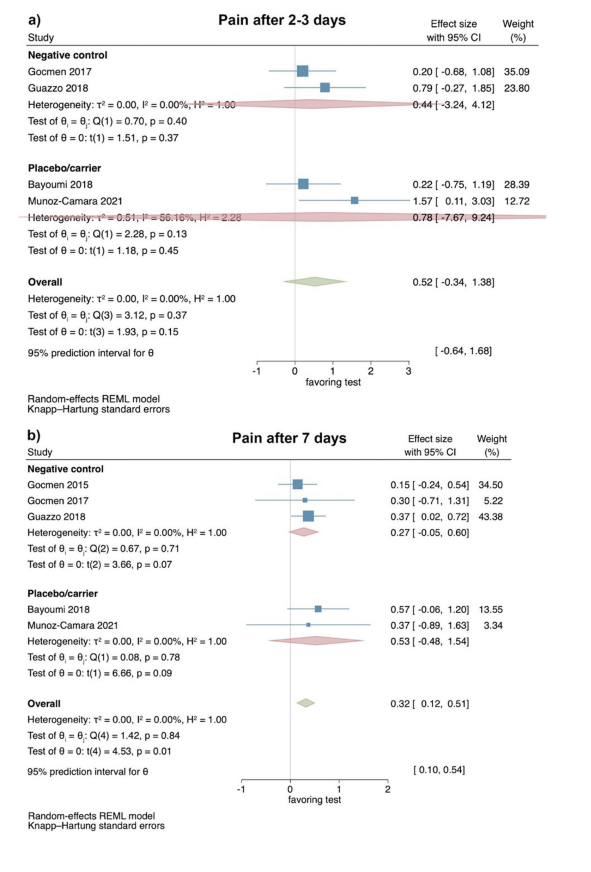
На основі результатів 4 РКД, сприйняття болю не показало статистично значущих відмінностей між тестовою та контрольними групами через 2–3 дні після операції (розмір ефекту: 0.52; 95% ДІ: − 0.34–1.38; p = 0.15), без статистичної гетерогенності серед досліджень (I2 = 0.00%; p = 0.37). Окремі аналізи з 2 дослідженнями, що порівнювали HyA з негативною контрольною групою (розмір ефекту: 0.44; 95% ДІ: − 3.24–4.12; p = 0.37) та HyA з плацебо/носієм (розмір ефекту: 0.78; 95% ДІ: − 7.67–9.24; p = 0.45) також не мали статистичної значущості (Рис. 2a).
На основі результатів 5 РКД, сприйняття болю через 7 днів після операції було значно нижчим у тестових групах, що застосовували HyA (розмір ефекту: 0.32; 95% ДІ: 0.12–0.51; p = 0.01), без статистичної гетерогенності серед досліджень (I2 = 0.00%; p = 0.84). Однак окремі аналізи не мали статистичної значущості для порівняння HyA з негативною контрольною групою (3 дослідження; розмір ефекту: 0.27; 95% ДІ: − 0.05–0.60; p = 0.07) та для порівняння HyA з плацебо/носієм (2 дослідження; розмір ефекту: 0.53; 95% ДІ: − 0.48–1.54; p = 0.09; Рис. 2b).
Клінічні дослідження—оцінка набряку через 2–3 та 7 днів після хірургічного видалення LM3
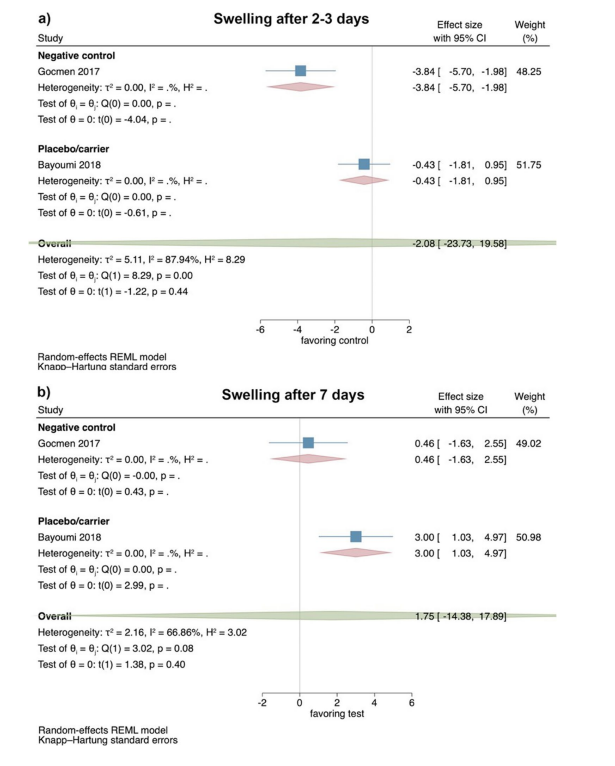
На основі результатів 2 РКД, ступінь набряку через 2–3 дні після операції не показала значної різниці між тестовою та контрольними групами (ефект: − 2.08; 95% ДІ: − 23.73–19.58; p = 0.44); однак статистична гетерогенність між дослідженнями була значною (I2 = 87.94%; p < 0.01; Рис. 3a).
Аналогічно, ступінь набряку через 7 днів після операції також не показав значної різниці між тестовими та контрольними групами (розмір ефекту: 1.75; 95% ДІ: − 14.38–17.89; p = 0.40), а статистична гетерогенність серед досліджень знову була значною (I2 = 66.86%; p = 0.08; Рис. 3b). Не було можливості провести окремий аналіз для порівняння HyA з будь-яким негативним контролем або групою плацебо/переносником через обмежену кількість досліджень.
Клінічні дослідження — оцінка тризмусу через 2–3 та 7 днів після хірургічного видалення LM3
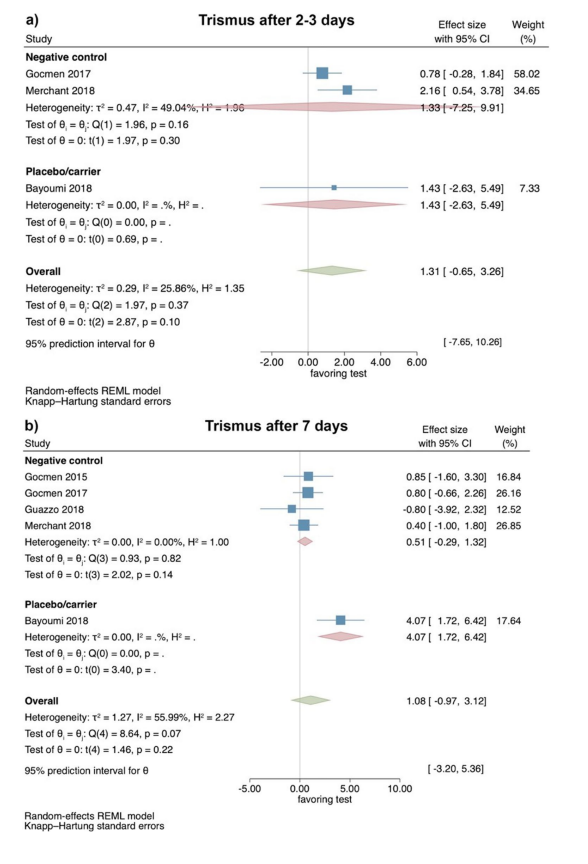
На основі результатів 3 РКД, тризмус через 2–3 дні після операції не показав значних відмінностей між тестовою та контрольними групами (розмір ефекту: 1.31; 95% ДІ: − 0.65–3.26; p = 0.10), без статистичної гетерогенності серед досліджень (I2 = 25.86%; p = 0.37). Окремі аналізи також не виявили статистичної значущості для порівняння HyA з негативною контрольною групою (2 дослідження; розмір ефекту: 1.33; 95% ДІ: − 7.25–9.91; p = 0.30), тоді як лише одне дослідження було доступне для порівняння HyA з групою плацебо/переносника (Рис. 4a).
На основі результатів 5 РКД, тризмус не показав значних відмінностей між тестовою та контрольними групами через 7 днів після операції (розмір ефекту: 1.08; 95% ДІ: − 0.97–3.12; p = 0.22); однак статистична гетерогенність серед досліджень була значною (I2 = 55.99%; p = 0.07). Окремі аналізи також не показали значних відмінностей між HyA та негативною контрольною групою (4 дослідження; розмір ефекту: 0.51; 95% ДІ: − 0.29–1.32; p = 0.14), тоді як лише одне дослідження було доступне для порівняння HyA з групою плацебо/переносника (Рис. 4b).
Оцінка ризику упередженості
Серед доклінічних досліджень, якість оцінки варіювала від 20 до 40% (Додаток 4); лише звітування про базові характеристики та інші джерела упередженості були оцінені у всіх дослідженнях як низький ризик упередженості.
Включені RCT були оцінені як такі, що мають певні занепокоєння (n = 13) або низький ризик упередженості (n = 5) (Додаток 5). Жоден з RCT не відхилився від запланованого втручання, 5 RCT були оцінені як такі, що мають певні занепокоєння в процесі рандомізації, і приблизно половина досліджень була оцінена як такі, що мають певні занепокоєння у своїй звітності щодо відсутніх даних про результати, вимірюванні результату та виборі звітних результатів. Більшість нерандомізованих досліджень були оцінені як такі, що мають низький ризик упередженості (n = 3), тоді як одне дослідження було оцінене як таке, що має певні занепокоєння (Додаток 6).
Якість доказів (GRADE)
Для результатів мета-аналізу, що включає 2 доклінічні випробування, впевненість у доказах для параметра результату BV/TV після 3 місяців була оцінена як низька (Додаток 8a).
Впевненість у доказах, отриманих з мета-аналізів, що включають клінічні випробування, була оцінена як помірна для сприйняття болю та тризмусу і як низька для оцінки набряку (Додаток 8b).
Обговорення
HyA продемонстрував протизапальні, антиедематозні, остеоіндуктивні та проангіогенетичні властивості; отже, здається, що HyA покращує загоєння ран.
Цей систематичний огляд мав на меті надати всебічну оцінку всіх доступних доказів (тобто доклінічних та клінічних) щодо впливу застосування HyA у зв'язку з видаленням зубів. Загалом, здається, що застосування HyA у зв'язку з хірургічним видаленням LM3 може позитивно вплинути на зменшення болю протягом першого післяопераційного тижня. Зокрема, мета-аналіз 5 клінічних досліджень показав, що місцеве (внутрішньохірургічне) застосування гелю HyA було пов'язане зі статистично значущим зменшенням сприйняття болю через 7 днів після операції в порівнянні з контрольною групою, в якій не було додаткової маніпуляції з раною або застосування плацебо/носія. Застосування HyA, здається, не вплинуло на інші часто виникаючі ускладнення після видалення LM3 (тобто набряк та тризм) або у зв'язку з неоперативним видаленням нормально прорізаних зубів.
Цей позитивний ефект внутрішньохірургічного застосування Гіалуронової кислоти (ГіА) на сприйняття болю протягом першого післяопераційного тижня видалення LM3 доповнює результати попереднього систематичного огляду, який також оцінював можливу користь ГіА в тій же вказівці. Зокрема, на основі іншого вибору досліджень, застосування ГіА значно зменшило біль як на 3-й, так і на 7-й післяопераційний день. Очевидно, позитивний ефект ГіА в дуже ранні післяопераційні дні, спостережений у тому огляді, не був виявлений у даному мета-аналізі, через збільшену інформацію, надану 2 додатковими дослідженнями, включеними сюди, а також через виключення нерандомізованого дослідження, яке сильно сприяло групі тестування ГіА. Позитивний ефект ГіА в плані зменшення сприйняття болю можна частково пояснити його модулюючим ефектом на запальну реакцію в хірургічному місці. Було раніше продемонстровано, що ГіА може знижувати виробництво та експресію простагландину E2, брадикініну та субстанції P, які всі беруть участь у передачі та сприйнятті болю. Проте будь-який потенційний позитивний ефект ГіА на місцеву запальну реакцію не обов'язково призводить до меншого набряку та/або тризмусу в клініці, оскільки як аналізи, включені сюди, так і ті, що в згаданому огляді, не вказали на жодні відмінності між тестовими та контрольними групами щодо цих аспектів. Однак ці результати слід інтерпретувати з обережністю через невелику кількість оригінальних досліджень та відсутність стандартизації в методах оцінки набряку обличчя, а також в самій інтервенції. Наприклад, включені дослідження рідко надавали інформацію про рівень хірургічної складності та/або застосований дизайн клаптя, аспекти, які можуть вплинути на параметри результату. Більше того, відсутність будь-якого значного позитивного ефекту ГіА на сприйняття болю при не-хірургічному видаленні регулярно прорізаних зубів, що спостерігалося в більшості досліджень (4 з 5), включених у цей огляд, не слід інтерпретувати як відсутність дії ГіА. Це може бути пов'язано з різницями в режимі загоєння, тобто «закритий» після хірургічного видалення LM3 проти «відкритого» після видалення регулярно прорізаних зубів, де відсутність первинного закриття та будь-якого носія могло призвести до швидкого виведення ГіА. Чи може застосування ГіА в носії покращити його дію, важко оцінити, оскільки це використовувалося лише в одному дослідженні, яке не показало жодних відмінностей. Проте також слід пам'ятати, що в більшості випадків, нескладне видалення зуба асоціюється з низьким рівнем болю, і тому будь-який можливий позитивний ефект ГіА може бути важко зафіксувати. Насправді, в єдиному порівняльному дослідженні з управління AO, включеному в цей огляд, було повідомлено про значне зменшення болю після операції в групах, які отримували ГіА (без первинного закриття та без використання носія).
Деякі з досліджень про загоєння після видалення регулярно прорізаних зубів, включених до цього огляду, також оцінювали можливий вплив застосування HyA на загоєння м'яких і твердих тканин. У 3 з 4 досліджень, що оцінювали загоєння м'яких тканин, було повідомлено про позитивний ефект HyA на основі часу до і/або відсотка закриття лунки, а також на основі оцінок для оцінки загоєння м'яких тканин. На відміну від цього, у 3 порівняльних дослідженнях, внутрішньо- або післяопераційне використання гелю HyA не мало жодного позитивного ефекту з точки зору змін розмірів альвеоли в порівнянні з відсутністю застосування HyA, після періоду спостереження 3-4 місяці. Насправді, в одному з досліджень, де після збереження гребеня з використанням графту лунки з колагеном, знепротеїнізованим мінералом кістки великої рогатої худоби та герметизацією лунки за допомогою колагенової матриці, гель HyA застосовувався на колагенову матрицю три рази на день протягом 1 тижня, було спостережено значно більше горизонтальної втрати кістки на корональному аспекті лунок видалення. Ці результати щодо відсутності позитивного ефекту HyA на кістку можуть здаватися дещо суперечливими з результатами, представленими в передклінічних дослідженнях, включених до цього огляду. У 2 дослідженнях, що повідомляли про загоєння неінфікованих лунок видалення у здорових або діабетичних щурів, застосування HyA значно покращило загоєння кістки в порівнянні з контрольною групою. Аналогічно, у 3 з 3 досліджень на собаках, що повідомляли про загоєння інфікованих лунок видалення, застосування HyA або самостійно, або з колагеновою губкою чи знепротеїнізованим мінералом кістки великої рогатої худоби з колагеном як носієм, покращувало загоєння кістки. Важливо зазначити, що цей позитивний ефект HyA на загоєння кістки не був продемонстрований у єдиному можливому мета-аналізі щодо BV/TV, ймовірно, через те, що обидва дослідження використовували пізній час загоєння для цієї конкретної моделі тварини; тобто, загоєння кістки всередині лунки видалення у собаки є досить просунутим після 3 місяців, навіть без будь-якого лікування. Варто зазначити, що BV/TV у групі HyA був подібний до того, що в іншій тестовій групі, лікуваній рекомбінантним людським морфогенетичним білком-2 (rhBMP-2), відомим дуже потужним агентом, що покращує кістку. Крім того, такі позитивні ефекти HyA на загоєння кістки також були продемонстровані в інших передклінічних дослідженнях, що використовують моделі дефектів критичного розміру. У перспективі жодне дослідження з хірургічного видалення LM3 не оцінювало результати загоєння на дистальному аспекті нижнього другого моляра, місці, яке часто асоціюється з глибоким пародонтальним дефектом після видалення імпактованого LM3.
Цей огляд також намагався визначити, чи може застосування HyA зменшити частоту AO після видалення зуба; однак у дослідженнях було обмежене повідомлення про цю ускладнення. У цьому контексті застосування HyA загалом вважається безпечним і без побічних ефектів; однак слід зазначити, що HyA може призвести до значних небажаних подій у разі, якщо його вводять (ін'єкція) в тканини. Тут лише одне дослідження повідомило про подовжений час кровотечі після закриття рани в порівнянні з контрольною групою; однак гемостаз вважався таким, що відповідає фізіологічному часовому інтервалу, і тому не вважався небажаною подією. Усі інші дослідження, включені в цей огляд, не згадували про будь-які побічні ефекти або ускладнення після застосування HyA. Окрім того факту, що HyA безпечно застосовувати у зв'язку з хірургічним LM3 або нехірургічним видаленням зуба, не можна зробити висновків щодо найбільш ефективної формули HyA (наприклад, низька vs. висока концентрація, не зшита vs. зшита, гель vs. спрей) або способу застосування (наприклад, з vs. без носія, частота), і тому не можна надати чітку рекомендацію.
В цілому, лише обмежена кількість добре спроектованих, рандомізованих доклінічних та клінічних досліджень могла бути ідентифікована тут і об'єднана в мета-аналіз. Більше того, як зазначено вище, існує відсутність консенсусу та інформації про деталі продуктів HyA, а також про хірургічні деталі (наприклад, рівень хірургічної складності або дизайн клаптя). Ці обмеження призвели до загальної низької або помірної впевненості в доказах. У майбутніх дослідженнях слід впровадити кращу та більш стандартизовану звітність про деталі продуктів HyA, дозування та застосування, а також довші терміни спостереження, щоб дозволити більш повну оцінку потенціалу використання HyA у зв'язку з видаленням зубів. Крім того, майбутні оновлені систематичні огляди, що включають більшу кількість досліджень, також повинні враховувати в мета-аналізах порівняння між дослідженнями з паралельними групами та дослідженнями в дизайні розділеного рота. Це було б особливо цікаво для параметрів, таких як сприйняття болю, що не є можливим тут через дуже обмежену кількість досліджень з розділеним ротом.
Висновок
Результати даного систематичного огляду та мета-аналізів показали, що внутрішньохірургічне застосування гіалуронової кислоти (HyA) у зв'язку з видаленням хірургічного LM3 призвело до значного зменшення сприйняття болю через 7 днів після операції, тоді як ранній післяопераційний біль, тризмус і ступінь набряку не змінилися. Крім того, здається, що застосування HyA може позитивно вплинути на загоєння м'яких тканин після нехірургічного видалення нормально прорізаних зубів, але, здається, не зменшує моделювання альвеолярного гребеня після видалення, хоча дані з доклінічних досліджень вказують на те, що HyA може покращити утворення кістки.
Автори: Данієль Домік, Крістіна Бертл, Тобіас Ланг, Ніколаос Пандіс, Крістіан Ульм, Андреас Ставропулос
Посилання:
- Упадхйая C, Хумагай H (2010) Поширеність сухої лунки після видалення постійних зубів у Катмандуському університеті навчального госпіталю (KUTH), Дхулікхел, Кавре, Непал: дослідження. Kathmandu Univ Med J (KUMJ) 8(29):18–24
- Акінбамі BO, Годспауер T (2014) Суха лунка: випадки, клінічні особливості та фактори ризику. Int J Dent 2014:796102
- Дуарте-Родрігес L та ін. (2018) Видалення третього моляра та його вплив на якість життя: систематичний огляд та мета-аналіз. Qual Life Res 27(10):2477–2489
- Халабі D та ін. (2018) Хлоргексидин для профілактики альвеолярного остеїту: рандомізоване клінічне дослідження. J Appl Oral Sci 26:e20170245
- Кан KW та ін. (2002) Залишкові пародонтальні дефекти дистально від другого моляра нижньої щелепи через 6–36 місяців після видалення враженого третього моляра. J Clin Periodontol 29(11):1004–1011
- Пенг KY та ін. (2001) Пародонтальний статус другого моляра нижньої щелепи після видалення третього моляра. J Periodontol 72(12):1647–1651
- МакБет N та ін. (2017) Зміни жорстких і м'яких тканин після збереження альвеолярного гребеня: систематичний огляд. Clin Oral Implants Res 28(8):982–1004
- Табернер-Вальверду M та ін. (2015) Ефективність різних методів управління сухою лункою: систематичний огляд. Med Oral Patol Oral Cir Bucal 20(5):e633–e639
- Табернер-Вальверду M, Санчес-Гарсес M, Гей-Ескода C (2017) Ефективність різних методів профілактики сухої лунки та аналіз факторів ризику: систематичний огляд. Med Oral Patol Oral Cir Bucal 22(6):e750–e758
- Хан W та ін. (2022) Протизапальна активність олігосахаридів гіалуронової кислоти специфічного розміру. Carbohydr Polym 276:118699
- Гарріс LG, Річардс RG (2004) Адгезія Staphylococcus aureus до різних оброблених титанових поверхонь. J Mater Sci Mater Med 15(4):311–314
- Романо CL та ін. (2017) Гіалуронова кислота та її композити як місцевий антимікробний/антиадгезивний бар'єр. J Bone Jt Infect 2(1):63–72
- Матheus HR та ін. (2021) Асоціація гіалуронової кислоти з депротенізованим бичачим графтом покращує кістковий ремонт та збільшує утворення кістки в дефектах критичного розміру. J Periodontol 92(11):1646–1658
- Юн J, Лі J, Ха CW та ін. (2021) Вплив 3D-друкованого каркаса з полілактичної кислоти з гіалуроновою кислотою та без неї на регенерацію кістки. J Periodontol 1–11. https://doi.org/10.1002/JPER.21-0428
- Шираката Y та ін. (2021) Загоєння пародонтальних ран/регенерація двостінних внутрішньокісткових дефектів після реконструктивної хірургії з використанням крос-зв'язаного гіалуронового гелю з або без колагенової матриці: доклінічне дослідження на собаках. Quintessence Int 0(0):308–316
- Шираката Y та ін. (2021) Загоєння букових ясенних рецесій після лікування лише з використанням коронально просунутого клаптя або в комбінації з крос-зв'язаним гіалуроновим гелем. Експериментальне дослідження на собаках. J Clin Periodontol 48(4):570–580
- Марія де Соуза G та ін. (2020) Ефективність гіалуронової кислоти в контролі болю, набряку та тризмусу після видалення третіх молярів: систематичний огляд та мета-аналіз. J Oral Maxillofac Surg 14:14
- де Вріс R та ін. (2015) Протокол для підготовки, реєстрації та публікації систематичних оглядів досліджень втручань на тваринах. Evid-Based Preclin Med 2:e00007
- Пейдж MJ та ін. (2021) Заява PRISMA 2020: оновлені рекомендації для звітування про систематичні огляди. Syst Rev 10(1):89
- Хуійманс CR та ін. (2014) Інструмент SYRCLE для оцінки ризику упередженості в дослідженнях на тваринах. BMC Med Res Methodol 14:43
- Стерн JAC та ін. (2019) RoB 2: переглянутий інструмент для оцінки ризику упередженості в рандомізованих випробуваннях. BMJ 366:l4898
- Стерн JA та ін. (2016) ROBINS-I: інструмент для оцінки ризику упередженості в нерандомізованих дослідженнях втручань. BMJ 355:i4919
- Хіггінс JPT, Томпсон SG, Спігельхалтер DJ (2009) Повторна оцінка мета-аналізу з випадковими ефектами. J R Stat Soc A Stat Soc 172(1):137–159
- Вей D та ін. (2016) Використання підходу GRADE в систематичних оглядах досліджень на тваринах. J Evid Based Med 9(2):98–104
- Чен H та ін. (2015) Як використовувати gradepro gdt для оцінки якості доказів у систематичних оглядах досліджень втручань: Вступ. Chin J Evid Based Med 15:600–606
- Мендес RM та ін. (2010) Вплив одношарових вуглецевих нанотрубок та їх функціоналізації натрієвою гіалуронатою на кістковий ремонт. Life Sci 87(7–8):215–222
- Капітан M та ін. (2021) Первинне спостереження факторів, що заважають лікуванню альвеолярного остеїту з використанням гіалуронової кислоти з октенідином - серія клінічних випадків. Biomolecules 11(8):04
- Мартінс-Юніор PA та ін. (2016) Оцінка функціоналізованих вуглецевих нанотрубок натрієвою гіалуронатою в запальних процесах для застосувань у регенеративній медицині рота. Clin Oral Invest 20(7):1607–1616
- Катандзано O та ін. (2018) Композитні спонжі з альгінату-гіалуронану для доставки транексамової кислоти в постекстракційні альвеолярні рани. J Pharm Sci 107(2):654–661
- Мендес RM та ін. (2008) Натрієва гіалуронат прискорює процес загоєння в лунках зубів щурів. Arch Oral Biol 53(12):1155–1162
- Са MA та ін. (2013) Вуглецеві нанотрубки, функціоналізовані натрієвою гіалуронатою, відновлюють кістковий ремонт у лунках діабетичних щурів. Oral Dis 19(5):484–493
- Кім JJ та ін. (2016) Гіалуронова кислота покращує утворення кістки в лунках видалення з хронічною патологією: пілотне дослідження на собаках. J Periodontol 87(7):790–795
- Кім JJ та ін. (2019) Біомодифікація компрометованих лунок видалення з використанням гіалуронової кислоти та rhBMP-2: експериментальне дослідження на собаках. J Periodontol 90(4):416–424
- Лі JB та ін. (2021) Впливи гіалуронової кислоти та депротенізованого бичачого мінералу з 10% колагеном для збереження гребеня в компрометованих лунках видалення. J Periodontol 23:23
- Корай M та ін. (2014) Ефективність спрею з гіалуроновою кислотою на набряк, біль і тризмус після хірургічного видалення вражених третіх молярів. Int J Oral Maxillofac Surg 43(11):1399–1403
- Гокмен G та ін. (2015) Антиоксидантна та протизапальна ефективність гіалуронової кислоти після видалення третього моляра. J Craniomaxillofac Surg 43(7):1033–1037
- Гокмен G та ін. (2017) Впливи гіалуронової кислоти на кровотечу після видалення третього моляра. J Appl Oral Sci 25(2):211–216
- Афат İM, Акдоган ET, Гонул O (2018) Впливи фібрину, багатого лейкоцитами та тромбоцитами, самостійно та в комбінації з гіалуроновою кислотою на біль, набряк і тризмус після хірургічного видалення вражених третіх молярів. J Oral Maxillofac Surg 76(5):926–932
- Баюм A, Надершах M, Альбандар A, Альсулаіміані B, Санкур I та ін. (2018) Вплив крос-зв'язаного гіалуронату в хірургічному видаленні вражених третіх молярів. Int J Dent Oral Health 4(2). https://doi.org/10.16966/2378-7090.254
- Гуазо R та ін. (2018) Вплив на загоєння ран топічного гелю, що містить амінокислоти та натрієву гіалуронат, застосованого до альвеолярної лунки після видалення третього моляра нижньої щелепи: подвійне сліпе рандомізоване контрольоване дослідження. Quintessence Int 49(10):831–840
- Мерчант R та ін. (2018) Порівняльна оцінка клінічної ефективності спрею з гіалуроновою кислотою та спрею з фізіологічним розчином на набряк, біль і тризмус після хірургічного видалення враженого третього моляра – рандомізоване контрольоване дослідження з розділеним ротом. Int J Sci Res 7:152
- Афат IM, Акдоган ET, Гонул O (2019) Впливи фібрину, багатого лейкоцитами та тромбоцитами, самостійно та в комбінації з гіалуроновою кислотою на раннє загоєння м'яких тканин після хірургічного видалення вражених третіх молярів: проспективне клінічне дослідження. J Craniomaxillofac Surg 47(2):280–286
- Муньйоз-Камара D, Пардо-Самора G, Камачо-Алонсо F (2020) Післяопераційні ефекти внутрішньоальвеолярного застосування 0,2% хлоргексидину або 1% гелів з гіалуроновою кислотою після видалення третього моляра нижньої щелепи: подвійне сліпе рандомізоване контрольоване клінічне дослідження. Clin Oral Investig 24:24
- Йілмаз N та ін. (2017) Ефективність гіалуронової кислоти в лунках після видалення вражених третіх молярів: пілотне дослідження. Niger J Clin Pract 20(12):1626–1631
- Ян H та ін. (2020) Дослідження непогіршення ефективності двох продуктів гіалуронової кислоти в лунках після видалення вражених третіх молярів. Maxillofac Plast Reconstr Surg 42(1):40
- Фавія G та ін. (2008) Прискорене загоєння ран м'яких тканин рота та ангіогенний ефект, викликаний пулом амінокислот, поєднаних з натрієвою гіалуронатою (AMINOGAM®). J Biol Regul Homeost Agents 22(2):109–116
- Баюмі AM, Ян A, Амуді WA, Шакір M (2015) Впливи використання гіалуронової кислоти на лунки видалення. Int J Dent Oral Health 2(1). https://doi.org/10.16966/2378-7090.157
- Алкантара CEP та ін. (2018) Гіалуронова кислота прискорює кістковий ремонт у людських зубних лунках: рандомізоване тричі сліпе клінічне дослідження. Braz Oral Res 32:e84
- Лоренц J та ін. (2018) Ін'єкційний матеріал для заміни кістки на основі бета-TCP та гіалуронану досягає повної регенерації кістки, проходячи майже повну деградацію. Int J Oral Maxillofac Implants 33(3):636–644
- Марін S та ін. (2020) Результат лікування гіалуроновою кислотою на загоєння ран після видалення у пацієнтів з погано контрольованим діабетом 2 типу: рандомізоване контрольоване дослідження з розділеним ротом. Med Oral Patol Oral Cir Bucal 25(2):e154–e160
- Мостафа D та ін. (2021) Вплив гелю гіалуронової кислоти на загоєння простих лунок видалення зубів: пілотне дослідження. Open Access Maced J Med Sci 9(D):190–195
- Екхут C та ін. (2022) Рандомізоване контрольоване дослідження, що оцінює гель гіалуронової кислоти як агента для загоєння ран у збереженні альвеолярного гребеня. J Clin Periodontol 49(3):280–291
- Косола S, Олдойні G, Боккуцці M, Джаммарінаро E, Геновесі A, Ковані U, Маркончіні S (2022) Формула, збагачена амінокислотами, для післяопераційного догляду за лунками видалення, оцінена за допомогою 3D внутрішньоротового сканування. Int J Environ Res Public Health 19(6):3302. https://doi.org/10.3390/ijerph19063302
- Кочеро N та ін. (2019) Ефективність натрієвої гіалуронат та синтетичних амінокислот у постекстракційних лунках у пацієнтів з печінковою недостатністю: дослідження з розділеним ротом. J Biol Regul Homeost Agents 33(6):1913–1919
- Дубовіна D та ін. (2016) Використання гіалуронової та амінокапронової кислоти в лікуванні альвеолярного остеїту. Військово-санітарний огляд 73(11):1010–1015
- Суханек J, Іванчакова RK, Моттл R, Браун KZ, Пілнейова KC, Пілбаурова N, Шмідт J, Суханкова Клеплова T (2019) Медичний пристрій на основі гіалуронової кислоти для лікування альвеолярного остеїту - клінічне дослідження. Int J Environ Res Public Health 16:3698. https://doi.org/10.3390/ijerph16193698
- Блум IR (2002) Сучасні погляди на суху лунку (альвеолярний остеїт): клінічна оцінка стандартизації, етіопатогенезу та управління: критичний огляд. Int J Oral Maxillofac Surg 31(3):309–317
- Лі J-B, Чу S, Амара HB та ін. (2021) Впливи гіалуронової кислоти та депротенізованого бичачого мінералу з 10% колагеном для збереження гребеня в компрометованих лунках видалення. J Periodontol 1–12. https://doi.org/10.1002/JPER. 20-0832
- Са MA та ін. (2013) Вуглецеві нанотрубки, функціоналізовані натрієвою гіалуронатою, відновлюють кістковий ремонт у лунках діабетичних щурів. Oral Dis 19(5):484–493
- Марін S та ін. (2020) Результат лікування гіалуроновою кислотою на загоєння ран після видалення у пацієнтів з погано контрольованим діабетом 2 типу: рандомізоване контрольоване дослідження з розділеним ротом. Medicina Oral, Patologia Oral y Cirugia Bucal 25(2):e154–e160
