Клінічне використання лазера Er,Cr:YSGG в ендодонтичній терапії
Машинний переклад
Оригінальна стаття написана мовою EN (посилання для прочитання) .
Повна ліквідація бактерій з інфікованих систем кореневих каналів залишається найважливішою метою ендодонтичної терапії. Однак, незважаючи на безліч нових продуктів і технік, досягти цієї мети продовжує бути складним завданням для нашої професії. Історично ендодонтичне лікування зосереджувалося на дезінфекції кореневих каналів з "захороненням" залишкових бактерій у дентинних канальцях та недоступних ділянках системи кореневих каналів. Хоча багато факторів були пов'язані з етіологією ендодонтичних невдач, стало очевидно, що ці "захоронені" бактерії відіграють ключову роль у збереженні ендодонтичної хвороби.
Хоча вражаючі результати були отримані in vitro, енергія лазера сама по собі не змогла досягти повного знищення бактерій у видалених зубах. З клінічної точки зору очевидно, що для стерилізації систем кореневих каналів потрібна комбінація різних методів лікування. Крім того, існує багато клінічних перешкод, які ще більше ускладнюють здатність лікаря досягти цієї мети. До них відносяться, але не обмежуються: обмежений ендодонтичний доступ, складна анатомія кореневих каналів, обмеження технік зрошення та інструментування, нездатність захоронити бактерії та нездатність досягти і знищити бактерії глибоко в структурі зуба.
Хоча метою цієї статті є зосередження на клінічному використанні лазера Er,Cr:YSGG з радіальними насадками, необхідно мати чіткий протокол лікування, щоб зменшити бактеріальне навантаження в каналі перед використанням лазера та полегшити доставку лазерної енергії до найкритичнішої частини кореневого каналу, апікальної третини.
Лазер ербієвого, хромованого йтрію, скандію, галію та гранату (Er,Cr:YSGG) випромінює на довжині хвилі 2,780 нм і добре поглинається водою. Чим менша глибина проникнення у воду або тканину (або чим вища абсорбція), тим більша здатність лазера різати або аблатувати тканину (Рис. 1). Оскільки ця довжина хвилі дуже схожа на максимум абсорбції води в гідроксиапатиті, фотоеабляція відбувається там, де вода випаровується миттєво, тим самим аблатуючи навколишню тканину. Гордона та ін. виявили, що можливо досягти розширення та колапсу внутрішньотрубної води на глибину до 1,000 мкм або більше. Ця абсорбція, викликана мікропульсом, була здатна виробляти акустичні хвилі, достатньо сильні, щоб порушити та знищити внутрішньотрубні бактерії.
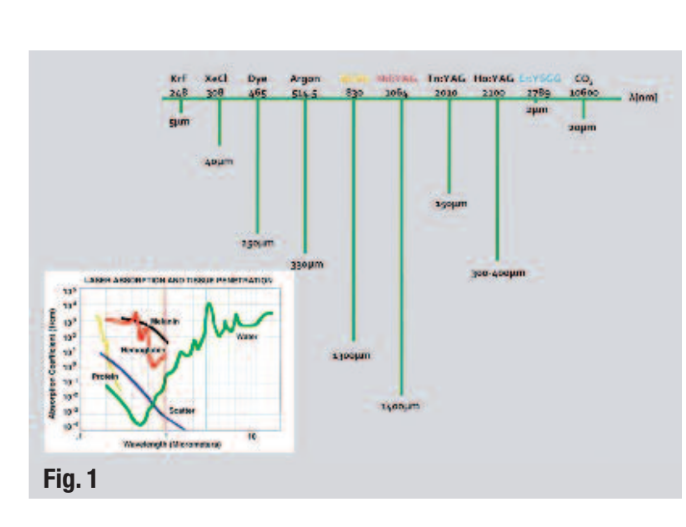
Ці результати є значущими, оскільки бактерії були виявлені на глибинах 1000 мкм, з E. faecalis на глибинах 800 мкм. Іриганти, такі як натрію гіпохлорит, мають обмежений вплив на ці бактерії з глибиною проникнення лише 100 мкм. Нещодавно було виявлено, що збільшення концентрації, часу експозиції та температури покращує проникнення NaOCl.
Обіцяючі показники знищення бактерій за допомогою лазера Er,Cr:YSGG з радіальними насадками були зафіксовані в видалених зубах. Зниження дезінфекції на 99,7% було досягнуто для E. faecalis на глибинах 200 мкм у дентині та 94,1% (1 лог) на глибинах 1,000 мкм.
Розробка радіальної лазерної насадки (Biolase Technology, Inc.) з формою насадки, яка випромінює лазерну енергію у вигляді широкого конуса, забезпечує кращий охоплення стінок кореневих каналів, ніж насадки з кінцевим випромінюванням (Рис. 2). Це полегшує проникнення випромінюваної лазерної енергії в дентинові канальці, досягаючи бактерій, які проникли глибоко в дентин.
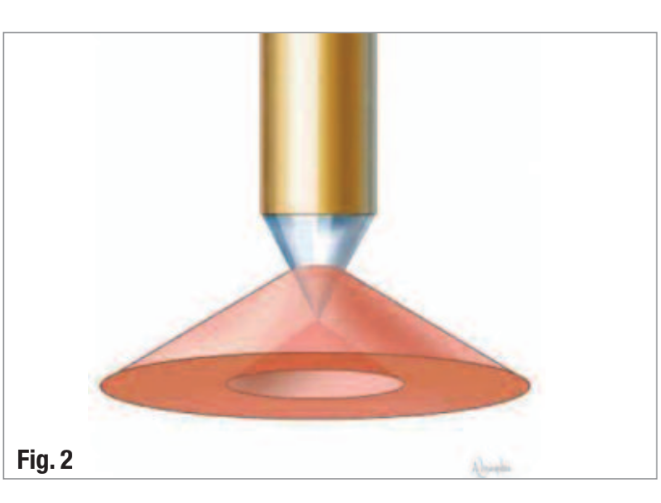
Протокол лікування
Сучасні техніки, що включають ручні та/або ротаційні інструменти, полив під позитивним тиском, з або без сонічної та ультразвукової агітації, не забезпечують повної дезінфекції каналу. Протокол лікування, представлений у цій статті, включає три основні компоненти: управління робочою шириною кореневого каналу, полив апікальної частини під негативним тиском та лазерну терапію всередині каналу.
Управління робочою шириною
Робоча ширина (РШ) кореневого каналу - це діаметр каналу безпосередньо перед його апікальним звуженням. Аллен виявив, що 97 % каналів, які не були очищені до їх РШ, мали залишкові забруднення в критичній апікальній зоні, тоді як 100 % тих, що були очищені до їх РШ, були вільні від забруднень на відстані 1 мм від апікального звуження. Дослідження показали, що нам потрібно очищати до більших розмірів, щоб видалити бактерії та забруднення. Звичайні конусні файли не можуть цього досягти без переміщення каналу, створення смугових перфорацій, ослаблення зуба або розділення інструментів. Файл LightSpeed LSX (Discus Dental) є унікальним, надзвичайно гнучким, безконусним інструментом з NiTi, здатним очищати до РШ. Остаточний апікальний розмір - це розмір інструмента, який завершує підготовку РШ і визначається, коли файл LSX застряє на відстані 4 мм (або більше) від робочої довжини (РД), і вимагає сильного натиску, щоб досягти РД. Індивідуально створені апікальні підготовки є критично важливими для передбачувано успішної ендодонтії та надають значні переваги:
- ефективне видалення інфікованого матеріалу, сміття, запаленої та некротичної тканини з апікального регіону;
- дозволяє розміщення іригуючої голки на WL для негативного тиску апікальної ірригації;
- сприяє розміщенню внутрішньоканальної медикації глибше в каналі;
- та сприяє розміщенню радіально-стріляючого лазерного наконечника в межах 1 мм від WL.
Негативний тиск апікальної ірригації
Існує дві основні причини, чому іригуючі засоби не досягають критичних останніх 3 мм кореневого каналу. По-перше, при використанні ірригації з позитивним тиском з боковою вентиляційною голкою мало що промивається за глибиною голки. Більшість іригуючого засобу слідує шляхом найменшого опору і виходить з каналу, при цьому апікальне промивання проникає лише на 1-2 мм апікально від кінця голки. Щоб досягти ефективного апікального промивання, наконечник голки потрібно розмістити на відстані 1 мм від WL, що значно підвищує ризик нещасного випадку з натрію гіпохлоритом.
По-друге, наявність апікального парового замка від повітря, що застрягло в каналі, а також аміаку і вуглекислого газу, що вивільняються внаслідок розчинної дії гіпохлориту натрію на пульпову тканину, заважає проникненню іригентів у апікальну третину. Цей паровий замок не можна усунути ручними або ротаційними файлами, сонічною або ультразвуковою активацією. У недавньому дослідженні паровий замок призвів до «значного накопичення сміття та залишків змащувального шару» в апікальних 0,5 до 1,0 мм закритих систем кореневих каналів.
EndoVac (Discus Dental) є справжньою системою іригації з апікальним негативним тиском, яка забезпечує безперервну, високу подачу свіжих рідин до терміна каналу з одночасним евакуацією. Вона складається з головного насадка для подачі (Рис. 3), який подає рідину до пульпової камери, та макро- і мікроканули (Рис. 4), які відводять рідину з камери до терміна каналу шляхом евакуації.
Ця система усуває парову блокаду та забезпечує відмінне очищення, дезінфекцію та видалення шару забруднень, практично усуваючи загрозу нещасного випадку з натрію гіпохлоритом. У порівнянні з іригацією під позитивним тиском з голкою ProRinse, EndoVac виробляв канали, які були на 366% та 671% чистішими на відстані 1 та 3 мм від WL відповідно.
Коли EndoVac використовувався в поєднанні з інструментами LightSpeed LSX, канали були на 99 і 99,5 % вільні від сміття на відстані 1 і 3 мм від робочої довжини, відповідно.
Лазерна терапія всередині каналу
Остаточний етап підготовки та дезінфекції кореневих каналів завершується за допомогою лазера Waterlase MD (Er,Cr:YSGG) з використанням радіально-стріляючих наконечників (Biolase Technology).
Лазерні наконечники доступні в двох розмірах: RFT2 і RFT3 з діаметрами 275 і 415 мкм, відповідно (Рис. 5). Наконечник RFT2 вставляється на 1 мм коротше від робочої довжини, вимагаючи розмірів підготовки каналу ISO 30 або більше, тоді як наконечник RFT3 вставляється до з'єднання середньої та апікальної третини, вимагаючи розмірів каналу ISO 45 або більше. Ці розміри добре відповідають типовим робочим ширинам підготовки, підготовленим за допомогою файлів LSX. Лазерна терапія всередині каналу виконується в два етапи: етап очищення для видалення шламу та сміття, та етап дезінфекції для абляції тканин та усунення бактерій.

Фаза очищення (1.25 Вт; 50 Гц; 24 % повітря; 30 % води)
Ця фаза використовує воду та видаляє шламовий шар і сміття без використання хімічних іригантів. Це займає від двох до трьох хвилин на канал і використовує гідро-фотоніку для створення потужного мікро-агітаційного ефекту по всій системі каналу.
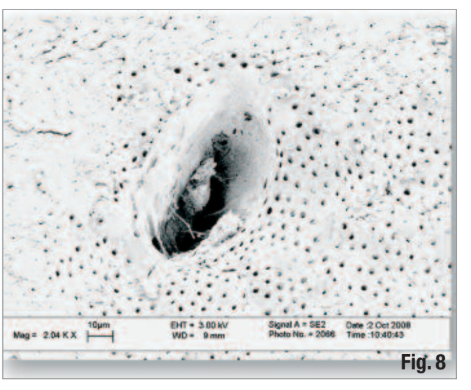
Загалом вважається, що видалення шламового шару сприяє очищенню та дезінфекції дентинних канальців і покращує герметизацію кореневого каналу. При об'єднанні результатів двох досліджень, Er,Cr:YSGG з радіальними наконечниками забезпечив значно краще видалення шламового шару в апікальній, середній та корональній третинах, ніж дві ротаційні техніки. Ця надзвичайно ефективна дія відкриває дентинні канальці, бічні канали та ізмуси в підготовці до дезінфекції (Рис. 6–8).


Техніка очищення після завершення доступу, підготовки робочої ширини та зрошення з негативним тиском:
- використовуйте RFT2 для виконання очищення апікальної та часткової корональної двох третин;
- виберіть рекомендовані налаштування лазера в режимі зволоження;
- заповніть канал стерильним розчином;
- вставте наконечник RFT2 на 1 мм коротше від WL;
- активуйте лазер при витягуванні наконечника коронально зі швидкістю приблизно 1 мм/с і підтримуйте наконечник у контакті з бічною поверхнею стінки каналу протягом всього проходу від апікальної до корональної частини;
- повторіть кроки 4 і 5 один або два рази, щоб переконатися, що весь внутрішній канал очищено (Рис. 9);
- вставте наконечник RFT3 в ручку для виконання остаточного очищення корональної двох третин;
- заповніть канал стерильним розчином;
- вставте наконечник до з'єднання апікальної та середньої третини кореневого каналу; та
- повторіть кроки 5 і 6.
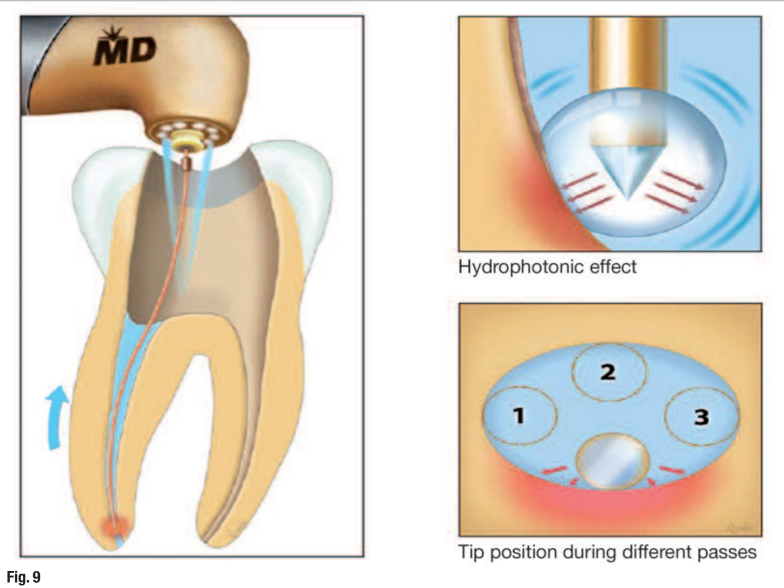
Фаза дезінфекції (0.75 Вт; 20 Гц; 10 %повітря; 0 %води)
Як було зазначено раніше, лазерна енергія, що випромінюється лазером Er,Cr:YSGG, сильно поглинається водою в тканинах і мікроорганізмах, що призводить до миттєвої фотоабляції. Крім того, внаслідок мікропульсового розширення та колапсу внутрішньотрубної води виникають акустичні хвилі, які достатньо сильні, щоб порушити та знищити внутрішньотрубні бактерії. Цей ефект є найбільш ефективним у сухому режимі, оскільки лазерна енергія не поглинається водяним спреєм і може проявити свій повний ефект на бактерії. Це було підтверджено Гордоном та ін., які досягли 99.7 % рівня знищення E. faecalis у сухому режимі. Техніка для фази дезінфекції така ж, як і для фази очищення, але з іншими налаштуваннями лазера в сухому режимі.
Клінічні застосування
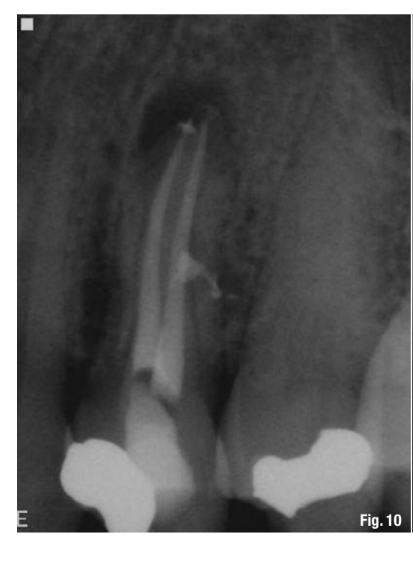
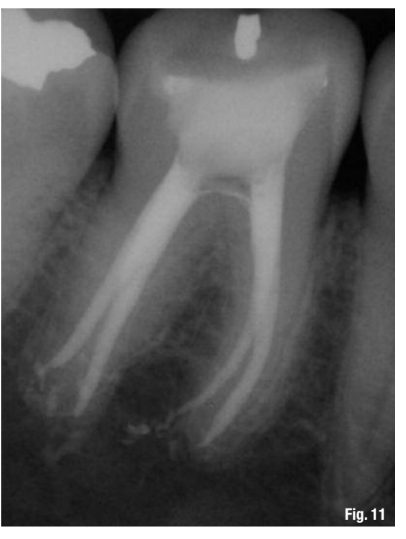
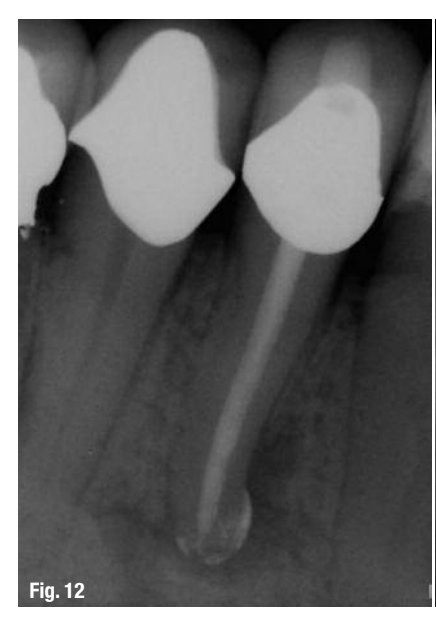
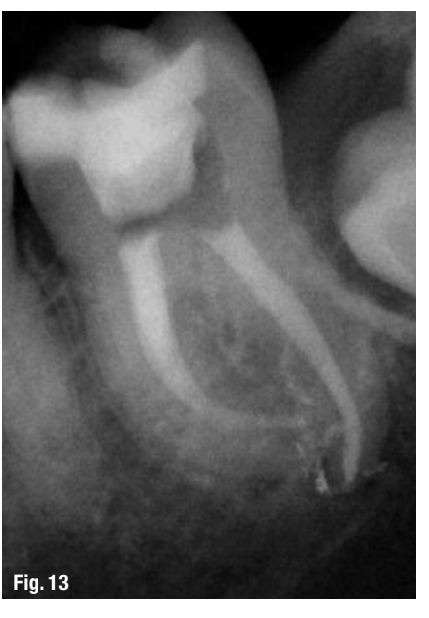
Хоча цей протокол рекомендований для всіх ендодонтичних лікувань (Рис. 10–13), він є найбільш цінним у наступних клінічних ситуаціях:
- інфіковані випадки з апікальними, латеральними та/або фуркальними радіолюцентностями;
- повторні лікування з періапікальною пародонтитом;
- гостро запалені випадки, особливо ті, що діагностовані з синдромом тріснутого зуба;
- внутрішня та зовнішня резорбція;
- постійні інфекції, що не піддаються традиційному ендодонтичному лікуванню; та
- незрозумілий, тривалий післяопераційний дискомфорт.
Резюме
Описано протокол очищення, формування та дезінфекції кореневих каналів, який максимізує видалення тканин, сміття, шару забруднень та бактерій з систем кореневих каналів. Використовуючи комбінацію управління робочою шириною з інструментами LightSpeed LSX, поливу з високим об'ємом з негативним тиском на верхівці та евакуації з системою EndoVac, а також внутрішньоканальну лазерну терапію з радіальними насадками за допомогою лазера WaterlaseMD, можливість усунення бактерій з інфікованих систем кореневих каналів може незабаром стати реальністю.
Посилання:
- Siqueira JF, Rocas IN: Клінічні наслідки та мікробіологія бактеріальної стійкості після лікувальних процедур. J Endod. 2008;34(11):1291–1301.
- Gordon W, Atabakhsh VA, Meza F, Doms A, Nissan R, Rizoiu I, Stevens R: Антимікробна ефективність лазера ербію, хрому: іттрій-скандій-галлій-гранат з радіальними випромінювальними наконечниками на стінках кореневих каналів, інфікованих Enterococcus faecalis. JADA. 2007;138(7):992–1002.
- Kouchi Y, Ninomiya J, Yasuda H, Fukui K, Moriyama T, Okamoto H: Розташування Streptococcus mutans у дентинних канальцях відкритих інфікованих кореневих каналів. J Dent Res. 1980;59:2038–46.
- Haapasalo M, Orstavik D: Інфекція та дезінфекція дентинних канальців in vitro. J Dent Res. 1987;66(8):1375–9.
- Berutti E, Marini R, Angeretti A: Здатність проникнення різних іригантів у дентинні канальці. J Endod. 1997;23:725–7.
- Zou L, Shen Y, Li W, Haapasalo M: Проникнення натрію гіпохлориту в дентин. J Endod. 2010;36(5):793–6.
- Schoop U, Barylyak A, Goharkhay K, Beer F, Wernisch J, Georgopoulos A, Sperr W, Moritz A: Вплив лазера ербію, хрому: іттрій-скандій-галлій-гранат з радіальними наконечниками на ендодонтичне лікування. Lasers Med Sci. 2007;24(1):59–65.
- Allen F: Дослідження in vivo очищення апікальної частини. General Dentistry. 2007;449–56.
- Kerekes K, Tronstad L: Морфометричні спостереження за кореневими каналами людських молярів. J Endod. 1977;3:114–8.
- Wu MK, R’oris A, Barkis D, Wesselink P: Поширеність та обсяг довгих овальних каналів в апікальній третині. OOO. 2000;89(6):739–43.
- Chow TW: Механічна ефективність іригації кореневих каналів. J Endod. 1983;9(11):475–8.
- Tay FR, Gu L, Schoeffel GL, Wimmer C, Susin L, Zhang K, Arun SN, Kim J, Looney JW, Pashley DJ: Вплив парового замка на очищення кореневих каналів за допомогою голки з боковим випуском для подачі іриганта під позитивним тиском. J Endod. 2010;36(4):745–50.
- Schoeffel J: Метод EndoVac для ендодонтичної іригації, Частина 2–Ефективність. Dentistry Today. 2008;27(1).
- Nielsen BA, Baumgartner JC: Порівняння системи EndoVac з іригацією голкою кореневих каналів. J Endod. 2007;33(5):611–5.
- Prashanth VS: Оцінка нової системи для іригації кореневих каналів у порівнянні з традиційною: ексвіво дослідження. Discus Dental, Culver City, CA: The EndoFiles Newsletter. 2008.
- Sung E, Rankin DD, Rizoiu I, Chueh P: Технологія Biolase. неопубліковане дослідження. 2008.
- Peters O, Barbakow F: Вплив іригації на сміття та слизовий шар на стінках каналу: дослідження з скануючою електронною мікроскопією. J Endod. 2000;26(1):6–10.