Варіабельність артерій скронево-нижньощелепного суглоба
Машинний переклад
Оригінальна стаття написана мовою EN (посилання для прочитання) .
Анотація
Дослідження мало на меті вивчити артеріальну варіабельність скронево-нижньощелепного суглоба (СНЩС). У цьому проспективному дослідженні варіабельність судинності вивчалася за допомогою 3D об'ємної візуалізації КТ ангіографії, включаючи випадкових пацієнтів у двох лікарнях. Було розроблено оцінювальну сітку з 16 квадрантів (A1-D4), використовуючи план Франкфурта як основну референцію. Для кожного квадранта кількість артеріальних гілок або відгалужень оцінювалася як чітко видима (2), частково видима (1) або не видима (0).
Усього було залучено 50 пацієнтів (середній вік 62.9 ± 16.0); 21 (42%) були чоловіками, а 29 (58%) жінками. Автори спостерігали двостороннє підвищення артеріальної щільності в задній частині висхідної гілки нижньої щелепи (p < 0.0001), що відповідає квадрантам B2 (5.92 ± 2.27 і 6.14 ± 2.56), B3 (9.76 ± 2.97 і 11.18 ± 2.86) та B4 (7.38 ± 2.78 і 8.10 ± 2.42). Було виявлено сильну кореляцію між кількістю судин і варіабельністю регіону (r ¼ 0.87, p ¼ 0.00001). Ніяких відмінностей між чоловіками і жінками не спостерігалося.
У межах обмежень дослідження була виявлена артеріальна варіабельність у території ТМЖ. Задня зона кондилю та рами є найбільш васкуляризованою областю, з великою варіабельністю, що представляє підвищений ризик хірургічних кровотеч. Тому це знання, здається, є особливо актуальним для хірургів, які займаються ТМЖ та іншими операціями на обличчі або радіологічними втручаннями на обличчі/мозку. Автори закликають до проведення майбутніх досліджень з включенням більших вибірок та детального вивчення артеріальних гілок у цій області.
Вступ
Анатомічні васкулярні варіації є важливою частиною медичних знань, з особливим інтересом до хірургічних та медичних спеціальностей з інтервенційними діями. У контексті голови та шиї ці васкулярні варіації можуть мати клінічні та хірургічні наслідки в різних областях, включаючи хірургію обличчя, травми обличчя, управління артеріовенозними мальформаціями, інтервенційні та судинні радіологічні процедури, реконструкції обличчя з можливими васкулярними анастомозами та косметичні втручання.
Анатомічна область скронево-нижньощелепного суглоба (СНЩС) має складну артеріальну васкуляризацію, зосереджену на гілках зовнішньої сонної артерії (ЗСА). Література не є одностайною щодо нормального розташування васкуляризації в цій території та існування артеріальних анатомічних варіацій (Туре, 2018).
У 1978 році Годлевський та ін. (1978) виявили, що кровопостачання в області СНЩС в основному здійснюється через поверхневу скроневу артерію (ПСА), передню тимпанічну артерію (ПТА) та глибоку задню скроневу артерію (ГЗСА). Глибока вушна артерія (ГВА), поперечна обличчя артерія (ПОА) та середня менінгеальна артерія (СМА) мали більшу варіацію (Годлевський та ін., 1978). Нещодавня стаття підтвердила, що кровопостачання СНЩС є циркумференційним, зробивши висновок, що всі артерії в радіусі 3 см сприяли васкуляризації СНЩС через виникнення вторинних капілярів, які розгалужуються, щоб оточити капсулу суглоба (Кучча та ін., 2013). Більше того, також було описано, що більшість васкулярного постачання, здається, походить з латерального та медіального аспектів головки кондиля. ПСА, внутрішня щелепна артерія (ВЩА), нижня альвеолярна артерія (НАА) та СМА були зображені у всіх випадках. Поперечна обличчя артерія (ПОА), масетерна артерія (МА), ПТА та кондилярна гілка ПСА були описані з частотою 70%, 60%, 60% та 50% відповідно (Кучча та ін., 2013).
Клінічний випадок від Ezure та ін. (2011) описує повну відсутність лицевої артерії (ЛА), звертаючи увагу на наслідки цієї анатомічної варіації в клінічній практиці. ЛА зазвичай використовується в хіміотерапії при раку голови та шиї, а також у мікроваскуляризованих клаптях для складних реконструкцій обличчя (Shimizu та ін., 1990); тому важливо знати анатомічні варіації цієї артерії.
Знання цих анатомічних варіацій має велике значення в хірургії TMJ, хірургії слинної залози, естетичній хірургії обличчя, інтервенційній радіології, візуалізації та реконструкціях обличчя, а також у запобіганні судинним травмам, пов'язаним з артеріальною травмою (Cillo та ін., 2005; Vesnaver, 2020; Gerbino та ін., 2021; Cooney та ін., 2020; Mao та ін., 2021).
Тривимірна (3D) візуалізація об'єму є перспективною неінвазивною технікою, що використовується для оцінки внутрішньочерепної судинності (Sparacia et al., 2007; Cascio et al., 2020). Ця техніка успішно окреслила анатомію судинного постачання скронево-нижньощелепного суглоба з хорошою роздільною здатністю та деталізацією (Cuccia et al., 2013).
Основною метою цього дослідження було проаналізувати артеріальну варіабельність в області скронево-нижньощелепного суглоба. З нашого відома, жодне попереднє дослідження не розглядало цю тему.
Дизайн дослідження
Було розроблено проспективне дослідження для аналізу артеріальної варіабельності ТМЖ у осіб, які проходили контрастну ангіографію КТ в рамках португальської програми лікування інсультів (“Via Verde do AVC”), в період з 1 грудня 2019 року по 31 січня 2020 року в нейрорентгенологічних відділеннях наступних центрів:
Центр госпітальної та університетської медицини Лісабона Центральний (CHULC) та Університетський госпіталь Сан-Жуан (CHSJ).
Дослідження було схвалено етичними комітетами та правліннями різних залучених установ (CHSJ-№ 427/19 та CHULC - 800/2019). Критерії включення та виключення з дослідження представлені в Таблиці 1.

Протокол зображення
Перша лікарня, CHULC, використовувала сканер GE LightSpeed 64 з гелікоїдним типом сканування та сканер GE BrightSpeed 16 з аксіальним типом сканування. Контрастний розчин, що використовувався під час процедури, був неіонним йодованим агентом: Іомепрол 175 г йоду. Друга лікарня, CHSJ, використовувала сканер Philips Tomoscan Brilliance 16 та два контрастні агенти: Іогексол та Іомепрол.
Аналіз артеріальної варіабельності в території ТМЖ
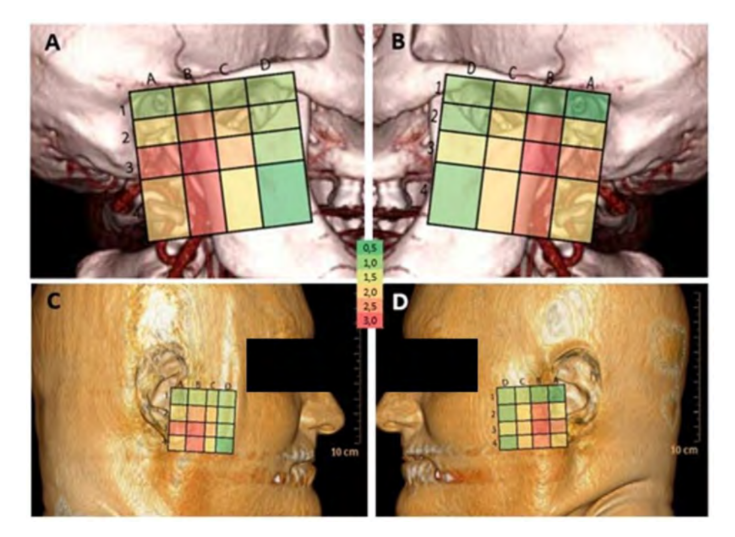
Для оцінки артеріальної анатомії темпоромандибулярної області автори розробили сітку з 16 квадрантів. Франкфуртський план (FP) (Taub, 2007) використовувався як основна референція для цих квадрантів. Друга горизонтальна лінія (b) була проведена паралельно до FP, використовуючи дотичну до сигмоїдальної виїмки як орієнтир. Третя горизонтальна лінія (c), також паралельна до FP, представляє дотичну до нижнього краю мастоїдної частини скроневої кістки. Четверта горизонтальна лінія (d), паралельна до FP, слідує за дотичною до верхньої поверхні остистого відростка хребця C2. Нарешті, остання горизонтальна лінія (a) є лінією, паралельною до FP, яка знаходиться на півдорозі між FP та другою лінією (b). Вертикальні лінії всі перпендикулярні до FP. Перша вертикальна лінія (e) є дотичною до увігнутості переднього краю висхідної гілки нижньої щелепи, друга вертикальна лінія (f) є дотичною до максимальної опуклості нижньощелепної виїмки, а третя вертикальна лінія (g) є дотичною до переднього гребеня нижньощелепного кондиля. Четверта (h) та п'ята лінії (i) є дотичними, відповідно, до переднього та заднього краю зовнішнього слухового каналу (Рис. 1).
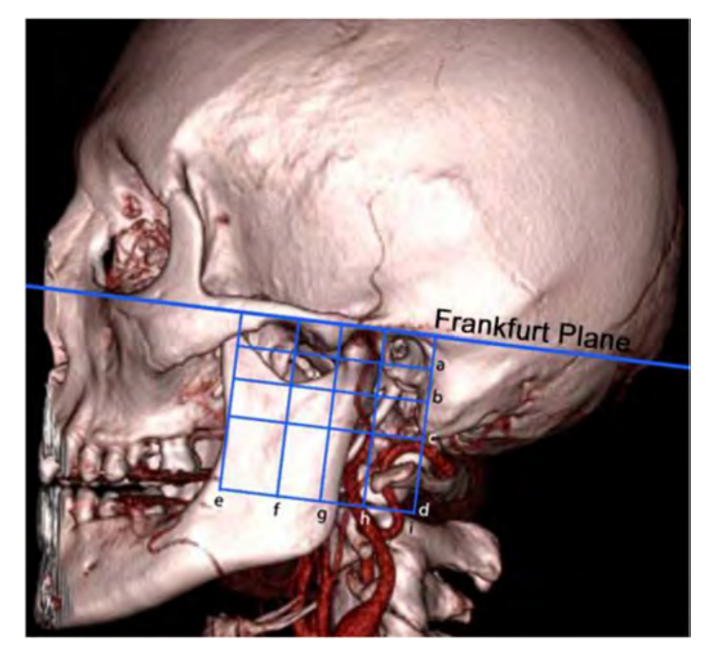
Зображення КТ у форматі DICOM були інтегровані в програмне забезпечення Horos™ та піддані 3D рендерингу з такими параметрами: для зображень, отриманих з CHULC, було встановлено рівень вікна (WL) 257, ширину вікна (WW) 296, CLUT “VR Червоні Судини (8-біт)”, непрозорість зворотної логарифмічної таблиці, стандартні тіні, без фільтра, паралельна проекція та 0% фону для червоного, зеленого та синього; для зображень, отриманих з CHSJ, було встановлено WL 140, WW 120, CLUT “VR Червоні Судини (8-біт)”, непрозорість зворотної логарифмічної таблиці, стандартні тіні, без фільтра, паралельна проекція та 0% фону для червоного, зеленого та синього. Ці параметри були обрані для імітації зовнішнього джерела світла. Це дозволило отримати зображення з більш реалістичним виглядом анатомічних структур та легше ізолювати кісткові та судинні структури (Cuccia et al., 2013).
Різні квадранти були намальовані в програмному забезпеченні, використовуючи описані посилання, і були проаналізовані індивідуально, використовуючи наступну систему класифікації: кожна артеріальна гілка, знайдена в квадранті, була категоризована як чітко видима (2 бали), частково видима/лише видима на короткій ділянці (1 бал) або не видима (0 балів) (Такігі та ін., 1998). Для кожного набору КТ-зображень індивіда були створені дві таблиці: одна для правого ТМД, а інша для лівого ТМД. Ці таблиці відповідають раніше визначеним квадрантам (Рис. 1).
Статистичний аналіз
Після артеріальної оцінки кожного квадранта було визначено число, обчисливши суму значень, присвоєних кожному судині, спостереженому в цій області. Потім для кожного квадранта з обох сторін було обчислено середнє значення та стандартне відхилення (SD). Нормальність даних була перевірена для всіх тестів. Усі тести проводилися для кожної гемілоби. Порівняння середніх значень квадрантів проводилося за допомогою тесту Крускала-Уолліса. Оскільки варіабельність безпосередньо пов'язана зі стандартним відхиленням, для кожного отриманого значення було обчислено 95% довірчий інтервал (a ¼ 0.05). Припускаючи, що "s" - це стандартне відхилення, "n" - це кількість спостережень (50 в кожному квадранті кожної гемілоби), а "a" - це рівень значущості, вважалося, що анатомічна варіабельність квадранта буде значущою з клінічної точки зору, якщо нижній межевий значення 95% довірчого інтервалу для його стандартного відхилення буде більшим за 2. Значення 2 відповідало чітко видимій артеріальній гілці або двом частково видимим судинам. Це правило називалося мінімальною варіабельністю (VM). Кореляція середніх балів зі стандартним відхиленням була отримана за допомогою тесту Пірсона. Після цього було проведено порівняльний аналіз отриманих даних між чоловіками та жінками за допомогою непараметричного тесту розподілу Манна-Уїтні. Нульова гіпотеза була визначена як відсутність статистично значущої різниці між статями, тоді як альтернативна гіпотеза була визначена як наявність цієї різниці.
Результати
У це дослідження було включено 50 пацієнтів (29 чоловіків і 21 жінка), віком від 24 до 87 років. Середній вік жінок становив 61.1 ± 18.8 (середнє ± СД), а чоловіків - 65.3 ± 11.5 (середнє ± СД).
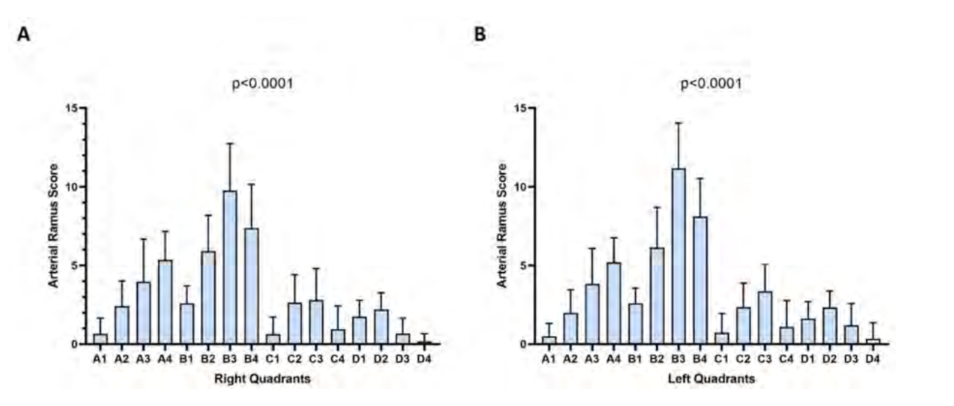
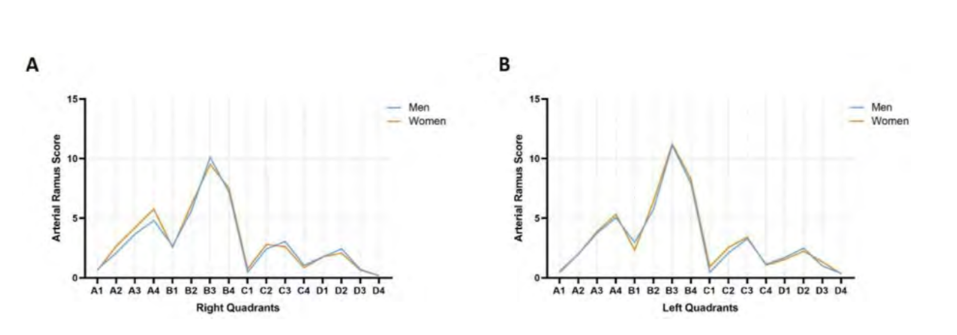
Оцінки артеріальних гілок, відповідно до системи класифікації, отримані в правій та лівій гемісфері, представлені в Рис. 2. Білатерально квадранти B3, B4 та B2 мали статистично значущу більшу судинну щільність (p < 0.0001). Також білатерально квадрант D4 мав статистично значущу знижену артеріальну щільність (p < 0.0001).
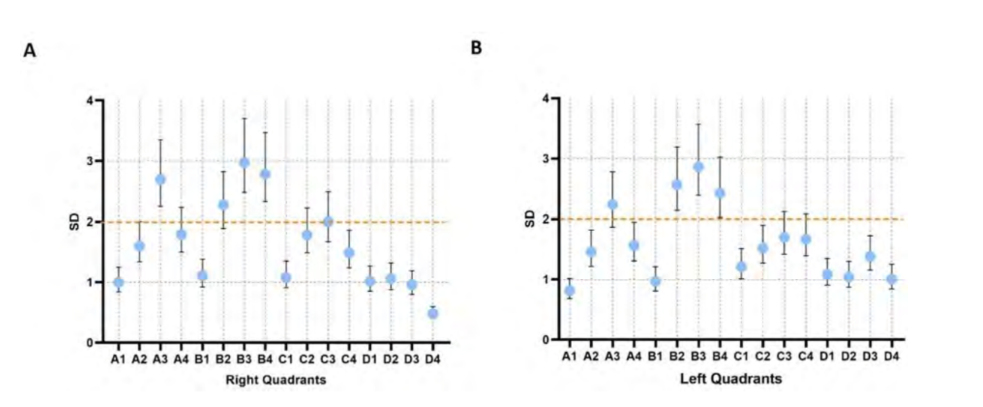
Довірчі інтервали 95% SD застосували встановлене правило VM (значення нижньої межі 95% довірчого інтервалу для його SD було більше 2 середніх балів). У правій геміфасі квадранти A3 (SD = 2.25 - 3.35), B3 (SD = 2.48 - 3.7) та B4 (SD = 2.33 - 3.47) є єдиними, які демонструють значну артеріальну варіабельність (Рис. 3A). Аналогічно, у лівій геміфасі квадранти B2 (SD = 2.14 - 3.19), B3 (SD = 2.39 - 3.57) та B4 (SD = 2.03 - 3.02) мають значну варіабельність (Рис. 3B). Довірчі інтервали квадрантів B2 (SD = 1.89 - 2.82) та A3 (SD = 1.87 - 2.78) у правій та лівій геміфасі відповідно мають значні відхилення; однак вони охоплюють значення, визначене в правилі VM, що означає, що їх варіабельність не може вважатися значною. Більше того, аналіз кореляції Пірсона між SD та оцінками артеріального гілки дозволив нам перевірити, що квадранти з більшими SD відповідають тим, що мають вищі значення артеріального гілки у правій (r = 0.87 P = 0.00001, Рис. 4A) та лівій геміфасі (r = 0.87 P = 0.00002, Рис. 4B); це вказує на те, що ці квадранти більш васкуляризовані. Аналогічно, квадранти з меншими SD мають зменшену васкуляризацію (Рис. 4).
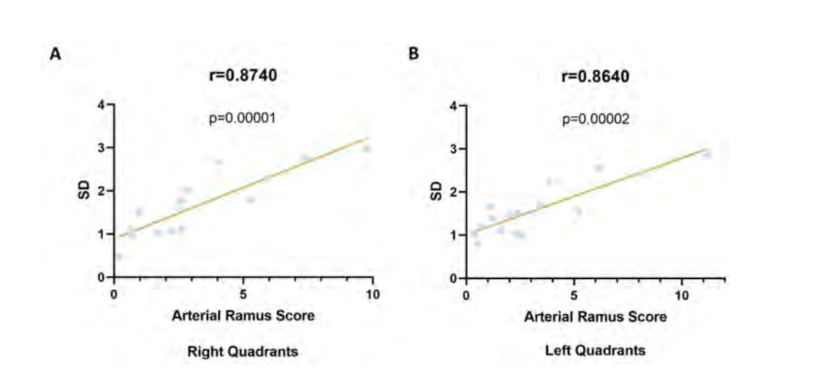
Для полегшення візуалізації варіацій кровопостачання між усіма квадрантами та анатомічними зонами, до яких вони відповідають, була створена карта (Рис. 5), де тепліші кольори відповідають більшій варіації артеріальної анатомії (вищий показник SD), а холодніші кольори відповідають меншій варіації.
Аналіз між двома статями показав, що немає значних відмінностей у варіабельності в кожному геміфасі. Значення, отримані з тесту, не дозволили відхилити нульову гіпотезу - це означає, що групи є подібними для p > 0.05 (Рис. 6).
Обговорення
СКТ є суглобом, розташованим у високоваскуляризованій області. Знання про васкулярні варіації цієї області може сприяти кращому розумінню захворювань, пов'язаних з цим суглобом, та їх лікування. Для вивчення шийно-черепно-лицевих артерій у великих (Sparacia et al., 2007) та малих калібрів (Cuccia et al., 2013) дослідженнях використовувалося 3D об'ємне моделювання. Однак аналізи розподілу кровопостачання в області СКТ є відносно рідкісними.
У даному дослідженні показано, що 3D об'ємне моделювання КТ ангіографії з використанням FP може бути ефективно використано для вивчення варіабельності артеріальних регіонів, що оточують область СКТ.
Регіони, обмежені квадрантами (B3, B4), які охоплюють задній аспект висхідного гілки нижньої щелепи, є найбільш васкуляризованими і мають більшу васкулярну варіабельність (Рис. 2 та 3). Крім того, було виявлено кореляцію між існуванням більшої кількості судин і вищою варіабельністю і навпаки (Рис. 4). Це є результатом кількох факторів. Анатомічні варіації самої нижньої щелепи (Alomar et al., 2007) та навколишніх кісткових структур можуть впливати на сприйняття васкулярних варіацій, змінюючи розташування квадрантів, створених авторами (Рис. 6). Опис односторонніх відсутностей певних судин міг бути однією з причин виявлених двосторонніх відмінностей (Ezure et al., 2011). Wasicky та Pretterklieber (2000) описали, що походження ATA варіювало в широких межах і дивно демонструвало латеральність. У тій же статті також згадуються 9 випадків, у яких ATA зображено в подвійному вигляді, а також 1 випадок з трійним представленням. Враховуючи цю інформацію, ми можемо краще зрозуміти причину більшої варіабельності, виявленої в цих квадрантах.
Анатомічна територія скронево-нижньощелепного суглоба також використовується кількома спеціальностями в їхніх хірургічних методах. З різних підходів, описаних для хірургії скронево-нижньощелепного суглоба, виділяються преаурикулярний (Tauro et al., 2020; Vesnaver, 2020; Gerbino et al., 2021; Luo et al., 2021) та ендоауральний (Assef et al., 2019); обидва вони відносно близькі до квадрантів, розглянутих у цьому дослідженні. У недавньому дослідженні хірургічних ускладнень при артроскопії скронево-нижньощелепного суглоба екстраартикулярна кровотеча в задньому проколі становила 6,1%, у порівнянні з 0% у передньому проколі, що підтверджує, що задня область має підвищений ризик кровотечі
(ÂАнджело та ін., 2021). Паротидні (Кім та ін., 2014) та деякі естетичні хірургії обличчя (Гіотакіс та ін., 2020) також передбачають розрізи в тій же території. У всіх цих хірургіях існують супутні ризики. До них відносяться анестезіологічні, інфекційні, неврологічні, отологічні та судинні ускладнення, а також інструментальні збої та запальні проблеми (Ісідо та ін., 2015). Геморагії та післяопераційні гематоми є поширеними наслідками процедур у цій високосудинній території (Гольмлунд та ін., 1985). Талебзаде та ін. (1999) повідомили, що в медіальній області ТМЖ є кілька судинних та нервових структур, що може підвищити ризик геморагії та неврологічних ушкоджень. Результати цього дослідження підкреслюють для хірургів ТМЖ, що ця область має варіабельність у кровопостачанні, і персоналізоване дослідження судинного профілю може зменшити хірургічні ускладнення.
Основними обмеженнями цього дослідження були: 1) широкий діапазон віку учасників; 2) різниця в розмірах і площі одного й того ж квадранта у різних осіб, що виникає через анатомічні відмінності в кісткових структурах, які використовуються як еталон; 3) участь програми “Via Verde do AVC” у отриманні зображень; 4) відсутність розрахунку надійності між оцінювачами та всередині оцінювачів. Програма “Via Verde do AVC”, яка діє в Португалії з 2005 року (Silva and Gouveia, 2012), застосовується до кожного пацієнта, який має ознаки цереброваскулярної аварії (CVA, інсульт) і звертається за допомогою до національних служб охорони здоров'я. Ця програма полегшила використання КТ-зображень для цього дослідження; однак вона також ускладнила як відбір, так і оцінку цих зображень. Крім того, більшість цих пацієнтів мають судинну патологію, таку як викривлення шийних артерій або атеросклеротичну стенозу каротидних біфуркацій, що може призвести до артефактів під час отримання КТ-ангиографії.
Майбутні дослідження можуть надати більш надійні дані для доповнення результатів цього дослідження шляхом збільшення розміру вибірки, охоплення різноманітної групи осіб, не запитуючи про етнічну приналежність особи з причин конфіденційності в аналізі даних, та усунення всіх можливих судинних змін через підозру на інсульт. Оскільки існує лише невелика кількість подібних досліджень, покращення будь-якого з цих факторів сприятиме отриманню більш надійних і репрезентативних результатів у майбутньому дослідженні. Зазвичай вибірка, обрана в дослідженнях того ж масштабу, є набором трупів, з тестами та оцінками, що проводяться через дисекцію анатомічних структур (Alomar et al., 2007) та гістологічний аналіз тканин (Siéssere et al., 2008).
Висновок
3D об'ємна візуалізація КТ ангіографії продемонструвала великі перспективи для оцінки артеріальної варіабельності в території скронево-нижньощелепного суглоба. Задня зона кондилю та рами є найбільш васкуляризованою областю, з великою варіабельністю, що представляє підвищений ризик хірургічної кровотечі. Хірурги скронево-нижньощелепного суглоба, серед інших, повинні бути обізнані про ці міркування, оскільки більшість хірургічних технік для скронево-нижньощелепного суглоба виконується в цій території.
Автори: Девід Фаустіно Âнгело, Жонатас Ногейра, Кароліна Пінійро, Гонсало Алвеш, Генрік Жозе Кардозо
Посилання:
- Аломар, Х., Медрано, Х., Кабратоса, Х., Клаверо, Х.А., Лоренте, М., Серра, І., Моніль, Х.М., Сальвадор, А., 2007. Анатомія скронево-нижньощелепного суглоба. Семінар. Ультразвук КТ МР 28, 170-183.
- Âнгело, Д.Ф., Араужо, Р.А.Д., Санс, Д., 2021. Хірургічні ускладнення, пов'язані з артроскопією скронево-нижньощелепного суглоба: проспективний аналіз 39 однопортальних проти 43 двопортальних процедур. Міжнародний журнал оральної та щелепно-лицевої хірургії 50, 1089-1094.
- Ассеф, К.А.Н., Карвальо, П.Х.А., Герра, Р.К., 2019. Артроскопічно асистований короткий ендоауральний підхід для анкерування диска скронево-нижньощелепного суглоба. Британський журнал оральної та щелепно-лицевої хірургії 57, 93-94.
- Каскіо, Ф., Каччіола, А., Портаро, С., Басиле, Г.А., Різзо, Г., Феліппу, А.В.Д., Феліппу, А.В.Д., Брушетта, А., Анфузо, К., Каскіо, Ф., Міларді, Д., Браманті, А., 2020. Пряме об'ємне рендеринг комп'ютерної томографії передньої етмоїдальної артерії: описове анатомічне дослідження. Міжнародний архів оториноларингології 24, e38-e46.
- Чілло-молодший, Дж.Е., Сінн, Д., Труельсон, Дж.М., 2005. Управління геморагією середньої менінгеальної та поверхневої скроневої артерії під час операції з повної заміни скронево-нижньощелепного суглоба з використанням гелевої гемостатичної речовини. Журнал черепно-лицевої хірургії 16, 309-312.
- Куні, М., О'Коннелл, Дж.Е., Весі, Дж.А., Ван Еден, С., 2020. Нескальпельне лікування дитячих та підліткових кондилів нижньої щелепи: ретроспективний огляд 49 послідовних випадків, що лікувалися в третинному центрі. Журнал черепно-максилярно-лицевої хірургії 48, 666-671.
- Кучча, А.М., Карадона, К., Карадона, Д., Анастасі, Г., Міларді, Д., Фавалоро, А., Де П'єтро, А., Ангілері, Т.М., Карадона, Л., Кутронео, Г., 2013. Артеріальне кровопостачання скронево-нижньощелепного суглоба: анатомічне дослідження та клінічні наслідки. Іміджинг Сайс Дент 43, 37-44.
- Езуре, Х., Мори, Р., Іто, Дж., Оцука, Н., 2011. Випадок повністю відсутньої лицевої артерії. Міжнародний журнал акустики та вібрацій 4.
- Гербіно, Дж., Сегура-Пальєрес, І., Рамієрі, Дж., 2021. Остеохондрома кондилю нижньої щелепи: показання до різних хірургічних методів: серія випадків 7 пацієнтів. Журнал черепно-максилярно-лицевої хірургії 49, 584-591.
- Гіотакіс, Е.І., Гіотакіс, А.І., 2020. Модифікований розріз для підтяжки обличчя та клапоть поверхневої м'язово-апоневротичної системи при злоякісності привушної залози: ретроспективне дослідження та огляд літератури. Світовий журнал хірургії онкології 18, 8.
- Годлевський, Г., Босі, Дж., Жираудон, М., Дюссо, Дж., Паварт, Дж.Ц., Лопес, Дж.Ф., 1978. Артеріальна васкуляризація скронево-нижньощелепного суглоба]. Бюлетень Асоціації анатомії 62, 229-236.
- Холмлунд, А., Хеллсінг, Г., 1985. Артроскопія скронево-нижньощелепного суглоба. Дослідження аутопсії. Міжнародний журнал оральної хірургії 14, 169-175.
- Ішіда, Й., Чоса, Е., Танігучі, Н., 2015. Псевдоаневризма як ускладнення артроскопії плеча. Хірургія коліна. Спортивна травматологія. Артроскопія 23, 1549-1551.
- Кім, Д.Й., Парк, Г.Ц., Чо, Й.В., Чхой, С.Х., 2014. Часткова поверхнева паротидектомія через ретроаурикульний розріз. Клінічний експериментальний оториноларинголог 7, 119-122.
- Луо, Х., Бі, Р., Цзян, Н., Чжу, С., Лі, Й., 2021. Клінічні результати відкритого лікування старих переломів головки кондилю у дорослих. Журнал черепно-максилярно-лицевої хірургії 49, 480-487.
- Мао, Й., Чен, Х., Сіе, Х., Сюй, В., Чжан, С., Чжан, С., 2021. Оцінка покращеного анкерного цвяха в хірургії репозиції диска скронево-нижньощелепного суглоба: проспективне дослідження 25 пацієнтів. Журнал черепно-максилярно-лицевої хірургії 3, S1010-S5182.
- Сімідзу, Т., Сакакура, Й., Хатторі, Т., Ямагучі, Н., Кубо, М., Сакакура, К., 1990. Суперселективна внутрішньоартеріальна хіміотерапія в поєднанні з опроміненням: попередній звіт. Американський журнал оториноларингології 11, 131-136.
- Сієсере, С., Вітті, М., Семпріні, М., Регало, С.Ц., Ійомаса, М.М., Діас, Ф.Й., Ісса, Дж.П., де Соуза, Л.Г., 2008. Макроскопічні та мікроскопічні аспекти скронево-нижньощелепного суглоба, пов'язані з його клінічними наслідками. Мікрон 39, 852-858.
- Сілва, С., Гouveia, М., 2012. Програма “Via verde do AVC”: аналіз впливу на смертність від інсульту (португальською). Португальський журнал громадського здоров'я 30, 172-179.
- Спарасія, Г., Бенчівінні, Ф., Банко, А., Сарно, Ч., Бартолота, Т., Лагалла, Р., 2007. Обробка зображень для КТ ангіографії шийно-черепних артерій: оцінка техніки переформатування. Ла Радіологія медична 112, 224-238.
- Такая, Р., Вестессон, П.-Л., Охаші, Й., Тогасі, Х., 1998. МР ангіографія скронево-нижньощелепного суглоба у безсимптомних добровольців. Оральна радіологія 14, 69-74.
- Талебзаде, Н., Розенштейн, Т.П., Погрел, М.А., 1999. Анатомія структур медіально до скронево-нижньощелепного суглоба. Оральна хірургія. Оральна медицина. Оральна патологія. Оральна радіологія. Ендодонтія 88, 674-678.
- Тауб, П.Й., 2007. Цефалометрія. Журнал черепно-лицевої хірургії 18, 811-817.
- Тауро, Д.П., Манай, Р.С., 2020. Нюанси хірургії анкілозу скронево-нижньощелепного суглоба: поради та хитрощі. Журнал щелепно-лицевої хірургії 19, 178-183.
- Туре, Г., 2018. Артеріальна васкуляризація кондилю нижньої щелепи та переломи кондилю. Пластична та реконструктивна хірургія 141, 718e-725e.
- Веснавер, А., 2020. Вивихнуті дитячі переломи кондилю - чи завжди слід дотримуватися консервативного лікування? Журнал черепно-максилярно-лицевої хірургії 48, 933-941.
- Васікі, Р., Преттерклібер, М.Л., 2000. Людська передня тимпанічна артерія. Живильна артерія середнього вуха з високою варіабельністю походження. Клітини Тканини Органи 166, 388-394.